解题方法
1 . 根据实验操作及现象,得出结论正确的是
| 选项 | 实验操作及现象 | 结论 |
| A |  和稀硫酸混合产生浅黄色沉淀和刺激性气味的气体 和稀硫酸混合产生浅黄色沉淀和刺激性气味的气体 | 硫酸表现氧化性, 表现还原性 表现还原性 |
| B | 向酸性 溶液中滴加乙苯,溶液褪色 溶液中滴加乙苯,溶液褪色 | 乙苯的苯环中含有碳碳双键 |
| C | Ag与HI溶液生成黄色沉淀和无色气体 |  和 和 生成AgI,促进Ag和HI溶液发生反应生成AgI和 生成AgI,促进Ag和HI溶液发生反应生成AgI和 |
| D | 在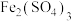 溶液中加入铜粉,溶液变蓝色 溶液中加入铜粉,溶液变蓝色 | 氧化性: , ,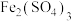 和Cu发生置换反应 和Cu发生置换反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
2 . 下列方案设计、现象和结论不正确的是
| 实验方案 | 现象 | 结论 | |
| A | 试管中依次加入3mL乙醇2mL浓硫酸、2mL乙酸及沸石后连接好装置并加热 | 饱和碳酸钠液面上出现有香味的无色油状液体 | 有酯类物质生成 |
| B | 将 液体和 液体和 固体分别暴露在潮湿空气中 固体分别暴露在潮湿空气中 | 只有前者会冒“白烟” | 相同条件下水解程度: |
| C | 室温下,将 溶液和稀 溶液和稀 混合 混合 | 溶液变浑浊且有刺激性气味的气体生成 |  既体现还原性又体现氧化性 既体现还原性又体现氧化性 |
| D | 向 溶液中加入5滴 溶液中加入5滴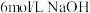 溶液 溶液 | 溶液由橙色变黄色 |  减小,平衡向 减小,平衡向 减小的方向移动 减小的方向移动 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
3 . 已知 ,在酸化的KI溶液中通入
,在酸化的KI溶液中通入 ,观察到溶液变为棕色并出现混浊,继续通入
,观察到溶液变为棕色并出现混浊,继续通入 ,直到溶液棕色恰好褪去,发生的反应分别为:
,直到溶液棕色恰好褪去,发生的反应分别为: ,
, ,下列说法错误的是
,下列说法错误的是
 ,在酸化的KI溶液中通入
,在酸化的KI溶液中通入 ,观察到溶液变为棕色并出现混浊,继续通入
,观察到溶液变为棕色并出现混浊,继续通入 ,直到溶液棕色恰好褪去,发生的反应分别为:
,直到溶液棕色恰好褪去,发生的反应分别为: ,
, ,下列说法错误的是
,下列说法错误的是A. 和水在KI的催化下可以发生氧化还原反应 和水在KI的催化下可以发生氧化还原反应 |
| B.物质的氧化性或还原性强弱与浓度有关 |
C.整个过程中被氧化的 和被还原的 和被还原的 物质的量比为1:2 物质的量比为1:2 |
| D.配制碘酒时可以加入一定量KI |
您最近一年使用:0次
名校
4 . 下列物质性质与用途具有对应关系的是
| A.FeS具有氧化性,可用于制取硫酸 |
B. 不溶于水,可以作半导体材料 不溶于水,可以作半导体材料 |
C. 具有还原性,可用于漂白某些有色物质 具有还原性,可用于漂白某些有色物质 |
D. 具有难挥发性,可用于制取挥发性酸 具有难挥发性,可用于制取挥发性酸 |
您最近一年使用:0次
解题方法
5 . 由实验操作和现象,可得出相应正确结论的是
| 实验操作 | 现象 | 结论 | |
| A | 向NaBr溶液中滴加过量氯水,再加入淀粉KI溶液 | 先变橙色,后变蓝色 | 氧化性: Cl2>Br2>I2 |
| B | 将铁锈溶于浓盐酸,再滴加酸性高锰酸钾溶液 | 高锰酸钾溶液的紫色褪去 | 铁锈中含有二价铁 |
| C | 向铬酸钾溶液中缓慢滴加硫酸 | 黄色变为橙红色 |  +H2O +H2O 2 2 +2H+,增大氢离子浓度,平衡向生成 +2H+,增大氢离子浓度,平衡向生成 和的方向移动 和的方向移动 |
| D | 向蔗糖溶液中滴加稀硫酸,水浴加热,再加入新制Cu(OH)2悬浊液 | 无砖红色沉淀 | 蔗糖未发生水解 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
6 . 一种从含砷废水[砷主要以亚砷酸(H3AsO3)形式存在]中回收砷的工艺流程如图:
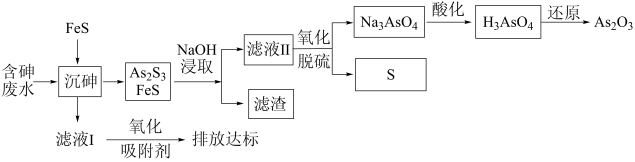
已知:
I.As2S3+6NaOH=Na3AsO3+Na3AsS3+3H2O
II.As2S3(s)+3S2-(aq) 2AsS
2AsS (aq)
(aq)
III.砷酸(H3AsO4)在酸性条件下有强氧化性,能被氢碘酸等还原
下列说法错误的是

已知:
I.As2S3+6NaOH=Na3AsO3+Na3AsS3+3H2O
II.As2S3(s)+3S2-(aq)
 2AsS
2AsS (aq)
(aq)III.砷酸(H3AsO4)在酸性条件下有强氧化性,能被氢碘酸等还原
下列说法错误的是
| A.As2S3中砷元素的化合价为+3价 |
| B.“沉砷”过程中FeS可以用过量的Na2S代替 |
C.用氧气进行“氧化脱硫”涉及离子方程式AsS +2O2=AsO +2O2=AsO +3S↓ +3S↓ |
| D.能用氢碘酸、淀粉溶液检验还原后溶液中是否仍存在砷酸 |
您最近一年使用:0次
2022-04-27更新
|
248次组卷
|
3卷引用:湖南省永州市2022届高三高考第三次适应性考试化学试题
2021·全国·模拟预测
7 . 含铬废水会严重污染环境,一种烟气协同处理含铬废水(含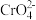 、
、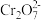 、泥沙等)的流程如图:
、泥沙等)的流程如图:

已知:① ②酸性条件下,
②酸性条件下,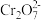 表现强氧化性
表现强氧化性
下列说法错误的是
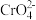 、
、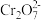 、泥沙等)的流程如图:
、泥沙等)的流程如图: 
已知:①
 ②酸性条件下,
②酸性条件下,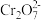 表现强氧化性
表现强氧化性下列说法错误的是
| A.“沉降”的主要目的是除去泥沙等不溶物 |
B.“调pH”时存在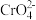 转化为 转化为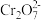 |
C. 溶液可用盐酸代替 溶液可用盐酸代替 |
D.母液经处理可获得 |
您最近一年使用:0次
名校
8 . 已知K2Cr2O7溶液中存在平衡: Cr2O72-(橙色)+H2O 2CrO42-(黄色)+2H+。保持温度不变,用K2Cr2O7溶液进行下列实验:
2CrO42-(黄色)+2H+。保持温度不变,用K2Cr2O7溶液进行下列实验:
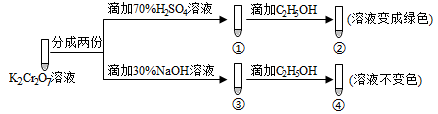
结合实验,下列说法正确的是
 2CrO42-(黄色)+2H+。保持温度不变,用K2Cr2O7溶液进行下列实验:
2CrO42-(黄色)+2H+。保持温度不变,用K2Cr2O7溶液进行下列实验:
结合实验,下列说法正确的是
| A.①中溶液变黄,③中溶液橙色加深 |
| B.上述可逆反应的平衡常数:①<③ |
| C.K2Cr2O7溶液的氧化性在酸性条件下更强 |
| D.若向④中加入70%H2S04溶液至过量,溶液变为橙色 |
您最近一年使用:0次
2017-03-31更新
|
560次组卷
|
4卷引用:2017届河南省郑州、平顶山、濮阳市高三第二次质量预测(二模)理综化学试卷
名校
9 . 下列事实不能用平衡移动原理解释的是
A.镁条在水中产生少量气泡后反应停止,在1mol/L 溶液中持续产生气泡 溶液中持续产生气泡 |
| B.二氧化锰与稀盐酸共热不产生氯气,与浓盐酸共热产生氯气 |
| C.在硫酸铜溶液中加入氯化钠固体,充分溶解后溶液变为蓝绿色 |
| D.在氯水中加入少量碳酸钙,可以增强氯水的氧化性 |
您最近一年使用:0次
解题方法
10 . 铬与铝性质相似,但活泼性比铝弱、熔点比铝高。下列说法错误的是
| A.可用铝热反应制备铬 |
| B.常温下铬在浓硝酸中发生钝化 |
C.可直接蒸发 溶液制备无水 溶液制备无水 |
D.已知碱性条件下,Cr(Ⅲ)可被氧化为Cr(Ⅵ),则其氧化产物为 |
您最近一年使用:0次



