1 . 下列事实中不能用勒夏特列原理来解释的是
| A.在合成氨工业中不断补充N2和H2并将生成的NH3及时地从混合气中分离出来 |
| B.合成氨的反应需要加入催化剂 |
| C.增大压强有利于合成氨的反应 |
| D.开启啤酒瓶后,瓶中马上泛起大量泡沫 |
您最近一年使用:0次
2 . 下列说法正确的是
A.在恒容恒温条件下,当 达到平衡后,再充入一定量的 达到平衡后,再充入一定量的 后达平衡, 后达平衡, 转化率将增大 转化率将增大 |
B.对于反应 达平衡后,缩小容器体积, 达平衡后,缩小容器体积, 的浓度增大 的浓度增大 |
| C.可逆反应达到平衡后,增大任何一种反应物的量,都可使平衡正向移动 |
D.在恒温条件下,当 反应平衡后,缩小体积,活化分子百分数增加 反应平衡后,缩小体积,活化分子百分数增加 |
您最近一年使用:0次
3 . 下列事实不能用勒夏特列原理解释的是
| A.使用新型催化剂可使氮气与氢气在常温常压下合成氨气 |
| B.用排饱和食盐水的方法收集氯气 |
C. 溶液中加入固体KSCN后颜色变深 溶液中加入固体KSCN后颜色变深 |
| D.石灰石与稀盐酸在密闭瓶中反应结束后,打开瓶塞,溶液中有气泡产生 |
您最近一年使用:0次
名校
4 . 已知 呈粉红色,
呈粉红色, 呈蓝色,
呈蓝色,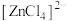 为无色。现将
为无色。现将 溶于水,加入浓盐酸后,溶液由粉红色变为蓝色,存在以下平衡:
溶于水,加入浓盐酸后,溶液由粉红色变为蓝色,存在以下平衡: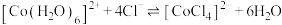 ,用该溶液做实验,溶液的颜色变化如下:
,用该溶液做实验,溶液的颜色变化如下:
 呈粉红色,
呈粉红色, 呈蓝色,
呈蓝色,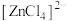 为无色。现将
为无色。现将 溶于水,加入浓盐酸后,溶液由粉红色变为蓝色,存在以下平衡:
溶于水,加入浓盐酸后,溶液由粉红色变为蓝色,存在以下平衡: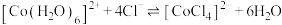 ,用该溶液做实验,溶液的颜色变化如下:
,用该溶液做实验,溶液的颜色变化如下:
A.等物质的量的 和 和 中 中 键数之比为 键数之比为 |
B.由实验1可推知 |
C.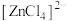 和 和 的配位数之比为 的配位数之比为 |
D.由实验③可知配离子的稳定性: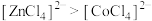 |
您最近一年使用:0次
名校
5 . 下述反应可制备特种陶瓷的原料MgO:MgSO4(s)+CO(g) MgO(s)+CO2(g)+SO2(g) △H>0,该反应在某密闭容器中达到平衡时,下列分析正确的是
MgO(s)+CO2(g)+SO2(g) △H>0,该反应在某密闭容器中达到平衡时,下列分析正确的是
 MgO(s)+CO2(g)+SO2(g) △H>0,该反应在某密闭容器中达到平衡时,下列分析正确的是
MgO(s)+CO2(g)+SO2(g) △H>0,该反应在某密闭容器中达到平衡时,下列分析正确的是| A.恒温时,增大压强平衡逆向移动,平衡常数减小 |
| B.容积不变时,升高温度,混合气体的平均相对分子质量减小 |
| C.恒温恒容时,分离出部分CO2气体可提高MgSO4的转化率 |
D.恒温恒容时,冲入CO气体,达到新平衡时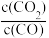 增大 增大 |
您最近一年使用:0次
名校
6 . 下列事实不能用勒夏特列原理解释的是
A.用饱和食盐水来除 中的 中的 | B.红棕色的 加压后颜色变深 加压后颜色变深 |
| C.开启啤酒瓶后,瓶中马上泛起大量泡沫 | D.增大压强,有利于 与 与 反应生成 反应生成 |
您最近一年使用:0次
2024-02-13更新
|
119次组卷
|
2卷引用:陕西省咸阳市实验中学2022-2023学年高三上学期第二次月考化学试题
名校
解题方法
7 . 某MOFs多孔材料孔径大小和形状恰好将N2O4“固定”,能高选择性吸附NO2。废气中的NO2被吸附后,经处理能全部转化为HNO3。原理示意图如下:
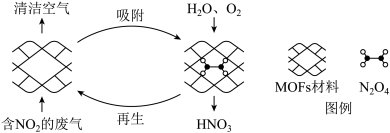
下列说法不正确的是

下列说法不正确的是
A.使用多孔材料不能改变 的焓变 的焓变 |
B.使用多孔材料能促进 平衡正向移动 平衡正向移动 |
C.加入 和 和 ,发生的反应方程式为 ,发生的反应方程式为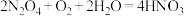 |
D.温度升高会提高 的平衡转化率 的平衡转化率 |
您最近一年使用:0次
名校
8 . 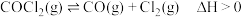 .当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加
.当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加 的浓度 ④减压 ⑤恒压通入惰性气体 ⑥加催化剂,能提高
的浓度 ④减压 ⑤恒压通入惰性气体 ⑥加催化剂,能提高 转化率的是
转化率的是
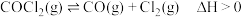 .当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加
.当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加 的浓度 ④减压 ⑤恒压通入惰性气体 ⑥加催化剂,能提高
的浓度 ④减压 ⑤恒压通入惰性气体 ⑥加催化剂,能提高 转化率的是
转化率的是| A.①②④ | B.③⑤⑥ | C.②③⑤ | D.①④⑤ |
您最近一年使用:0次
名校
解题方法
9 . 某化学小组通过测定溶液pH,计算K2Cr2O7溶液中“Cr2O (橙色)+H2O=2CrO
(橙色)+H2O=2CrO (黄色)+2H+”的平衡常数,结果如下:
(黄色)+2H+”的平衡常数,结果如下:
下列说法不合理的是
 (橙色)+H2O=2CrO
(橙色)+H2O=2CrO (黄色)+2H+”的平衡常数,结果如下:
(黄色)+2H+”的平衡常数,结果如下:| 实验序号 | 温度(°C) | K2Cr2O7溶液浓度(mol/L) | pH | 平衡常数 |
| ① | 26.3 | 0.1000 | a | 2.5×10-15 |
| ② | 26.3 | 0.3000 | 3.78 | b |
| ③ | 50.0 | 0.1000 | 3.75 | 1.01×10-14 |
| A.a大于3.78 |
| B.b等于2.5×10-15 |
| C.由实验①③结果可说明该反应为吸热反应 |
| D.向实验①2mL溶液中加入6滴6mol/LNaOH溶液,溶液橙色加深;恢复原温度,平衡常数不变 |
您最近一年使用:0次
名校
10 . 某同学研究浓度对化学平衡的影响,下列说法正确的是
已知: (aq) (橙色) +H2O(l)
(aq) (橙色) +H2O(l) 2
2 (aq) (黄色)+2H+(aq) △H=+13.8kJ/mol
(aq) (黄色)+2H+(aq) △H=+13.8kJ/mol
已知:
 (aq) (橙色) +H2O(l)
(aq) (橙色) +H2O(l) 2
2 (aq) (黄色)+2H+(aq) △H=+13.8kJ/mol
(aq) (黄色)+2H+(aq) △H=+13.8kJ/mol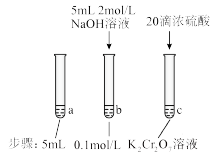 | 待试管b中颜色不变后与试管a比较,溶液颜色变浅。滴加浓硫酸,试管c温度略有升高,溶液颜色与试管a相比,变深。 |
| A.该反应为氧化还原反应 |
B.待试管b中溶液颜色不变的目的是使 完全反应 完全反应 |
| C.试管c中的现象说明影响平衡的主要因素是温度 |
| D.该实验不能证明减小生成物浓度平衡正向移动 |
您最近一年使用:0次



