某化学小组通过测定溶液pH,计算K2Cr2O7溶液中“Cr2O (橙色)+H2O=2CrO
(橙色)+H2O=2CrO (黄色)+2H+”的平衡常数,结果如下:
(黄色)+2H+”的平衡常数,结果如下:
下列说法不合理的是
 (橙色)+H2O=2CrO
(橙色)+H2O=2CrO (黄色)+2H+”的平衡常数,结果如下:
(黄色)+2H+”的平衡常数,结果如下:| 实验序号 | 温度(°C) | K2Cr2O7溶液浓度(mol/L) | pH | 平衡常数 |
| ① | 26.3 | 0.1000 | a | 2.5×10-15 |
| ② | 26.3 | 0.3000 | 3.78 | b |
| ③ | 50.0 | 0.1000 | 3.75 | 1.01×10-14 |
| A.a大于3.78 |
| B.b等于2.5×10-15 |
| C.由实验①③结果可说明该反应为吸热反应 |
| D.向实验①2mL溶液中加入6滴6mol/LNaOH溶液,溶液橙色加深;恢复原温度,平衡常数不变 |
更新时间:2024-01-03 21:52:44
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下面关于化学反应的限度的叙述中,正确的是
| A.化学反应的限度都相同 |
| B.可以通过改变温度控制化学反应的限度 |
| C.可以通过延长化学反应的时间改变化学反应的限度 |
| D.当一个化学反应在一定条件下达到限度时,反应即停止 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列叙述及解释正确的是
| A.2NO2(g)(红棕色)⇌N2O4(g)(无色)△H<0,在平衡后,对平衡体系采取缩小容积、增大压强的措施,因为平衡向正反应方向移动,故体系颜色变浅 |
| B.H2(g) + I2(g)⇌2HI(g) △H<0,在平衡后,对平衡体系采取增大容积、减小压强的措施,因为平衡不移动,故体系颜色不变 |
| C.对于N2+3H2⇌2NH3,平衡后,压强不变,充入Ar,平衡左移 |
| D.FeCl3+3KSCN⇌Fe(SCN)3(红色)+3KCl,在平衡后,加少量KCl,因为平衡向逆反应方向移动,故体系颜色变浅 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】在新制的氯水中存在平衡:Cl2+H2O HCl+HClO。加入少量下列物质能使c(HClO)增大的是
HCl+HClO。加入少量下列物质能使c(HClO)增大的是
 HCl+HClO。加入少量下列物质能使c(HClO)增大的是
HCl+HClO。加入少量下列物质能使c(HClO)增大的是| A.CaCO3 | B.NaOH | C.CaSO3 | D.HCl |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】对于任何一个平衡体系,采取下列措施一定会引起平衡移动的是
| A.使用催化剂 | B.增加体系的压强 | C.加入一种反应物 | D.升高温度 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列实验方案和相关操作正确的是( )
A.检验淀粉的水解程度:淀粉溶液中加少量稀硫酸,加热4-5分钟后取样于试管中,滴加新制 悬浊液并加热试管,检验淀粉是否发生水解 悬浊液并加热试管,检验淀粉是否发生水解 |
B.探究温度对化学平衡的影响:将少量 晶体溶于95%的乙醇溶液,逐滴加蒸馏水至溶液恰好呈粉红色,用酒精灯加热,观察颜色变化 晶体溶于95%的乙醇溶液,逐滴加蒸馏水至溶液恰好呈粉红色,用酒精灯加热,观察颜色变化 |
C.检验火柴头中是否含有氯元素:将未燃的火柴头浸泡在少量水中,片刻后取少量溶液于试管中,向其中滴加 溶液和稀硝酸,观察是否出现白色沉淀 溶液和稀硝酸,观察是否出现白色沉淀 |
D.反应速率的比较:将不同浓度的 与稀硫酸混合后,测定收集相同体积的气体所需时间,即可比较化学反应速率的快慢 与稀硫酸混合后,测定收集相同体积的气体所需时间,即可比较化学反应速率的快慢 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在体积为1 L的恒容密闭容器中充入一定量的H2S气体,平衡时三种组分的物质的量与温度的关系如图所示,下列说法错误的是
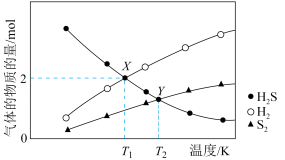

| A.X点和Y点的压强之比为10∶11 |
B.反应 在T1时的平衡常数小于T2时的平衡常数 在T1时的平衡常数小于T2时的平衡常数 |
| C.T2时,向Y点容器中再充入1.5 mol H2S和0.5 mol H2,重新平衡前v(正)>v(逆) |
| D.T1时,若起始时向容器中充入5 mol H2S气体,则平衡时H2S的转化率小于50% |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】升高温度,下列数据不一定增大的是
| A.化学反应速率v | B.水的离子积常数KW |
| C.化学平衡常数K | D.醋酸钠的水解平衡常数Kb |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】温度和压强对反应X+Y 2Z的影响如图所示。图中横坐标表示温度,纵坐标表示平衡时混合气体中Z的体积分数。下列叙述正确的是
2Z的影响如图所示。图中横坐标表示温度,纵坐标表示平衡时混合气体中Z的体积分数。下列叙述正确的是

 2Z的影响如图所示。图中横坐标表示温度,纵坐标表示平衡时混合气体中Z的体积分数。下列叙述正确的是
2Z的影响如图所示。图中横坐标表示温度,纵坐标表示平衡时混合气体中Z的体积分数。下列叙述正确的是
| A.相同温度下,10kPa、100kPa、1000kPa压强时对应该反应的平衡常数不同 |
| B.X、Y、Z均为气态 |
| C.X和Y中最多只有一种为气态,Z为气态 |
| D.上述反应的逆反应的ΔH>0 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】在一定温度下,下列反应的化学平衡常数数值如下:
①2NO(g) N2(g)+O2(g) K1=1×1030
N2(g)+O2(g) K1=1×1030
②2H2(g)+O2(g) 2H2O(g) K2=2×1081
2H2O(g) K2=2×1081
③2CO2(g) 2CO(g)+O2(g) K3=4×10-92
2CO(g)+O2(g) K3=4×10-92
以下说法正确的是
①2NO(g)
 N2(g)+O2(g) K1=1×1030
N2(g)+O2(g) K1=1×1030②2H2(g)+O2(g)
 2H2O(g) K2=2×1081
2H2O(g) K2=2×1081③2CO2(g)
 2CO(g)+O2(g) K3=4×10-92
2CO(g)+O2(g) K3=4×10-92以下说法正确的是
| A.该温度下,反应①的平衡常数表达式为K1=c(N2)·c(O2) |
B.该温度下,反应2H2O(g) 2H2(g)+O2(g)的平衡常数的数值为 5×10-82 2H2(g)+O2(g)的平衡常数的数值为 5×10-82 |
| C.该温度下,反应①、反应②的逆反应、反应③产生O2的倾向由大到小的顺序为NO>CO2>H2O |
| D.增大压强,反应①、反应②、反应③的化学平衡常数分别为:不变、变大、变小 |
您最近一年使用:0次

 N2O4(g)平衡体系加压后颜色加深
N2O4(g)平衡体系加压后颜色加深
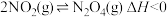 。在测定
。在测定 的相对分子质量时,下列条件中,测定结果误差最小的是
的相对分子质量时,下列条件中,测定结果误差最小的是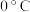 、压强
、压强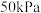
 、压强
、压强
 、压强
、压强