1 . 利用合成气(主要成分为CO、CO2、 H2) 一定条件下合成甲醇(CH3OH),发生的主要反应如下:
Ⅰ. CO(g) + 2H2(g)=CH3OH(g) △H。
Ⅱ. CO(g) + H2O(g)=CO2(g) +H2(g) ∆H2=-41.2 kJ/mol
回答下列问题:
(1)已知反应①中的相关化学键键能数据如下:
写出由二氧化碳、氢气制备甲醇的热化学方程式_______ 反应I在_______ (填“高温”、“低温”或“任意温度”)条件下自发进行。
(2)在T℃时,向5L恒容密闭容器中加入0.6 mol CO和0.45 molH2,发生反应Ⅰ。CO和CH3OH的浓度在不同时刻的变化状况如图所示:
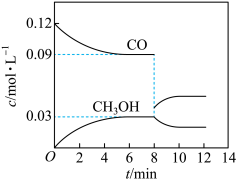
①下列能够说明反应在第6min时达到平衡状态的是______
A.混合气体的平均摩尔质量不再改变
B. CH3OH 的浓度不变
C. v(CO)正 : v(H2)逆= 2:1
D. P(CO):P( H2)= 1:2
第8 min时改变的条件是_______
②在第12 min时升高温度,重新达到平衡时,化学平衡常数将_______ (填 “增大”“不变”或“减小”),理由是_______
(3)某科研小组研究了反应CO(g) + 2H2(g)= CH3OH(g)的动力学,获得其速率方程v=k[c(H2)]1/2[c(CO)]m,k为速率常数(只受温度影响),m为CO的反应级数。在某温度下进行实验,测得各组分初浓度和反应初速率如下:
CO的反应级数m=_______ , 当实验2进行到某时刻,测得c(H3)= 0.010 mol·L-1,则此时的反应速率v_______ mol·L-1·s-1(已知: ≈0.3)。
≈0.3)。
(4)利用CH4重整CO2的催化转化如图所示,CH4与CO2重整反应的方程式为_______ 。有关转化过程,下列说法正确的是_______ (填序号)。
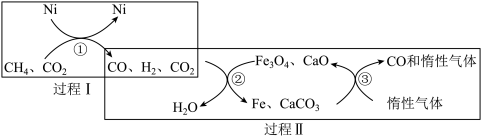
a. 过程Ⅰ中CO2未参与反应
b.过程Ⅱ实现了含碳物质与含氢物质的分离
c.转化②中CaO消耗过程中的CO2,有利于反应正向进行
d. 转化③中Fe与CaCO3,反应的物质的量之比为4:3
Ⅰ. CO(g) + 2H2(g)=CH3OH(g) △H。
Ⅱ. CO(g) + H2O(g)=CO2(g) +H2(g) ∆H2=-41.2 kJ/mol
回答下列问题:
(1)已知反应①中的相关化学键键能数据如下:
| 化学键 | H-H | C-O | C≡O | H-O | C-H |
| E/(kJ/mol) | 436 | 343 | 1076 | 465 | 413 |
(2)在T℃时,向5L恒容密闭容器中加入0.6 mol CO和0.45 molH2,发生反应Ⅰ。CO和CH3OH的浓度在不同时刻的变化状况如图所示:

①下列能够说明反应在第6min时达到平衡状态的是
A.混合气体的平均摩尔质量不再改变
B. CH3OH 的浓度不变
C. v(CO)正 : v(H2)逆= 2:1
D. P(CO):P( H2)= 1:2
第8 min时改变的条件是
②在第12 min时升高温度,重新达到平衡时,化学平衡常数将
(3)某科研小组研究了反应CO(g) + 2H2(g)= CH3OH(g)的动力学,获得其速率方程v=k[c(H2)]1/2[c(CO)]m,k为速率常数(只受温度影响),m为CO的反应级数。在某温度下进行实验,测得各组分初浓度和反应初速率如下:
| 实验序号 | c(H2)/mol/L | c(CO)/mol/L | v/mol/L |
| 1 | 0.100 | 0.100 | 1.2×10-2 |
| 2 | 0.050 | 0.100 | 8.4×10-3 |
| 3 | 0.100 | 0.200 | 2.4×10-2 |
 ≈0.3)。
≈0.3)。(4)利用CH4重整CO2的催化转化如图所示,CH4与CO2重整反应的方程式为

a. 过程Ⅰ中CO2未参与反应
b.过程Ⅱ实现了含碳物质与含氢物质的分离
c.转化②中CaO消耗过程中的CO2,有利于反应正向进行
d. 转化③中Fe与CaCO3,反应的物质的量之比为4:3
您最近一年使用:0次
名校
2 . 一定条件下,通过下列反应可以制备特种陶瓷的原料 MgO, MgSO4(s) + CO(g) ⇌ MgO(s) + CO2(g) + SO2(g) ΔH > 0。该反应在恒容的密闭容器中达到平衡后(A 点),若仅改变图中横坐标 x 的值, 重新达到平衡后,纵坐标 y 随 x 变化趋势合理的是( )(忽略固体物质所占有的体积)
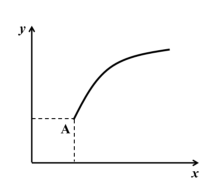

| A.x 为温度,y 为容器内混合气体的密度 |
| B.x 为 MgSO4的质量,y 为 CO 的平衡转化率 |
| C.x 为 CO2的物质的量,y 为 CO 的平衡转化率 |
| D.x 为 SO2的浓度,y 为 CO2的平衡浓度 |
您最近一年使用:0次
2020-10-28更新
|
347次组卷
|
4卷引用:四川省巴中市巴中中学、南江中学2021-2022学年高二上学期半期联考化学试题



