名校
1 . 痛风病与关节滑液中形成的尿酸钠(NaUr)有关(NaUr增多,病情加重),其化学原理为:
 。下列说法
。下列说法
| A.饮食中摄入过多食盐,会加重痛风病病情 | B.大量饮水会增大痛风病发作的可能性 |
| C.寒冷季节更易诱发关节疼痛 | D.患痛风病的人应少吃能代谢产生更多尿酸的食物 |
您最近一年使用:0次
2024-02-21更新
|
161次组卷
|
41卷引用:辽宁省葫芦岛市2020-2021学年高二上学期期末考试化学试题
辽宁省葫芦岛市2020-2021学年高二上学期期末考试化学试题北京市房山区2020-2021学年高二上学期期末考试化学试题河南省焦作市县级重点中学2021-2022学年高二上学期期中考试化学试题吉林省长白山第二高级中学校2021-2022学年高三上学期第二次月考化学试题北京市第四十四中学2021-2022学年高二上学期期中考试化学试题北京市顺义区杨镇第一中学2021-2022学年高二上学期期中考试化学试题 北京市西城区2019-2020学年度高二上学期期末考试化学试题上海市奉贤区2020届高三5月教学质量调研(二模)化学试题湖北省黄冈市麻城市实验高中2020-2021学年高二上学期10月月考化学试题江西省赣州市南康中学2020-2021学年高二上学期第二次大考化学试题内蒙古阿荣旗第一中学2020-2021学年高二上学期期中考试化学试题山西省朔州市怀仁县大地学校2020-2021学年高二上学期第三次月考化学试题北京市第四十三中学2020-2021学年高二上学期12月月考化学试题北京市房山区2022-2023学年高二上学期期中质量检测化学试题北京市第七中学2022-2023学年高二上学期期中化学试题北京市顺义区杨镇第一中学2022-2023学年高二上学期期中检测化学试题广东省信宜市第二中学2022-2023学年高二上学期11月月考化学试题广东省珠海市实验中学2022-2023学年高二上学期第一次段考化学试题北京市顺义区2023届高三第一次统练化学试题广东省汕头市聿怀中学2022-2023学年高二上学期期末线上考试化学试题安徽省宣城市2022-2023学年高二上学期期末调研考试化学试题广东省河源市龙川县第一中学2022-2023学年高二上学期期末考试化学试题(已下线)专题15 化学反应速率和化学平衡新疆乌鲁木齐市第四中学2022-2023学年高二下学期期中阶段诊断测试化学试题(已下线)第05讲 影响化学平衡的因素-【暑假自学课】2023年新高二化学暑假精品课(人教版2019选择性必修1)云南省玉溪师范学院附属中学2022-2023学年高二下学期期末考试化学试题北京市顺义牛栏山第一中学2023-2024学年高二上学期期中考试化学试题黑龙江省齐齐哈尔市恒昌中学校2022-2023学年高二上学期11月期中检测化学试题北京市清华大学附属中学2023-2024学年高二上学期期中考试化学试题北京市第六十六中学2023-2024学年高二上学期期中质量检测化学试题黑龙江省哈尔滨市第三十二中学校2023-2024学年高二上学期11月期中考试化学试题北京市大兴区兴华中学2023-2024学年高二上学期期中考试化学试题北京师范大学附属中学2023-2024学年高二上学期期中考试化学试卷北京市第一六六中学2022-2023学年高二上学期期中考试化学试卷北京师范大学第二附属中学2023-2024学年高二上学期期中考试化学试题浙江省宁波三锋教研联盟2023-2024学年高二上学期期中联考化学试题河南省信阳市淮滨县2022-2023学年高二上学期11月期中考试化学试题甘肃省平凉市第二中学2022-2023学年高二上学期期末考试(延考)化学试题四川省内江市2025届第三中学高二上学期化学试卷北京市北京师范大学附属中学平谷第一分校2023-2024学年高二上学期期中考试化学试题北京市顺义区2022-2023学年高三上学期第一次统练化学试卷
名校
2 . 900 ℃时,向2.0 L恒容密闭容器中充入0.40 mol乙苯,压强为2Mpa,发生反应: 。一段时间后,反应达到平衡,反应过程中测定的部分数据如下表所示:
。一段时间后,反应达到平衡,反应过程中测定的部分数据如下表所示:
下列说法正确的是
 。一段时间后,反应达到平衡,反应过程中测定的部分数据如下表所示:
。一段时间后,反应达到平衡,反应过程中测定的部分数据如下表所示:| 时间/min | 0 | 10 | 20 | 30 | 40 |
| n(乙苯)/mol | 0.40 | 0.30 | 0.24 | n2 | n3 |
| n(苯乙烯)/mol | 0.00 | 0.10 | n1 | 0.20 | 0.20 |
| A.保持其他条件不变,向容器中充入不参与反应的水蒸气作为稀释剂,则乙苯的转化率大于50.0% |
| B.反应在20 min时反应速率v(H2)=0.004 mol·L-1·min-1 |
| C.9000C该反应的平衡常数Kp=2/3MPa |
| D.相同温度下,起始时向容器中充入0.10 mol乙苯、0.10 mol苯乙烯和0.30 mol H2,则达到平衡前:v正<v逆 |
您最近一年使用:0次
10-11高二下·浙江杭州·期中
3 . 对已经达到化学平衡的反应: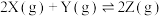 ,减小压强时,对反应产生的影响是
,减小压强时,对反应产生的影响是
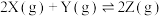 ,减小压强时,对反应产生的影响是
,减小压强时,对反应产生的影响是| A.逆反应速率增大,正反应速率减小,平衡向逆反应方向移动 |
| B.逆反应速率减小,正反应速率增大,平衡向正反应方向移动 |
| C.正、逆反应速率都减小,平衡向逆反应方向移动 |
| D.正、逆反应速率都增大,平衡向正反应方向移动 |
您最近一年使用:0次
2022-11-02更新
|
741次组卷
|
97卷引用:辽宁省恒仁满族自治县第二高级中学2021-2022学年高二上学期期中考试化学试题
辽宁省恒仁满族自治县第二高级中学2021-2022学年高二上学期期中考试化学试题辽宁省辽源市金鼎高级中学2016-2017学年高二上学期期末考试化学试卷辽宁省大连渤海高级中学2018-2019学年高二下学期期中考试化学试题黑龙江漠河市高级中学2020-2021学年高二上学期期末考试化学试题湖北省十堰市2020-2021学年高二上学期期末考试化学试题广东省惠州市2020-2021学年高二上学期期末考试化学试题广东省惠州市2020-2021学年高二上学期期末质量监测化学试题河南省开封市五县2020-2021学年高二上学期期末考试化学试题选择性必修1(SJ)专题2第三单元 化学平衡的移动山东省山大附中卧龙学校2021-2022学年高二上学期第一次月考化学试题甘肃省庆阳市第六中学2021-2022学年高二上学期期中考试化学(理)试题四川省广安代市中学校2021-2022学年高二上学期第一次月考化学试题广东省揭阳市惠来县第一中学2021-2022学年高二上学期第二次阶段考试化学试题新疆乌鲁木齐市第三十一中学2021-2022学年高二上学期期中考试化学试题内蒙古乌兰察布市部分学校2021-2022学年高二上学期期中联考化学试题甘肃省临夏州临夏县中学2021-2022学年高二上学期期中考试化学(B卷)试题福建省南安市柳城中学2021-2022学年高二上学期期中考试化学试题(已下线)2010—2011学年浙江省杭州学军中学高二下学期期中考试化学试卷(已下线)2010—2011学年内蒙古赤峰二中高一下学期期末考试化学试卷(已下线)2011-2012学年山东省鲁北中学高二上学期期中考试化学试卷(已下线)2011-2012学年山东省济宁市邹城二中高二上学期期中质量检测化学试卷(已下线)2011-2012学年云南省玉溪一中高二下学期期中考试化学试卷(已下线)2012-2013学年浙江省宁海县正学中学高二下学期第一次阶段性测试化学试卷(已下线)2012-2013学年昆明三中、滇池中学(滇中)高二下期中考试化学卷(已下线)2012-2013学年江苏省南京三中高二下学期期中考试化学试卷(已下线)2012-2013学年黑龙江省鹤岗一中高一下学期期末考试化学试卷(已下线)2013-2014学年河南省漯河市高二上学期期中考试化学试卷(已下线)2014-2015学年河南周口市沈丘县县直高级中学高二上第一次月考化学(已下线)2014-2015学年山东安丘市实验中学期中考试高二化学模拟(B)卷(已下线)2014秋安徽省淮北师范大学附属实验中学高二上学期期中化学试卷2015-2016学年陕西省西安第七十中学高二上学期期中测试化学试卷2015-2016学年宁夏育才中学高二上学期期中测试化学试卷2015-2016学年青海西宁第十四中学高二上期中考试化学卷2015-2016学年陕西省澄城县寺前中学高一下学期期中考试化学试卷(已下线)同步君 人教版 选修4 第2章 第3节 化学平衡状态2016-2017学年湖北省襄阳五中高二上开学考试化学试卷2016-2017学年河北省博野中学高二上学期第二次月考化学试卷2016-2017学年宁夏育才中学高二上第一次月考化学卷2016-2017学年贵州省贵阳六中高二上10月月考化学卷2016-2017学年河北省张家口万全中学高二上第一次月考化学试卷2016-2017学年湖南省浏阳市第一中学高二上阶段性测试化学试卷2016-2017学年甘肃省民乐一中高二上10月月考化学试卷2016-2017学年山东省桓台二中高二12月检测化学试卷甘肃省会宁县第四中学2017-2018学年高二上学期期中考试化学试题云南省德宏州芒市第一中学2017-2018学年高二上学期期中考试化学试题山东省济南第一中学2017-2018学年高二上学期期中考试化学试题高中化学人教版 选修四 第二章 化学反应速率和化学平衡 第三节 化学平衡 化学平衡第二课时(化学平衡状态)【全国省级联考】广东省蓝精灵中学2017-2018 学年度高二上学期期末联考化学试题【全国百强校】河北省石家庄市辛集中学2018-2019学年高二上学期第一次月考化学试题甘肃省岷县一中2018-2019学年高二上学期第一次月考化学试题【全国百强校】黑龙江省哈尔滨市第六中学2018-2019学年高二上学期期中考试化学试题【全国百强校】贵州省铜仁市第一中学2018-2019学年高二上学期期中考试化学试题甘肃省高台县第一中学2018-2019学年高二上学期期中考试化学试题黑龙江省伊春市第二中学2018-2019学年高二(理)上学期期中考试化学试题甘肃省宁县二中2018-2019学年高二上学期期中考试化学试题四川省宜宾市第四中学2018-2019学年高二上学期期中考试理科综合化学试题高二人教版选修4 第二章 第三节 化学平衡河北省承德市第一中学2018-2019学年高二上学期第三次月考化学试题甘肃省镇原县孟坝中学2018-2019学年高二上学期期中考试化学试题新疆维吾尔自治区沙雅县第二中学2018-2019学年高二上学期期中考试化学试题河南省永城市实验高级中学2018-2019学年高二上学期期中考试化学试题上海市华东师范大学附属天山学校2018-2019学年高一第二学期期中考试化学试题黑龙江省哈尔滨市第六中学2019-2020学年高二10月月考化学试题湖南省永州市东安县第一中学2019-2020学年高二上学期第一次月考化学试题河北省鹿泉第一中学2019-2020学年高二9月月考化学试题甘肃省张掖市山丹县第一中学2019-2020学年上学期9月月考--高二化学江西省宜春九中(外国语学校)2019-2020学年高二上学期期中考试化学试题吉林省蛟河市朝鲜族中学校2019-2020学年高二上学期期中考试化学试题河北省石家庄市普通高中2019-2020学年高二10月月考化学(高考)试题新疆沙雅县第二中学2019-2020学年高二上学期期中考试化学试题贵州省毕节市实验高级中学2018-2019学年高二上学期期末考试化学试题湖南省邵阳市洞口县第四中学2019-2020学年高二上学期期中考试化学试题黑龙江省哈尔滨市第三十二中学2019-2020学年高二上学期期末考试化学试题云南省楚雄市楚雄实验中学2018—2019学年高二上学期9月月考化学试题黑龙江桦南二中2019-2020学年高二上学期期中考试化学试题广西桂林市第十八中学2019-2020学年高二下学期期中考试化学试题河北省石家庄市第二中学2019-2020学年高一下学期期末考试化学试题陕西省延安市吴起高级中学2019-2020学年高一下学期第四次质量检测(期末)化学试题黑龙江省海林市朝鲜族中学2020-2021学年高二上学期第一次月考化学试题海南省海口市第四中学2020-2021学年高二上学期第一次月考化学试题吉林省通化县综合高级中学2020-2021学年高二上学期期中考试化学试题新疆生产建设兵团第四师第一中学2020-2021学年高二上学期期中考试化学试题人教版(2019)高二化学选择性必修1第二章 化学反应速率与化学平衡 第二节 化学平衡 课时3 影响化学平衡的因素河北省唐山市河北唐山外国语学校2020-2021学年高二上学期期中考试(理科)化学试题宁夏长庆高级中学2020-2021学年高二上学期期中考试化学试题河北省张家口宣化一中2020-2021学年高二上学期12月月考化学试题福建省莆田第十五中学2018-2019学年高二上学期期末考试化学试题华中师范大学海南附属中学2019-2020学年高二上学期第三次月考化学试题吉林长春市榆树高级中学2019-2020学年高二下学期期末考试化学试题湖南省长沙宁乡市第十高级中学2020-2021学年高二上学期10月月考化学试题青海省西宁市大通回族土族自治县2021-2022学年高二上学期期末考试化学试题(已下线)第10讲 影响化学平衡的因素(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)湖北省随州市洛平许济四市联盟2022-2023学年高三上学期第一次质量检测化学试题湖北省黄州中学2022--2023学年高二上学期10月月考化学试题河南省灵宝市第五高级中学2021-2022学年高二下学期第一次月考化学试题广东省阳江市高新区2022-2023学年高二上学期1月期末考试化学试题作业(十二) 压强对化学平衡的影响 勒·夏特列原理
名校
4 . 下列事实能用勒夏特列原理来解释的是
A.实验室采用排饱和食盐水的方法收集氯气Cl2+H2O H++Cl-+HClO H++Cl-+HClO |
B.工业上合成氨反应N2(g)+3H2(g) 2NH3(g) △H<0选择500℃ 2NH3(g) △H<0选择500℃ |
C.H2、I2、HI平衡混合气体加压后颜色加深H2(g)+I2(g) 2HI(g) 2HI(g) |
D.SO2氧化成SO3,往往需要使用催化剂2SO2(g)+O2(g) 2SO3(g) 2SO3(g) |
您最近一年使用:0次
2022-08-25更新
|
418次组卷
|
10卷引用:辽宁省辽河油田第二高级中学2021-2022学年高二上学期开学考试化学试题
辽宁省辽河油田第二高级中学2021-2022学年高二上学期开学考试化学试题吉林省洮南市第一中学2021-2022学年高二上学期第一次月考化学试题吉林省长春市第二十中学2021-2022学年高二上学期第一次质量检测化学试题新疆昌吉州2021-2022学年高二上学期期中质量检测化学试题江西省宜春市万载中学2021-2022学年高二上学期第二次月考化学试题重庆市九校联盟2017-2018学年高二上学期期中考试化学试题【区级联考】天津市武清区2018-2019学年高二上学期期中质量调查化学试题湖南省永州市双牌县第二中学2019-2020学年高二上学期期中考试化学试题(选考)上海市奉贤中学2022-2023学年高二上学期10月阶段测试化学试题重庆市渝东六校共同体2022-2023学年高二上学期联合诊断考试化学试题
名校
5 . 高温下,某反应达平衡,平衡常数K= ,恒容时,温度升高,B的浓度减小,下列说法正确的是
,恒容时,温度升高,B的浓度减小,下列说法正确的是
①该反应的焓变为正值
②恒温恒容下,增大压强B浓度一定增大
③升高温度,平衡常数K值减小
④该反应化学方程式为C(g)+D(g) A(g)+B(g)
A(g)+B(g)
⑤增加A的量,A的转化率减小
⑥加入催化剂,平衡不移动,V(正)、V(逆)都不变
 ,恒容时,温度升高,B的浓度减小,下列说法正确的是
,恒容时,温度升高,B的浓度减小,下列说法正确的是①该反应的焓变为正值
②恒温恒容下,增大压强B浓度一定增大
③升高温度,平衡常数K值减小
④该反应化学方程式为C(g)+D(g)
 A(g)+B(g)
A(g)+B(g)⑤增加A的量,A的转化率减小
⑥加入催化剂,平衡不移动,V(正)、V(逆)都不变
| A.①③⑥ | B.①⑤ | C.①④⑤ | D.①②⑤ |
您最近一年使用:0次
6 . 碳酸锶(SrCO3)难溶于水,主要用于电磁材料和金属冶炼。一种由工业碳酸锶(含少量Ba2+、Ca2+、Mg2+、 Pb2+等)制备高纯碳酸锶的工艺流程如下:
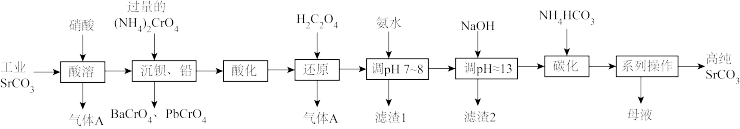
已知:I. Cr(OH)3为两性氢氧化物;
II.常温下,各物质的溶度积常数如下表所示。
回答下列问题:
(1)气体A的电子式为_______ 。
(2)“除钡、铅”时,pH过低会导致(NH4)2CrO4的利用率降低,原因为_______ (用离子方程式解释);“还原”时发生反应的离子方程式为_______ 。
(3)“滤渣1”的主要成分为_______ (填化学式)。
(4)用氨水和NaOH分步调节pH,而不是直接调节溶液的pH≈13的原因为_______ 。
(5)“调pH ≈13”后需对溶液进行煮沸并趁热过滤出滤渣2,煮沸并趁热过滤的原因为_______ 。
(6)已知:碳酸的电离常数Ka1=4.4×10-7、Ka2=4.7×10-11,则“碳化”时,反应Sr2+(aq)+2HCO (aq)
(aq) SrCO3(s)+H2CO3(aq)的平衡常数K=
SrCO3(s)+H2CO3(aq)的平衡常数K=_______ (保留两位有效数字)。
(7)“系列操作”中包含“200°C烘干”操作,烘干过程中除蒸发水分外,还能够除去SrCO3中的微量可溶性杂质,该杂质除NH4HCO3外还可能为_______ (填化学式)。

已知:I. Cr(OH)3为两性氢氧化物;
II.常温下,各物质的溶度积常数如下表所示。
| 化合物 | Cr(OH)3 | Ca(OH)2 | Mg(OH)2 | SrCO3 |
| Ksp近似值 | 1×10-31 | 5.5×10-6 | 1.8×10-11 | 5.6×10-10 |
(1)气体A的电子式为
(2)“除钡、铅”时,pH过低会导致(NH4)2CrO4的利用率降低,原因为
(3)“滤渣1”的主要成分为
(4)用氨水和NaOH分步调节pH,而不是直接调节溶液的pH≈13的原因为
(5)“调pH ≈13”后需对溶液进行煮沸并趁热过滤出滤渣2,煮沸并趁热过滤的原因为
(6)已知:碳酸的电离常数Ka1=4.4×10-7、Ka2=4.7×10-11,则“碳化”时,反应Sr2+(aq)+2HCO
 (aq)
(aq) SrCO3(s)+H2CO3(aq)的平衡常数K=
SrCO3(s)+H2CO3(aq)的平衡常数K=(7)“系列操作”中包含“200°C烘干”操作,烘干过程中除蒸发水分外,还能够除去SrCO3中的微量可溶性杂质,该杂质除NH4HCO3外还可能为
您最近一年使用:0次
2022-04-09更新
|
1198次组卷
|
13卷引用:辽宁省抚顺市第二中学2021-2022学年高三上学期10月月考化学试题
辽宁省抚顺市第二中学2021-2022学年高三上学期10月月考化学试题湖北省宜昌英杰学校2021-2022学年高三上学期9月月考化学试题河北省石家庄市2022届高三毕业班教学质量检测二(一模)化学试题(已下线)秘籍17 工艺流程的条件控制与计算-备战2022年高考化学抢分秘籍(全国通用)(已下线)专项15 工艺流程综合题-备战2022年高考化学阶段性新题精选专项特训(全国卷)(4月期)(已下线)化学-2022年高考押题预测卷01(山东卷)(已下线)化学-2022年高考考前押题密卷(湖南卷)(已下线)化学-2022年高考考前押题密卷(重庆卷)湖北省宜昌市夷陵中学2022届高三5月第二次限时训练(四模)化学试题山东省鄄城县第一中学2022-2023学年高二上学期期末考试化学试题湖南省株洲市九方中学2022-2023学年高三上学期第一次月考化学试题(已下线)河北省石家庄市2022届高三毕业班教学质量检测二(一模)(工业流程题)湖南省邵阳市第一中学2023届高三第五次月考化学试题
7 . 由γ一羟基丁酸(HOCH2CH2CH2COOH)生成γ-丁内酯( )的反应如下:HOCH2CH2CH2COOH
)的反应如下:HOCH2CH2CH2COOH 
 +H2O。在25°C时,溶液中γ一羟基丁酸初始浓度为0.180mol/L,随着反应的进行,测得γ一丁内酯的浓度随时间的变化如下表所示。下列说法中错误的是
+H2O。在25°C时,溶液中γ一羟基丁酸初始浓度为0.180mol/L,随着反应的进行,测得γ一丁内酯的浓度随时间的变化如下表所示。下列说法中错误的是
 )的反应如下:HOCH2CH2CH2COOH
)的反应如下:HOCH2CH2CH2COOH 
 +H2O。在25°C时,溶液中γ一羟基丁酸初始浓度为0.180mol/L,随着反应的进行,测得γ一丁内酯的浓度随时间的变化如下表所示。下列说法中错误的是
+H2O。在25°C时,溶液中γ一羟基丁酸初始浓度为0.180mol/L,随着反应的进行,测得γ一丁内酯的浓度随时间的变化如下表所示。下列说法中错误的是| t/min | 21 | 50 | 80 | 100 | 120 | 160 | 220 | ∞ |
| c/(mol/L) | 0.024 | 0.050 | 0.071 | 0.081 | 0.090 | 0.104 | 0.116 | 0.132 |
| A.在120min时,γ一羟基丁酸的转化率为50% |
| B.在50~80min内,以γ一丁内酯的浓度变化表示的反应速率为0.07mol/(L·min) |
| C.在25°C时,该反应的平衡常数为K=2.75 |
| D.为提高平衡时γ一羟基丁酸的转化率,可采取的措施是移出γ一丁内酯 |
您最近一年使用:0次
8 . “绿水青山就是金山银山”。运用化学反应原理研究氮的化合物的反应对缓解能源危机、治理环境污染具有重要意义。
(1)基态氮原子有___________ 种能量不同的电子
(2)肼是一种高能燃料。已知各共价键键能如表:
N2H4(g)+O2(g)⇌N2(g)+2H2O(l) ∆H=___________ kJ/mol,(注:肼的结构式为: 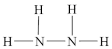 )
)
(3)目前,科学家正在研究一种以乙烯作为还原剂的脱硝(NO)原理,其脱硝机理如图1,脱硝率与温度、负载率(分子筛中催化剂的质量分数)的关系如图2所示。
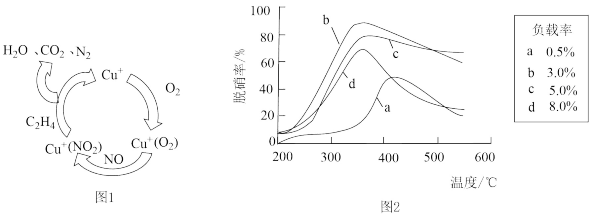
①若图1反应中NO与O2物质的量之比为2:1,则该脱硝原理总反应的化学方程式为:___________ 。
②为达到最佳的脱硝效果(分析图2),应采取的条件为___________ (填温度和负载率数值)。
(4)CaSO3与Na2SO4混合浆液可用于脱除NO2,反应过程为:
Ⅰ.CaSO3(s)+SO (aq)⇌CaSO4(s)+SO
(aq)⇌CaSO4(s)+SO (aq)
(aq)
Ⅱ.SO (aq)+2NO2(g)+H2O(l)⇌SO
(aq)+2NO2(g)+H2O(l)⇌SO (aq)+2NO
(aq)+2NO (aq)+2H+(aq)
(aq)+2H+(aq)
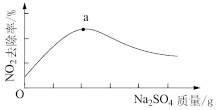
浆液中CaSO3质量一定时,Na2SO4的质量与NO2的去除率变化趋势如图所示。a点后NO2去除率降低的原因是___________ 。
(5)检测烟道气中NOx含量的步骤如下:
Ⅰ.将VL气样通入适量酸化的H2O2溶液中,使 完全被氧化为NO
完全被氧化为NO
Ⅱ.加水稀释至100.00mL,量取20.00mL该溶液,与V1mL c1 mol·L-1 FeSO4标准溶液(过量)充分混合;
Ⅲ.用c2mol·L-1 KMnO4标准溶液滴定剩余的 Fe2+,终点时消耗V2mL。
①某同学设计的如图滴定方式中,最合理的是___________ (夹持部分略去,填字母序号)
a.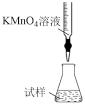 b.
b.  c.
c. 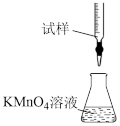
②滴定过程中有下列反应:3Fe2++NO +4H+=NO↑+3Fe3++2H2O, MnO
+4H+=NO↑+3Fe3++2H2O, MnO +5Fe2++8H+=Mn2++5Fe3++4H2O,判断下列情况对
+5Fe2++8H+=Mn2++5Fe3++4H2O,判断下列情况对 含量测定结果的影响(填“偏高”、“偏低”或“无影响”)
含量测定结果的影响(填“偏高”、“偏低”或“无影响”)
a.锥形瓶用蒸馏水洗净后没有干燥___________ 。
b.读取KMnO4标准溶液体积时,开始仰视读数,滴定结束时俯视读数___________ 。
(1)基态氮原子有
(2)肼是一种高能燃料。已知各共价键键能如表:
| N≡N | O=O | N−N | N−H | O−H | |
| 键能(kJ/mol) | 946 | 497 | 193 | 391 | 463 |
N2H4(g)+O2(g)⇌N2(g)+2H2O(l) ∆H=
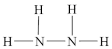 )
)(3)目前,科学家正在研究一种以乙烯作为还原剂的脱硝(NO)原理,其脱硝机理如图1,脱硝率与温度、负载率(分子筛中催化剂的质量分数)的关系如图2所示。

①若图1反应中NO与O2物质的量之比为2:1,则该脱硝原理总反应的化学方程式为:
②为达到最佳的脱硝效果(分析图2),应采取的条件为
(4)CaSO3与Na2SO4混合浆液可用于脱除NO2,反应过程为:
Ⅰ.CaSO3(s)+SO
 (aq)⇌CaSO4(s)+SO
(aq)⇌CaSO4(s)+SO (aq)
(aq)Ⅱ.SO
 (aq)+2NO2(g)+H2O(l)⇌SO
(aq)+2NO2(g)+H2O(l)⇌SO (aq)+2NO
(aq)+2NO (aq)+2H+(aq)
(aq)+2H+(aq)浆液中CaSO3质量一定时,Na2SO4的质量与NO2的去除率变化趋势如图所示。a点后NO2去除率降低的原因是

(5)检测烟道气中NOx含量的步骤如下:
Ⅰ.将VL气样通入适量酸化的H2O2溶液中,使
 完全被氧化为NO
完全被氧化为NO
Ⅱ.加水稀释至100.00mL,量取20.00mL该溶液,与V1mL c1 mol·L-1 FeSO4标准溶液(过量)充分混合;
Ⅲ.用c2mol·L-1 KMnO4标准溶液滴定剩余的 Fe2+,终点时消耗V2mL。
①某同学设计的如图滴定方式中,最合理的是
a.
 b.
b.  c.
c. 
②滴定过程中有下列反应:3Fe2++NO
 +4H+=NO↑+3Fe3++2H2O, MnO
+4H+=NO↑+3Fe3++2H2O, MnO +5Fe2++8H+=Mn2++5Fe3++4H2O,判断下列情况对
+5Fe2++8H+=Mn2++5Fe3++4H2O,判断下列情况对 含量测定结果的影响(填“偏高”、“偏低”或“无影响”)
含量测定结果的影响(填“偏高”、“偏低”或“无影响”)a.锥形瓶用蒸馏水洗净后没有干燥
b.读取KMnO4标准溶液体积时,开始仰视读数,滴定结束时俯视读数
您最近一年使用:0次
名校
9 . 煤炭是重要的化工原料,但属于不可再生能源,高效、清洁地利用煤炭资源至关重要。回答下列问题:
(1)煤的干馏反应中ΔS___ 0(填“>”、“<”或“=”)。
(2)煤的液化的原理是C(s)+H2O(g) CO(g)+H2(g) ΔH=akJ/mol;CO(g)+2H2(g)
CO(g)+H2(g) ΔH=akJ/mol;CO(g)+2H2(g) CH3OH(l) ΔH=bkJ/mol。则反应C(s)+H2O(g)+H2(g)
CH3OH(l) ΔH=bkJ/mol。则反应C(s)+H2O(g)+H2(g) CH3OH(l)的ΔH=
CH3OH(l)的ΔH=___ kJ/mol。
(3)煤的气化的原理是C(s)+2H2(g) CH4(g) ΔH。在1L密闭容器中投入1mol碳,并充入2molH2,测得相关数据如图所示。
CH4(g) ΔH。在1L密闭容器中投入1mol碳,并充入2molH2,测得相关数据如图所示。

①有关图1、图2的说法正确的有___ (填字母)。
a.p1<6MPa b.T1<1000K
c.ΔH>0 d.工业生产中,当温度为T2时,压强越高,经济效益越好
②图2中A点对应的平衡常数Kp=___ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
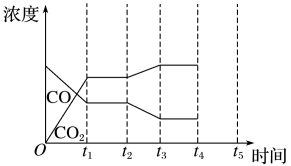
(4)煤可以生产水煤气。如图是反应CO(g)+H2O(g) H2(g)+CO2(g) ΔH<0中CO和CO2的浓度随时间发生变化的曲线,则t2时刻改变的条件可能是
H2(g)+CO2(g) ΔH<0中CO和CO2的浓度随时间发生变化的曲线,则t2时刻改变的条件可能是___ (写出1种即可);若t4时刻通过改变容积的方法将压强增大为原来的2倍,在图中t4~t5区间内画出CO、CO2浓度变化曲线,并标明物质名称(假设各物质状态均保持不变)___ 。
(1)煤的干馏反应中ΔS
(2)煤的液化的原理是C(s)+H2O(g)
 CO(g)+H2(g) ΔH=akJ/mol;CO(g)+2H2(g)
CO(g)+H2(g) ΔH=akJ/mol;CO(g)+2H2(g) CH3OH(l) ΔH=bkJ/mol。则反应C(s)+H2O(g)+H2(g)
CH3OH(l) ΔH=bkJ/mol。则反应C(s)+H2O(g)+H2(g) CH3OH(l)的ΔH=
CH3OH(l)的ΔH=(3)煤的气化的原理是C(s)+2H2(g)
 CH4(g) ΔH。在1L密闭容器中投入1mol碳,并充入2molH2,测得相关数据如图所示。
CH4(g) ΔH。在1L密闭容器中投入1mol碳,并充入2molH2,测得相关数据如图所示。
①有关图1、图2的说法正确的有
a.p1<6MPa b.T1<1000K
c.ΔH>0 d.工业生产中,当温度为T2时,压强越高,经济效益越好
②图2中A点对应的平衡常数Kp=
(4)煤可以生产水煤气。如图是反应CO(g)+H2O(g)
 H2(g)+CO2(g) ΔH<0中CO和CO2的浓度随时间发生变化的曲线,则t2时刻改变的条件可能是
H2(g)+CO2(g) ΔH<0中CO和CO2的浓度随时间发生变化的曲线,则t2时刻改变的条件可能是
您最近一年使用:0次
名校
10 . 某温度下,在恒容密闭容器中加入一定量X,发生反应2X(g) Y(s)+Z(g),一段时间后达到平衡。下列说法错误的是
Y(s)+Z(g),一段时间后达到平衡。下列说法错误的是
 Y(s)+Z(g),一段时间后达到平衡。下列说法错误的是
Y(s)+Z(g),一段时间后达到平衡。下列说法错误的是| A.加入一定量氩气,平衡不移动 |
| B.加入一定量X,达新平衡后α(X)不变 |
| C.加入一定量Z,达新平衡后m(Y)减小 |
| D.升高温度,若c(Z)增大,则△H>0 |
您最近一年使用:0次
2021-12-10更新
|
431次组卷
|
2卷引用:辽宁省沈阳市重点高中联合体2021-2022学年高三12月考试化学试题



