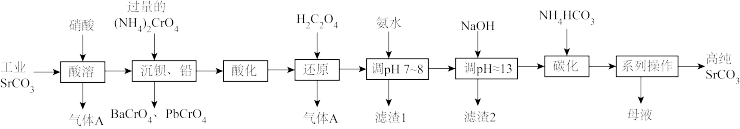
碳酸锶(SrCO3)难溶于水,主要用于电磁材料和金属冶炼。一种由工业碳酸锶(含少量Ba2+、Ca2+、Mg2+、 Pb2+等)制备高纯碳酸锶的工艺流程如下:
已知:I. Cr(OH)3为两性氢氧化物;
II.常温下,各物质的溶度积常数如下表所示。
回答下列问题:
(1)气体A的电子式为_______ 。
(2)“除钡、铅”时,pH过低会导致(NH4)2CrO4的利用率降低,原因为_______ (用离子方程式解释);“还原”时发生反应的离子方程式为_______ 。
(3)“滤渣1”的主要成分为_______ (填化学式)。
(4)用氨水和NaOH分步调节pH,而不是直接调节溶液的pH≈13的原因为_______ 。
(5)“调pH ≈13”后需对溶液进行煮沸并趁热过滤出滤渣2,煮沸并趁热过滤的原因为_______ 。
(6)已知:碳酸的电离常数Ka1=4.4×10-7、Ka2=4.7×10-11,则“碳化”时,反应Sr2+(aq)+2HCO (aq)
(aq) SrCO3(s)+H2CO3(aq)的平衡常数K=
SrCO3(s)+H2CO3(aq)的平衡常数K=_______ (保留两位有效数字)。
(7)“系列操作”中包含“200°C烘干”操作,烘干过程中除蒸发水分外,还能够除去SrCO3中的微量可溶性杂质,该杂质除NH4HCO3外还可能为_______ (填化学式)。

已知:I. Cr(OH)3为两性氢氧化物;
II.常温下,各物质的溶度积常数如下表所示。
| 化合物 | Cr(OH)3 | Ca(OH)2 | Mg(OH)2 | SrCO3 |
| Ksp近似值 | 1×10-31 | 5.5×10-6 | 1.8×10-11 | 5.6×10-10 |
(1)气体A的电子式为
(2)“除钡、铅”时,pH过低会导致(NH4)2CrO4的利用率降低,原因为
(3)“滤渣1”的主要成分为
(4)用氨水和NaOH分步调节pH,而不是直接调节溶液的pH≈13的原因为
(5)“调pH ≈13”后需对溶液进行煮沸并趁热过滤出滤渣2,煮沸并趁热过滤的原因为
(6)已知:碳酸的电离常数Ka1=4.4×10-7、Ka2=4.7×10-11,则“碳化”时,反应Sr2+(aq)+2HCO
 (aq)
(aq) SrCO3(s)+H2CO3(aq)的平衡常数K=
SrCO3(s)+H2CO3(aq)的平衡常数K=(7)“系列操作”中包含“200°C烘干”操作,烘干过程中除蒸发水分外,还能够除去SrCO3中的微量可溶性杂质,该杂质除NH4HCO3外还可能为
2022·河北石家庄·一模 查看更多[13]
河北省石家庄市2022届高三毕业班教学质量检测二(一模)化学试题(已下线)秘籍17 工艺流程的条件控制与计算-备战2022年高考化学抢分秘籍(全国通用)(已下线)专项15 工艺流程综合题-备战2022年高考化学阶段性新题精选专项特训(全国卷)(4月期)(已下线)化学-2022年高考押题预测卷01(山东卷)(已下线)化学-2022年高考考前押题密卷(湖南卷)(已下线)化学-2022年高考考前押题密卷(重庆卷)湖北省宜昌市夷陵中学2022届高三5月第二次限时训练(四模)化学试题辽宁省抚顺市第二中学2021-2022学年高三上学期10月月考化学试题山东省鄄城县第一中学2022-2023学年高二上学期期末考试化学试题湖北省宜昌英杰学校2021-2022学年高三上学期9月月考化学试题湖南省株洲市九方中学2022-2023学年高三上学期第一次月考化学试题(已下线)河北省石家庄市2022届高三毕业班教学质量检测二(一模)(工业流程题)湖南省邵阳市第一中学2023届高三第五次月考化学试题
更新时间:2022-04-09 17:08:14
|
相似题推荐
【推荐1】重铬酸钾 具有强氧化性,在实验室和工业中都有广泛的应用。
具有强氧化性,在实验室和工业中都有广泛的应用。 (黄色)和
(黄色)和 (橙色)在溶液中可相互转化。
(橙色)在溶液中可相互转化。
(1) 中元素铬(Cr)的化合价为
中元素铬(Cr)的化合价为_______ 。
(2)室温下,初始浓度为 的
的 溶液中
溶液中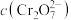 随
随 的变化如图所示。(忽略溶液体积变化)
的变化如图所示。(忽略溶液体积变化)

①用离子方程式表示 溶液中的转化反应
溶液中的转化反应_______ 。
②计算B点时 的转化率为
的转化率为_______ 。
③根据A点数据,计算上述反应的平衡常数_______ 。
(3)向橙色的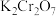 溶液中,滴加
溶液中,滴加 溶液,产生黄色沉淀,溶液pH减小。试推测黄色沉淀是
溶液,产生黄色沉淀,溶液pH减小。试推测黄色沉淀是_______ ,用平衡移动的原理解释溶液pH变小的原因是_______ 。
(4)用重铬酸钾法(一种氧化还原滴定法)可测定二价铁含量。
用 溶液滴定20.00mL未知浓度的含
溶液滴定20.00mL未知浓度的含 的溶液,恰好完全反应时消耗
的溶液,恰好完全反应时消耗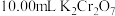 溶液,则溶液中
溶液,则溶液中 的物质的量浓度是
的物质的量浓度是_______ (已知: (未配平)。
(未配平)。
 具有强氧化性,在实验室和工业中都有广泛的应用。
具有强氧化性,在实验室和工业中都有广泛的应用。 (黄色)和
(黄色)和 (橙色)在溶液中可相互转化。
(橙色)在溶液中可相互转化。(1)
 中元素铬(Cr)的化合价为
中元素铬(Cr)的化合价为(2)室温下,初始浓度为
 的
的 溶液中
溶液中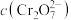 随
随 的变化如图所示。(忽略溶液体积变化)
的变化如图所示。(忽略溶液体积变化)
①用离子方程式表示
 溶液中的转化反应
溶液中的转化反应②计算B点时
 的转化率为
的转化率为③根据A点数据,计算上述反应的平衡常数
(3)向橙色的
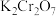 溶液中,滴加
溶液中,滴加 溶液,产生黄色沉淀,溶液pH减小。试推测黄色沉淀是
溶液,产生黄色沉淀,溶液pH减小。试推测黄色沉淀是(4)用重铬酸钾法(一种氧化还原滴定法)可测定二价铁含量。
用
 溶液滴定20.00mL未知浓度的含
溶液滴定20.00mL未知浓度的含 的溶液,恰好完全反应时消耗
的溶液,恰好完全反应时消耗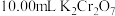 溶液,则溶液中
溶液,则溶液中 的物质的量浓度是
的物质的量浓度是 (未配平)。
(未配平)。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】(1)若适量的N2和O2完全反应,每生成23克NO2需要吸收16.95kJ的热量。写出该反应的热化学方程式_______ 。
(2)若25℃,101 kPa下,1 g CH4完全燃烧生成液态水和CO2气体,放出55.6 kJ的热量,则甲烷的燃烧热为_______ 。
(3)对于下列反应:2SO2(g)+ O2(g)⇌2SO3(g),如果2min内SO2的浓度由6 mol/L下降为2 mol/L,那么,用SO2浓度变化来表示的化学反应速率为_______ 。如果开始时SO2浓度为4mol/L,2min后反应达平衡,若这段时间内v(O2)为0.5mol/(L·min),那么2min时SO2的浓度为_______ 。
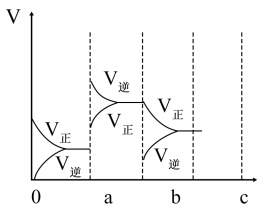
(4)下图表示在密闭容器中反应:2SO2(g)+O2(g)⇌2SO3(g) △H<0达到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况,ab过程中改变的条件可能是____ ;bc过程中改变的条件可能是_____ 。
(2)若25℃,101 kPa下,1 g CH4完全燃烧生成液态水和CO2气体,放出55.6 kJ的热量,则甲烷的燃烧热为
(3)对于下列反应:2SO2(g)+ O2(g)⇌2SO3(g),如果2min内SO2的浓度由6 mol/L下降为2 mol/L,那么,用SO2浓度变化来表示的化学反应速率为
(4)下图表示在密闭容器中反应:2SO2(g)+O2(g)⇌2SO3(g) △H<0达到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况,ab过程中改变的条件可能是

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】探究化学反应的快慢和限度具有十分重要的意义。
Ⅰ.某实验小组欲通过用酸性KMnO4和H2C2O4(草酸)反应测定单位时间内生成CO2的速率研究影响反应速率的因素,设计实验方案如下(KMnO4溶液已酸化),实验装置如图甲所示:

(1)上述反应的离子方程式为:___ ,该实验探究的是___ 对化学反应速率的影响。
(2)若实验①在2min末收集了4.48mLCO2(标准状况下),则在2min末,c(MnO )=
)=____ mol·L-1(假设混合溶液的体积为50mL,反应前后体积变化忽略不计)。
(3)除通过测定一定时间内CO2的体积来比较反应速率外,本实验还可通过测定____ 来比较化学反应速率。
(4)小组同学发现反应速率变化如图乙,其中t1~t2时间内速率变快的主要原因可能是:___ 。
Ⅱ.K2Cr2O7溶液中存在平衡:Cr2O (橙色)+H2O
(橙色)+H2O 2CrO
2CrO (黄色)+2H+。用K2Cr2O7溶液进行下列实验:
(黄色)+2H+。用K2Cr2O7溶液进行下列实验:

(5)向K2Cr2O7溶液中加入30%NaOH溶液,溶液呈____ 色,若再加入过量稀硫酸,则溶液呈____ 色。
(6)向K2Cr2O7溶液中逐滴加入Ba(NO3)2溶液(已知BaCrO4为黄色沉淀),则平衡向着____ 方向移动,溶液颜色变化为___ 。对比实验②和④可得出的结论是___ 。
Ⅰ.某实验小组欲通过用酸性KMnO4和H2C2O4(草酸)反应测定单位时间内生成CO2的速率研究影响反应速率的因素,设计实验方案如下(KMnO4溶液已酸化),实验装置如图甲所示:

| 实验序号 | A溶液 | B溶液 |
| ① | 20mL0.1mol·L-1 H2C2O4溶液 | 30mL0.01mol·L-1 KMnO4溶液 |
| ② | 20mL0.2mol·L-1 H2C2O4溶液 | 30mL0.01mol·L-1 KMnO4溶液 |
(2)若实验①在2min末收集了4.48mLCO2(标准状况下),则在2min末,c(MnO
 )=
)=(3)除通过测定一定时间内CO2的体积来比较反应速率外,本实验还可通过测定
(4)小组同学发现反应速率变化如图乙,其中t1~t2时间内速率变快的主要原因可能是:
Ⅱ.K2Cr2O7溶液中存在平衡:Cr2O
 (橙色)+H2O
(橙色)+H2O 2CrO
2CrO (黄色)+2H+。用K2Cr2O7溶液进行下列实验:
(黄色)+2H+。用K2Cr2O7溶液进行下列实验:
(5)向K2Cr2O7溶液中加入30%NaOH溶液,溶液呈
(6)向K2Cr2O7溶液中逐滴加入Ba(NO3)2溶液(已知BaCrO4为黄色沉淀),则平衡向着
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】Ⅰ.结合下表回答下列问题(均为常温下的数据):请回答下列问题:
(1)同浓度的 、
、 、
、 、
、 、
、 、
、 中结合
中结合 的能力最强的
的能力最强的_________ 。
(2)常温下0.1mol/L的 溶液在加水稀释过程中,下列表达式的数据一定变小的是_________(填字母)。
溶液在加水稀释过程中,下列表达式的数据一定变小的是_________(填字母)。
(3)取等体积物质的量浓度相等的 、HClO两溶液,分别用等浓度的NaOH稀溶液中和,则消耗的NaOH溶液的体积大小关系为:
、HClO两溶液,分别用等浓度的NaOH稀溶液中和,则消耗的NaOH溶液的体积大小关系为:
_________  (填“>”、“<”或“=”)
(填“>”、“<”或“=”)
Ⅱ.在两个体积均为2L的恒容密闭容器A、B中,起始投料如下表所示,在753K下进行反应: △H>0,
△H>0, 的平衡转化率如下表所示:
的平衡转化率如下表所示:
(4)容器A中,反应从开始到达平衡状态所用的时间为2min,则2min内该反应的平均反应速率为:
_________
(5)753K时,该反应的平衡常数K=_________ ;容器B中反应起始时v(正)_________ (填“>”“<”或“=”)v(逆)。
| 酸 | 电离常数(Ka) | 酸 | 电离常数(Ka) |
 |  |  |   |
| HClO |  |  |   |
 |  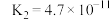 |
 、
、 、
、 、
、 、
、 、
、 中结合
中结合 的能力最强的
的能力最强的(2)常温下0.1mol/L的
 溶液在加水稀释过程中,下列表达式的数据一定变小的是_________(填字母)。
溶液在加水稀释过程中,下列表达式的数据一定变小的是_________(填字母)。A. | B. | C. | D. |
 、HClO两溶液,分别用等浓度的NaOH稀溶液中和,则消耗的NaOH溶液的体积大小关系为:
、HClO两溶液,分别用等浓度的NaOH稀溶液中和,则消耗的NaOH溶液的体积大小关系为:
 (填“>”、“<”或“=”)
(填“>”、“<”或“=”) Ⅱ.在两个体积均为2L的恒容密闭容器A、B中,起始投料如下表所示,在753K下进行反应:
 △H>0,
△H>0, 的平衡转化率如下表所示:
的平衡转化率如下表所示:| 容器 | 起始物质的量(n)/mol |  的平衡转化率 的平衡转化率 | |||
 |  | CO |  | ||
| A | 1 | 1 | 0 | 0 | 50% |
| B | 1 | 1 | 2 | 2 | |

(5)753K时,该反应的平衡常数K=
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】废弃物回收利用可变废为宝。某工业固体废物的组成为Al2O3、FeO、Fe2O3等。下图是以该固体废物为原料制取氧化铝、磁性Fe3O4胶体粒子的一种工艺流程:

(1)检验制备Fe3O4胶体粒子成功的实验操作名称是____________________________ 。
(2)写出由溶液B制备磁性Fe3O4胶体粒子的离子方程式___________________________ 。
(3)由溶液B制得Fe3O4胶体粒子的过程中,须持续通入N2。其原因是____________________________ 。
(4)向溶液C中加入NaHCO3溶液,溶液的pH_________ (填“增大”,“不变”或“减小”)。
(5)固体D是Al(OH)3,常温时Al(OH)3溶于NaOH溶液反应的平衡常数等于20,则此时Al(OH)3 A1O2-+H++H2O的电离常数K=
A1O2-+H++H2O的电离常数K=_______________ 。
(6)用重铬酸钾(K2Cr2O7)可测定产物磁性Fe3O4胶体粒子中铁元素的含量,过程如下图。已知,反应中K2Cr2O7被还原为Cr3+。
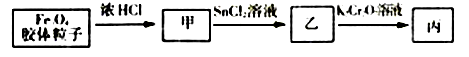
①写出甲→乙的化学方程式___________________________________ 。
②写出乙→丙的离子方程式_________________________________________ 。

(1)检验制备Fe3O4胶体粒子成功的实验操作名称是
(2)写出由溶液B制备磁性Fe3O4胶体粒子的离子方程式
(3)由溶液B制得Fe3O4胶体粒子的过程中,须持续通入N2。其原因是
(4)向溶液C中加入NaHCO3溶液,溶液的pH
(5)固体D是Al(OH)3,常温时Al(OH)3溶于NaOH溶液反应的平衡常数等于20,则此时Al(OH)3
 A1O2-+H++H2O的电离常数K=
A1O2-+H++H2O的电离常数K=(6)用重铬酸钾(K2Cr2O7)可测定产物磁性Fe3O4胶体粒子中铁元素的含量,过程如下图。已知,反应中K2Cr2O7被还原为Cr3+。
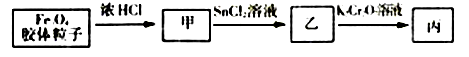
①写出甲→乙的化学方程式
②写出乙→丙的离子方程式
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】相同条件下,下列五种溶液:
①0.1 mol•L-1NH4Cl溶液 ②0.1 mol•L-1CH3COONH4溶液 ③0.1 mol•L-1NH4HSO4溶液 ④0.1 mol•L-1氨水 ⑤NH4Al(SO4)2溶液
请根据要求填写下列空白:
(1)溶液①呈_______ (填“酸”、“碱”或“中”)性,其原因是_______ (用离子方程式表示)。
(2)溶液①②③④中c(NH )由大到小的顺序是
)由大到小的顺序是_______ 。
(3)25℃时,将amol•L-1的氨水与0.1mol•L-1的盐酸等体积混合,反应平衡时溶液中c(NH )=c(Cl-),则溶液显
)=c(Cl-),则溶液显_______ 性(填“酸”、“碱”或“中”)
(4)常温下,某水溶液M中存在的离子有Na+、A2-、HA-、H+、OH-,存在的分子有H2O、H2A。
①写出酸H2A的电离方程式:_______ 。
②若溶液M由10mL 2mol•L-1NaHA溶液与10mL 2mol•L-1NaOH溶液混合而得,请写出溶液中各离子浓度大小关系_______ 。
(5)NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品中。图是0.1 mol•L-1电解质溶液的pH随温度变化的图象。

①其中符合0.1 mol•L-1NH4Al(SO4)2的pH随温度变化的曲线是_______ (填字母)。
②室温下0.1 mol•L-1NH4Al(SO4)2中2c(SO )-c(NH
)-c(NH )-3c(Al3+)=
)-3c(Al3+)=_______ mol•L-1。
①0.1 mol•L-1NH4Cl溶液 ②0.1 mol•L-1CH3COONH4溶液 ③0.1 mol•L-1NH4HSO4溶液 ④0.1 mol•L-1氨水 ⑤NH4Al(SO4)2溶液
请根据要求填写下列空白:
(1)溶液①呈
(2)溶液①②③④中c(NH
 )由大到小的顺序是
)由大到小的顺序是(3)25℃时,将amol•L-1的氨水与0.1mol•L-1的盐酸等体积混合,反应平衡时溶液中c(NH
 )=c(Cl-),则溶液显
)=c(Cl-),则溶液显(4)常温下,某水溶液M中存在的离子有Na+、A2-、HA-、H+、OH-,存在的分子有H2O、H2A。
①写出酸H2A的电离方程式:
②若溶液M由10mL 2mol•L-1NaHA溶液与10mL 2mol•L-1NaOH溶液混合而得,请写出溶液中各离子浓度大小关系
(5)NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品中。图是0.1 mol•L-1电解质溶液的pH随温度变化的图象。

①其中符合0.1 mol•L-1NH4Al(SO4)2的pH随温度变化的曲线是
②室温下0.1 mol•L-1NH4Al(SO4)2中2c(SO
 )-c(NH
)-c(NH )-3c(Al3+)=
)-3c(Al3+)=
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】氧化钇( )广泛应用于微波、军工、光学玻璃、陶瓷、激光、超导等许多尖端行业。利用废荧光粉(主要成分为ZnO、
)广泛应用于微波、军工、光学玻璃、陶瓷、激光、超导等许多尖端行业。利用废荧光粉(主要成分为ZnO、 ,还含有一定量的
,还含有一定量的 、
、 、MgO)等)为原料生产
、MgO)等)为原料生产 的工艺流程如图所示:
的工艺流程如图所示: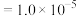 mol⋅L
mol⋅L 时,认为已沉淀完全。
时,认为已沉淀完全。
②常温下,相关金属离子开始沉淀和沉淀完全时的pH如图所示:
(1)“酸浸”时需适当提高浸取液的温度,其目的是_______ ;
采用离子浓度传感器测得相同时间内 的浸取率与浸取溶液温度的关系如图所示,
的浸取率与浸取溶液温度的关系如图所示, ℃后,
℃后, 的浸取率随温度升高而减小的原因是
的浸取率随温度升高而减小的原因是_______ 。_______ (填化学式)。
(3)“沉钇”后的滤液中浓度最大的金属离子是_______ (填离子符号);若常温下测得 恰好沉淀完全时滤液中
恰好沉淀完全时滤液中 mol⋅L
mol⋅L ,则
,则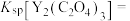
_______ mol⋅L (保留两位有效数字)。
(保留两位有效数字)。
(4)“沉钇”后所得晶体为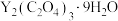 ,其中C元素的化合价为
,其中C元素的化合价为_______ 。
(5)“焙烧”时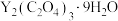 发生反应的化学方程式为
发生反应的化学方程式为_______ 。
 )广泛应用于微波、军工、光学玻璃、陶瓷、激光、超导等许多尖端行业。利用废荧光粉(主要成分为ZnO、
)广泛应用于微波、军工、光学玻璃、陶瓷、激光、超导等许多尖端行业。利用废荧光粉(主要成分为ZnO、 ,还含有一定量的
,还含有一定量的 、
、 、MgO)等)为原料生产
、MgO)等)为原料生产 的工艺流程如图所示:
的工艺流程如图所示: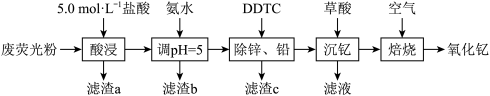
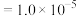 mol⋅L
mol⋅L 时,认为已沉淀完全。
时,认为已沉淀完全。②常温下,相关金属离子开始沉淀和沉淀完全时的pH如图所示:

(1)“酸浸”时需适当提高浸取液的温度,其目的是
采用离子浓度传感器测得相同时间内
 的浸取率与浸取溶液温度的关系如图所示,
的浸取率与浸取溶液温度的关系如图所示, ℃后,
℃后, 的浸取率随温度升高而减小的原因是
的浸取率随温度升高而减小的原因是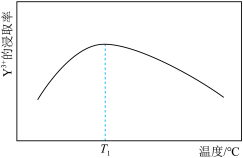
(3)“沉钇”后的滤液中浓度最大的金属离子是
 恰好沉淀完全时滤液中
恰好沉淀完全时滤液中 mol⋅L
mol⋅L ,则
,则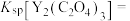
 (保留两位有效数字)。
(保留两位有效数字)。(4)“沉钇”后所得晶体为
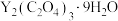 ,其中C元素的化合价为
,其中C元素的化合价为(5)“焙烧”时
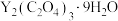 发生反应的化学方程式为
发生反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】 (三氯化六氨合钴)是一种橙黄色的晶体,溶于热水和稀盐酸中,在冷水、乙醇、浓盐酸中溶解度较小,可用于制备其他三价钴配合物。实验室制备
(三氯化六氨合钴)是一种橙黄色的晶体,溶于热水和稀盐酸中,在冷水、乙醇、浓盐酸中溶解度较小,可用于制备其他三价钴配合物。实验室制备 的装置和步骤如下:
的装置和步骤如下: 高纯水,加热溶解后加入1.5g催化剂活性炭,7mL浓氨水,搅拌,得到
高纯水,加热溶解后加入1.5g催化剂活性炭,7mL浓氨水,搅拌,得到 溶液。
溶液。
Ⅱ.将得到的 溶液冷却至10℃,加入7mL4%的
溶液冷却至10℃,加入7mL4%的 ,恒温
,恒温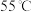 ,搅拌15min后冷却至2℃,抽滤,收集沉淀。
,搅拌15min后冷却至2℃,抽滤,收集沉淀。
Ⅲ.将沉淀转移入100mL烧杯中,用20mL、80℃的高纯水进行冲洗,再加入1mL的浓盐酸,搅拌均匀,_______,将活性炭滤出弃去。
Ⅳ.在滤液中加入3.5mL试剂b,搅拌后用冰水浴冷却至2℃析出沉淀,之后快速抽滤,弃去滤液,用无水乙醇洗涤沉淀3次,低温烘干,得到产品1.92g。
回答下列问题:
(1)仪器a的名称为_______ ,盛放的试剂是_______ 。
(2)常温下, ,从平衡角度解释,步骤I中先加NH4Cl,后加浓氨水的原因是
,从平衡角度解释,步骤I中先加NH4Cl,后加浓氨水的原因是_______ 。
(3)步骤Ⅲ中缺少的操作名称为_______ 。
(4)步骤Ⅳ中试剂b最好选择的是_______ (填标号)。
A.浓盐酸 B.稀盐酸 C.水
(5)由 制备
制备 的化学方程式为
的化学方程式为_______ 。
(6) 晶体中存在的化学键类型有_______(填标号)。
晶体中存在的化学键类型有_______(填标号)。
 (三氯化六氨合钴)是一种橙黄色的晶体,溶于热水和稀盐酸中,在冷水、乙醇、浓盐酸中溶解度较小,可用于制备其他三价钴配合物。实验室制备
(三氯化六氨合钴)是一种橙黄色的晶体,溶于热水和稀盐酸中,在冷水、乙醇、浓盐酸中溶解度较小,可用于制备其他三价钴配合物。实验室制备 的装置和步骤如下:
的装置和步骤如下: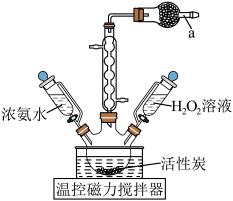
 高纯水,加热溶解后加入1.5g催化剂活性炭,7mL浓氨水,搅拌,得到
高纯水,加热溶解后加入1.5g催化剂活性炭,7mL浓氨水,搅拌,得到 溶液。
溶液。Ⅱ.将得到的
 溶液冷却至10℃,加入7mL4%的
溶液冷却至10℃,加入7mL4%的 ,恒温
,恒温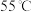 ,搅拌15min后冷却至2℃,抽滤,收集沉淀。
,搅拌15min后冷却至2℃,抽滤,收集沉淀。Ⅲ.将沉淀转移入100mL烧杯中,用20mL、80℃的高纯水进行冲洗,再加入1mL的浓盐酸,搅拌均匀,_______,将活性炭滤出弃去。
Ⅳ.在滤液中加入3.5mL试剂b,搅拌后用冰水浴冷却至2℃析出沉淀,之后快速抽滤,弃去滤液,用无水乙醇洗涤沉淀3次,低温烘干,得到产品1.92g。
回答下列问题:
(1)仪器a的名称为
(2)常温下,
 ,从平衡角度解释,步骤I中先加NH4Cl,后加浓氨水的原因是
,从平衡角度解释,步骤I中先加NH4Cl,后加浓氨水的原因是(3)步骤Ⅲ中缺少的操作名称为
(4)步骤Ⅳ中试剂b最好选择的是
A.浓盐酸 B.稀盐酸 C.水
(5)由
 制备
制备 的化学方程式为
的化学方程式为(6)
 晶体中存在的化学键类型有_______(填标号)。
晶体中存在的化学键类型有_______(填标号)。| A.σ键 | B.π键 | C.离子键 | D.配位键 |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】一种以含镍废料(含NiS、Al2O3、FeO、CaO、SiO2)为原料制取醋酸镍的工艺流程图如下:

相关离子生成氢氧化物的pH和相关物质的溶解性如下表:
(1)调节pH步骤中,溶液pH的调节范围是______________ 。
(2)滤渣1和滤渣3主要成分的化学式分别是_____________ 、__________________ 。
(3)酸浸过程中,1 molNiS失去6NA个电子,同时生成两种无色有毒气体。写出该反应的化学方程式________________________________ 。
(4)沉镍过程中,若c(Ni2+)=2.0mol·L-1,欲使100mL该滤液中的Ni2+沉淀完全[c(Ni2+)≤10-5 mol·L-1,则需要加入Na2CO3固体的质量最少为_________ g。(保留小数点后1位有效数字)。
(5)保持其他条件不变,在不同温度下对含镍废料进行酸浸,镍浸出率随时间变化如图。酸浸的最佳温度与时间为_______________ 。


相关离子生成氢氧化物的pH和相关物质的溶解性如下表:
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH | 物质 | 20℃时溶解性(H2O) |
| Fe3+ | 1.1 | 3.2 | CaSO4 | 微溶 |
| Fe2+ | 5.8 | 8.8 | NiF | 可溶 |
| A13+ | 3.0 | 5.0 | CaF2 | 难溶 |
| Ni2+ | 6.7 | 9.5 | NiCO3 | Ksp=9.60×10-6 |
(1)调节pH步骤中,溶液pH的调节范围是
(2)滤渣1和滤渣3主要成分的化学式分别是
(3)酸浸过程中,1 molNiS失去6NA个电子,同时生成两种无色有毒气体。写出该反应的化学方程式
(4)沉镍过程中,若c(Ni2+)=2.0mol·L-1,欲使100mL该滤液中的Ni2+沉淀完全[c(Ni2+)≤10-5 mol·L-1,则需要加入Na2CO3固体的质量最少为
(5)保持其他条件不变,在不同温度下对含镍废料进行酸浸,镍浸出率随时间变化如图。酸浸的最佳温度与时间为

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】五氧化二钽( )主要用作钽酸锂单晶和制造高折射低色散特种光学玻璃等。一种以含钽废料(主要成分为
)主要用作钽酸锂单晶和制造高折射低色散特种光学玻璃等。一种以含钽废料(主要成分为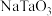 、
、 以及少量的FeO、
以及少量的FeO、 、
、 等)为原料制备
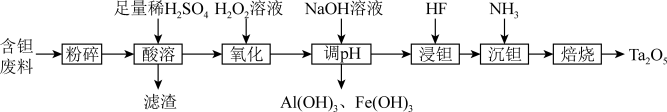
等)为原料制备 的工艺流程如图所示:
的工艺流程如图所示:
已知: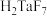 是弱酸。回答下列问题:
是弱酸。回答下列问题:
(1)“酸溶”时, 发生反应的基本反应类型为
发生反应的基本反应类型为_______ ,滤渣的主要成分是_______ (填化学式)。
(2)“氧化”时,发生反应的离子方程式为_______ 。
(3)常温下,“调pH”时,若过滤出沉淀后溶液的pH=5,列式计算 是否沉淀完全?
是否沉淀完全?_______ [已知:常温下,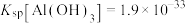 ,溶液中离子浓度小于或等于
,溶液中离子浓度小于或等于 时可视为沉淀完全]。
时可视为沉淀完全]。
(4)“浸钽”时,加入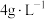 的HF溶液,浸出时间为4h,钽的浸出率随温度的变化如图所示。该HF溶液的物质的量浓度为
的HF溶液,浸出时间为4h,钽的浸出率随温度的变化如图所示。该HF溶液的物质的量浓度为_______  ,浸出的最佳温度为
,浸出的最佳温度为_______ ℃;“调pH”后,溶液中溶质主要为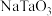 ,写出“浸钽”时生成
,写出“浸钽”时生成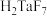 ,的离子方程式:
,的离子方程式:_______ 。

(5)“沉钽”时,生成 ,反应化学方程式为
,反应化学方程式为_______ 。
(6)本流程中使用钽废料100t,若得到85.0t纯净的 ,假设钽元素有85%转化为
,假设钽元素有85%转化为 ,则含钽废料中钽元素的质量分数为
,则含钽废料中钽元素的质量分数为_______ %(保留四位有效数字)。
 )主要用作钽酸锂单晶和制造高折射低色散特种光学玻璃等。一种以含钽废料(主要成分为
)主要用作钽酸锂单晶和制造高折射低色散特种光学玻璃等。一种以含钽废料(主要成分为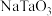 、
、 以及少量的FeO、
以及少量的FeO、 、
、 等)为原料制备
等)为原料制备 的工艺流程如图所示:
的工艺流程如图所示:
已知:
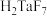 是弱酸。回答下列问题:
是弱酸。回答下列问题:(1)“酸溶”时,
 发生反应的基本反应类型为
发生反应的基本反应类型为(2)“氧化”时,发生反应的离子方程式为
(3)常温下,“调pH”时,若过滤出沉淀后溶液的pH=5,列式计算
 是否沉淀完全?
是否沉淀完全?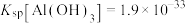 ,溶液中离子浓度小于或等于
,溶液中离子浓度小于或等于 时可视为沉淀完全]。
时可视为沉淀完全]。(4)“浸钽”时,加入
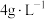 的HF溶液,浸出时间为4h,钽的浸出率随温度的变化如图所示。该HF溶液的物质的量浓度为
的HF溶液,浸出时间为4h,钽的浸出率随温度的变化如图所示。该HF溶液的物质的量浓度为 ,浸出的最佳温度为
,浸出的最佳温度为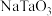 ,写出“浸钽”时生成
,写出“浸钽”时生成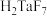 ,的离子方程式:
,的离子方程式:
(5)“沉钽”时,生成
 ,反应化学方程式为
,反应化学方程式为(6)本流程中使用钽废料100t,若得到85.0t纯净的
 ,假设钽元素有85%转化为
,假设钽元素有85%转化为 ,则含钽废料中钽元素的质量分数为
,则含钽废料中钽元素的质量分数为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】保山矿产资源丰富,其中铍矿的储量居云南省第二,是保山重要的矿产资源。某研究性学习小组利用本地铍矿石(含 和少量
和少量 )分离回收金属,设计流程如图:
)分离回收金属,设计流程如图:

已知:铍与铝化学性质相似, 熔融时能微弱电离。回答下列问题:
熔融时能微弱电离。回答下列问题:
(1)操作1的名称是_______ , 和
和 溶液反应的化学方程式是
溶液反应的化学方程式是_______ 。
(2) 的核外电子排布式是
的核外电子排布式是_______ ,写出 与稀
与稀 反应的离子方程式:
反应的离子方程式:_______ 。 的空间结构名称是
的空间结构名称是_______ 。
(3)从 溶液中获得
溶液中获得 晶体的操作是
晶体的操作是_______ 。电解熔融 制
制 时,除了需高温、通电外,还需加入一定量的
时,除了需高温、通电外,还需加入一定量的 ,原因是
,原因是_______ 。
(4)已知常温下, ,溶液2中
,溶液2中 ,要实现
,要实现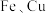 的分离,应调节溶液的
的分离,应调节溶液的 值不大于
值不大于_______ 。
 和少量
和少量 )分离回收金属,设计流程如图:
)分离回收金属,设计流程如图:
已知:铍与铝化学性质相似,
 熔融时能微弱电离。回答下列问题:
熔融时能微弱电离。回答下列问题:(1)操作1的名称是
 和
和 溶液反应的化学方程式是
溶液反应的化学方程式是(2)
 的核外电子排布式是
的核外电子排布式是 与稀
与稀 反应的离子方程式:
反应的离子方程式: 的空间结构名称是
的空间结构名称是(3)从
 溶液中获得
溶液中获得 晶体的操作是
晶体的操作是 制
制 时,除了需高温、通电外,还需加入一定量的
时,除了需高温、通电外,还需加入一定量的 ,原因是
,原因是(4)已知常温下,
 ,溶液2中
,溶液2中 ,要实现
,要实现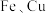 的分离,应调节溶液的
的分离,应调节溶液的 值不大于
值不大于
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】FeCl3是一种常用的净水剂,化学研究两小组甲、乙分别用如图装置制备无水FeCl3并证明产品中没有FeCl2,已知无水FeCl3在空气中易潮解,加热易升华。
I.小组甲拟用下图实验装置来制备无水FeCl3。(每个虚线框表示一个单元装置)

(1)请用文字描述方法改正以上装管的错误_____________ 。
II.小组乙用下列装置组装制备无水FeCl3的装置:
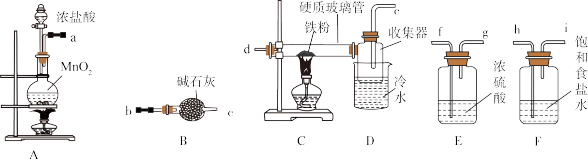
(2)A中发生反应的离子方程式为_______________ 。
(3)装置接口的连接顺序为__________ (用a、b、c……i表示):反应开始前应先点燃____ 处酒精灯(填“A”或“C”)。
(4)装置B的作用_________________ 。
(5)如果拆去E和F装置,可能的后果是___________ 。
(6)证明产品中没有FeCl2的操作____________ 。
I.小组甲拟用下图实验装置来制备无水FeCl3。(每个虚线框表示一个单元装置)

(1)请用文字描述方法改正以上装管的错误
II.小组乙用下列装置组装制备无水FeCl3的装置:

(2)A中发生反应的离子方程式为
(3)装置接口的连接顺序为
(4)装置B的作用
(5)如果拆去E和F装置,可能的后果是
(6)证明产品中没有FeCl2的操作
您最近一年使用:0次



