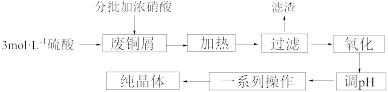
8. 一种利用废铜屑制硫酸铜晶体的实验流程及主要装置如下:

(1)盛浓硝酸的玻璃仪器名称为
_______。写出加浓硝酸刚开始时废铜屑溶解的离子方程式
_______,根据下图分析硝酸的用量如何影响CuSO
4·5H
2O产率
_______
(2)废铜屑中常含有铁、铅等杂质,铅可形成硫酸铅沉淀而除去,某些氢氧化物沉淀的pH如下表所示:
| 氢氧化钠 | 开始沉淀时的pH | 完全沉淀时的pH |
| Cu(OH)2 | 4.2 | 6.7 |
| Fe(OH)3 | 2.7 | 3.7 |
| Fe(OH)2 | 7.6 | 9.6 |
试分析铁元素除去的合适的pH范围
_______,为不引入杂质,调节pH时所加的物质为
_______。
(3)下列有关操作的说法错误的是_______。
| A.也可在烧瓶中先加入废铜屑、水,再缓缓加入浓硫酸、浓硝酸 |
| B.若废铜屑溶解时生成的两种气体与NaOH溶液反应后只生成一种盐,则实验中n(HNO3):n(H2SO4)为1:2 |
| C.趁热过滤时,使用短颈漏斗而不用长颈漏斗 |
| D.析出CuSO4·5H2O晶体的方法同于食盐水中析出氯化钠晶体 |
(4)图中“一系列操作”包含如下步骤,其正确的排序是:
_______a.自然冷却至室温
b.加热蒸发溶液至表面有晶膜出现
c. 停止过滤,取出晶体,置于滤纸上,再覆盖一-张纸,轻压吸干残液
d.用95%乙醇代替蒸馏水洗涤
e.减压过滤
(5)已知: 2Cu
2+ +4I
- =2CuI↓+I
2,I
2+ 2S
2O

=S
4O

+2I
-。称取纯晶体ag加入适量稀硫酸和水配成100mL溶液,每次取20.00mL,加入过量的KI溶液(杂质不参与反应),再加入几滴淀粉溶液,用c mol·L
-1 Na
2S
2O
3溶液滴定至终点,平均消耗Na
2S
2O
3溶液b mL,则所测试样中硫酸铜晶体的纯度为
_______ %