1 . 在其他条件不变的情况下,压强对化学平衡的影响规律
Δvg=(化学方程式中气态反应产物化学式前系数之和)-(化学方程式中气态反应物化学式前系数之和)。
(1)Δvg=0:改变压强,化学平衡___________ ;
(2)Δvg≠0:改变压强,化学平衡向___________ 方向移动。
Δvg=(化学方程式中气态反应产物化学式前系数之和)-(化学方程式中气态反应物化学式前系数之和)。
(1)Δvg=0:改变压强,化学平衡
(2)Δvg≠0:改变压强,化学平衡向
您最近一年使用:0次
名校
2 . 下列事实不能用平衡移动原理解释的是
| A.实验室使用排饱和食盐水的方法收集氯气 |
| B.高压比常压条件更有利于合成氨的反应 |
| C.注射器中的NO2气体,加压后颜色先变深后变浅,但比原来要深 |
| D.700K左右比室温更有利于合成氨的反应 |
您最近一年使用:0次
2022-03-09更新
|
164次组卷
|
2卷引用:湖北省恩施土家族苗族自治州高级中学2023-2024学年高二上学期期中考试化学试题
名校
3 . 对平衡2SO2(g)+O2 (g)  2 SO3 (g); △H= -198kJ/mol,为提高SO2的转化率,应采取的合理措施是
2 SO3 (g); △H= -198kJ/mol,为提高SO2的转化率,应采取的合理措施是
 2 SO3 (g); △H= -198kJ/mol,为提高SO2的转化率,应采取的合理措施是
2 SO3 (g); △H= -198kJ/mol,为提高SO2的转化率,应采取的合理措施是| A.升温、增压 | B.降温、增压 |
| C.升温、减压 | D.降温、减压 |
您最近一年使用:0次
2021-11-03更新
|
597次组卷
|
3卷引用:宁夏固原市第二中学2023-2024学年高二上学期期中考试化学试题
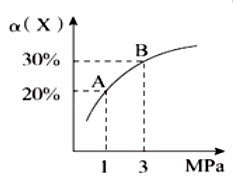
4 . 在一定条件下,反应X(g)+3Y(g) 2Z(g) ∆H=-92.4kJ/mol,X的平衡转化率(α)与体系总压强(P)的关系如图所示。下列说法正确的是
2Z(g) ∆H=-92.4kJ/mol,X的平衡转化率(α)与体系总压强(P)的关系如图所示。下列说法正确的是
 2Z(g) ∆H=-92.4kJ/mol,X的平衡转化率(α)与体系总压强(P)的关系如图所示。下列说法正确的是
2Z(g) ∆H=-92.4kJ/mol,X的平衡转化率(α)与体系总压强(P)的关系如图所示。下列说法正确的是
| A.图中A,B两点,达到相同的平衡体系 |
| B.上述反应在达到平衡后,增大压强,Y的转化率提高 |
| C.升高温度,平衡向逆反应方向移动,说明逆反应速率增大,正反应速率减小 |
| D.将1.0molX、3.0molY,置于1L密闭容器中发生反应,放出的热量为92.4kJ |
您最近一年使用:0次
2021-11-02更新
|
567次组卷
|
3卷引用:广东省广州市海珠外国语实验中学2022-2023学年高二上学期期末测试化学试题
名校
5 . 对于反应2SO2(g)+O2(g) 2SO3(g),下列说法正确的是
2SO3(g),下列说法正确的是
 2SO3(g),下列说法正确的是
2SO3(g),下列说法正确的是| A.反应的ΔS>0 |
B.反应的平衡常数可表示为K= |
| C.增大体系的压强能提高SO2的反应速率和转化率 |
| D.使用催化剂能改变反应路径,提高反应的活化能 |
您最近一年使用:0次
2021-10-18更新
|
598次组卷
|
7卷引用:专题06 化学反应的方向及调控【考点清单】(讲+练)-2023-2024学年高二化学期中考点大串讲(人教版2019选择性必修1)
(已下线)专题06 化学反应的方向及调控【考点清单】(讲+练)-2023-2024学年高二化学期中考点大串讲(人教版2019选择性必修1)广西百色市德保高中2023-2024学年高二上学期11月期中考试化学试题江苏省徐州市第三中学2021-2022学年高二上学期10月月考化学试题湖南省衡阳市田家炳实验中学2021-2022学年高二上学期期中考试化学试题湖北省新高考联考协作体2021-2022学年高二3月考试化学试题黑龙江省佳木斯市实验中学2021-2022学年高二上学期期末考试化学试题江苏省南通市通州区金沙中学2021-2022学年高二上学期第二次调研考试化学试题
名校
6 . 下列因素中一定能引起平衡移动的是
| A.催化剂 | B.温度 | C.浓度 | D.压强 |
您最近一年使用:0次
2021-01-05更新
|
294次组卷
|
5卷引用:2019年高考海南卷化学试题变式题(单选题)
名校
解题方法
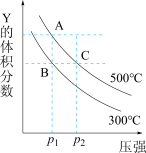
7 . 反应mX(g) nY(g)+pZ(g) ΔH,在不同温度下的平衡体系中物质Y的体积分数随压强变化的曲线如图所示。下列说法错误的是
nY(g)+pZ(g) ΔH,在不同温度下的平衡体系中物质Y的体积分数随压强变化的曲线如图所示。下列说法错误的是
 nY(g)+pZ(g) ΔH,在不同温度下的平衡体系中物质Y的体积分数随压强变化的曲线如图所示。下列说法错误的是
nY(g)+pZ(g) ΔH,在不同温度下的平衡体系中物质Y的体积分数随压强变化的曲线如图所示。下列说法错误的是
| A.该反应的ΔH>0 | B.m<n+p |
| C.B、C两点化学平衡常数:KB>KC | D.A、C两点的反应速率v(A)<v(C) |
您最近一年使用:0次
2022-09-15更新
|
2041次组卷
|
47卷引用:辽宁省部分重点中学2022-2023学年高二上学期期末联考化学试题
辽宁省部分重点中学2022-2023学年高二上学期期末联考化学试题山东省泰安市宁阳县复圣中学2022-2023学年高二上学期期末考试化学试题湖南省攸县第一中学2022-2023学年高二上学期期末考试化学试题辽宁省丹东市第二中学 大石桥市第三高级中学2022-2023学年高二上学期期末联考化学试题四川省宜宾市第四中学校2023-2024学年高二上学期9月月考化学试题四川省广安市岳池县第一中学2023-2024学年高二上学期第一次月考化学试题重庆市荣昌中学校2023-2024学年高二上学期期中考试化学试题四川省内江市威远中学校2023-2024学年高二上学期期中考试化学试题新疆石河子第一中学2023-2024学年高二上学期11月月考化学试题新疆生产建设兵团第二师八一中学2023-2024学年高二上学期期中考试化学(理科)试题四川省内江市威远中学校2023-2024学年高二上学期第二次月考(期中)化学试卷陕西省咸阳市实验中学2023-2024学年高二上学期段性检测(三)化学试题 贵州省遵义市仁怀市第六中学2023-2024学年高二上学期期中考试化学试题河南省驻马店市环际大联考2023-2024学年高二上学期11月期中考试化学试题福建省泉州市泉州中远学校2023-2024学年高二上学期11月期中化学试题2015-2016学年浙江台州中学高二上第三次统练化学试卷内蒙古自治区北京八中乌兰察布分校2018-2019学年高二下学期第一次月考化学试题湖北省随州二中2019-2020学年高二上学期9月份月考化学试题河南省新野县第一高级中学2019-2020学年高二上学期第二次月考化学试题甘肃省镇原县镇原中学2019-2020学年高二上学期期中考试化学(理)试题甘肃省镇原县镇原中学2019-2020学年高一上学期期中考试化学(理)试题广东省广州市2019-2020学年高二上学期期中模拟测试化学试题(二)2020年北京高二下学期 复习模拟试题二(选修4人教版)安徽省蚌埠田家炳中学2020-2021学年高二12月月考化学试题(已下线)练习7 化学平衡(二)-2020-2021学年【补习教材·寒假作业】高二化学(人教版)重庆市暨华中学校2021-2022学年高二上学期第一次月考化学试题四川省广安市武胜烈面中学校2021-2022学年高二10月月考化学试题天津市武清区崔黄口中学2021-2022学年高二上学期第一次练习化学试题重庆市永川景圣中学校2021-2022学年高二上学期第一次月考化学试题河南省平顶山九校联盟2021-2022学年高二上学期期中考试化学试题四川省广安市2021-2022学年高二上学期期末考试化学试题河南省宋基信阳实验中学2021-2022学年高三上学期12月月考化学试题吉林省长春市第六中学2021-2022学年高二上学期第三学程考试(理)化学试题陕西省西安市西航一中2021-2022学年高二上学期期中考试化学试题黑龙江省伊春市伊美区第二中学2021-2022学年高二上学期期中考试化学试题天津市武清区四校2022-2023学年高二上学期第一次阶段性练习化学试题上海市奉贤中学2022-2023学年高二上学期10月阶段测试化学试题贵州省黔西南州金成实验学校2022-2023学年高二上学期9月月考化学试题重庆市江津中学2022-2023学年高二上学期10月阶段性考试化学试题山东省滕州市第一中学2022-2023学年高二上学期11月月考化学试题湖南省长沙市长郡中学2022--2023学年高二上学期第二次线上月考化学试题湖南省长沙市长郡中学2022--2023学年高二上学期第二次线上月考化学试题新疆昌吉州行知学校2022-2023学年高二上学期第一次线上月考化学试题四川省广安市育才学校2022-2023学年高二上学期11月期中考试化学试题 重庆市育才中学校2022-2023学年高二上学期期中考试化学试题陕西省宝鸡市渭滨区2023-2024学年高二上学期期末考试化学试题河南省焦作市博爱县第一中学2023-2024学年高三上学期1月期末化学试题
名校
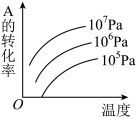
8 . 有一化学平衡:mA(g)+nB(g) pC(g)+qD(g)(如图)表示的是转化率与压强、温度的关系。分析图中曲线可以得出的结论是
pC(g)+qD(g)(如图)表示的是转化率与压强、温度的关系。分析图中曲线可以得出的结论是
 pC(g)+qD(g)(如图)表示的是转化率与压强、温度的关系。分析图中曲线可以得出的结论是
pC(g)+qD(g)(如图)表示的是转化率与压强、温度的关系。分析图中曲线可以得出的结论是
| A.正反应吸热 | B.m+n>p+q |
| C.正反应放热 | D.m+n<p+q |
您最近一年使用:0次
2020-12-14更新
|
685次组卷
|
3卷引用:河北省魏县第五中学2022-2023学年高二上学期1月期末考试化学试题
名校
9 . 下列叙述中不能用勒夏特列原理来解释的事实是
| A.N2(g)+3H2(g) ⇌ 2NH3(g),高压有利于合成氨 |
| B.实验室制取氯气时用排饱和食盐水除去氯气中的氯化氢气体 |
| C.2SO2(g)+O2(g) ⇌ 2SO3(g),加催化剂可以提高生产效率 |
| D.2NO2(g)⇌N2O4(g)ΔH<0,升高温度颜色加深 |
您最近一年使用:0次
名校
10 . 对于可逆反应:aA(气)+bB(气) mC(气)+nD(气)ΔH<0,下列说法正确的是
mC(气)+nD(气)ΔH<0,下列说法正确的是
 mC(气)+nD(气)ΔH<0,下列说法正确的是
mC(气)+nD(气)ΔH<0,下列说法正确的是| A.平衡移动,反应的平衡常数必改变 |
| B.增大压强平衡必移动 |
| C.升高温度平衡必移动 |
| D.加入催化剂平衡必移动 |
您最近一年使用:0次
2020-12-01更新
|
328次组卷
|
5卷引用:陕西省渭南市韩城市2023-2024学年高二上学期期中质量检测化学试题



