名校
1 . 一定温度下,某反应达平衡,平衡常数K=c(CH3OH)·c(H2O)/[c(CO2)·c3(H2)]。保持容器容积不变,升高温度,H2浓度减小,则下列说法不正确的是
| A.该反应化学方程式为CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) |
| B.恒温恒容下,再充入CO2气体,H2浓度一定减小 |
| C.恒温恒压下,再充入惰性气体,会降低反应物的转化率 |
| D.升高温度,会使正反应速率增大,平衡常数减小 |
您最近一年使用:0次
2022-11-13更新
|
85次组卷
|
3卷引用:广东省肇庆市第一中学2022-2023学年高二上学期期中考试化学试题
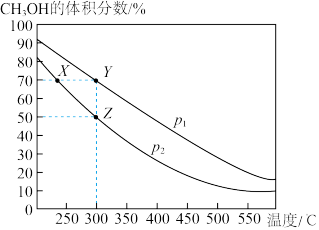
2 . CH3OH是重要的化工原料,工业上用CO与H2在催化剂作用下合成CH3OH,其反应为CO(g)+2H2(g)  CH3OH(g)。按n(CO)∶n(H2)=1∶2向密闭容器中充入反应物,测得平衡时混合物中CH3OH的体积分数在不同压强下随温度的变化如图所示。下列说法中,正确的是
CH3OH(g)。按n(CO)∶n(H2)=1∶2向密闭容器中充入反应物,测得平衡时混合物中CH3OH的体积分数在不同压强下随温度的变化如图所示。下列说法中,正确的是
 CH3OH(g)。按n(CO)∶n(H2)=1∶2向密闭容器中充入反应物,测得平衡时混合物中CH3OH的体积分数在不同压强下随温度的变化如图所示。下列说法中,正确的是
CH3OH(g)。按n(CO)∶n(H2)=1∶2向密闭容器中充入反应物,测得平衡时混合物中CH3OH的体积分数在不同压强下随温度的变化如图所示。下列说法中,正确的是
| A.p1<p2 | B.该反应的ΔH>0 |
| C.平衡常数:K(X)=K(Y) | D.在Z点时,CO转化率为75% |
您最近一年使用:0次
2022-04-11更新
|
346次组卷
|
23卷引用:广东省肇庆市第一中学2022-2023学年高二上学期期中考试化学试题
广东省肇庆市第一中学2022-2023学年高二上学期期中考试化学试题北京师大附中2017-2018学年上学期高二年级期中考试化学试卷云南省民族大学附属中学2019届高三上学期期中考试化学试题河南省实验中学2020-2021学年高二上学期期中考试化学试题江西省景德镇一中2020-2021学年高二上学期期中考试化学(2班)试题江西省南昌市第三中学2020~2021学年高二上学期期中考试化学试题北京市第四十四中学2021-2022学年高二上学期期中考试化学试题湖南省隆回县第二中学2022-2023学年高二上学期线上课程摸底(期中)考试化学试题山西省阳泉市第一中学校2022-2023学年高二上学期11月期中考试化学试题内蒙古北方重工业集团有限公司第三中学2019-2020学年高二10月月考化学试题湖北省武汉市汉阳一中2019-2020学年高二9月月考化学试题人教版选修四2019-2020学年高二上学期期末复习化学综合训练福建省漳州市龙海市第二中学2020届高三上学期第二次月考化学试题甘肃省张掖市第二中学2020届高三上学期11月月考化学试题江西省赣州市会昌中学2019-2020学年高二上学期第二次月考化学试题河北省衡水中学2020届高三上学期第四次调研考试化学试题【省级联考】浙江省2019—2020学年普通高校招生选考科目化学模拟试题(已下线)《2020年新高考政策解读与配套资源》模拟试题11-2020年北京新高考化学模拟试题福建省龙海第二中学2021届高三上学期第三次月考试题(1月)化学试题北京市通州区2021届高三一模化学试题四川省成都市蒲江县蒲江中学2019-2020学年高二上学期12月月考化学试题山西省运城市芮城中学2021-2022学年高二上学期12月月考化学试题广东省汕头市金山中学2021-2022学年高二上学期期末考试化学试题
名校
解题方法
3 . 一定温度下,将 和
和 充入
充入 密闭容器中发生反应:
密闭容器中发生反应: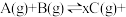
 ,在
,在 时达到平衡。在
时达到平衡。在 、
、 时分别改变反应的一个条件,测得容器中
时分别改变反应的一个条件,测得容器中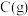 的浓度随时间变化情况如图所示。
的浓度随时间变化情况如图所示。
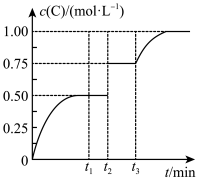
下列有关说法正确的是
 和
和 充入
充入 密闭容器中发生反应:
密闭容器中发生反应: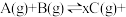
 ,在
,在 时达到平衡。在
时达到平衡。在 、
、 时分别改变反应的一个条件,测得容器中
时分别改变反应的一个条件,测得容器中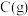 的浓度随时间变化情况如图所示。
的浓度随时间变化情况如图所示。
下列有关说法正确的是
A. |
B.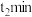 时改变的条件是使用催化剂 时改变的条件是使用催化剂 |
C. 时改变的条件是只增大生成物C的浓度 时改变的条件是只增大生成物C的浓度 |
D. 、 、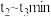 阶段反应的平衡常数均为4 阶段反应的平衡常数均为4 |
您最近一年使用:0次
2022-01-19更新
|
82次组卷
|
3卷引用:广东省肇庆市第一中学2022-2023学年高二上学期期中考试化学试题
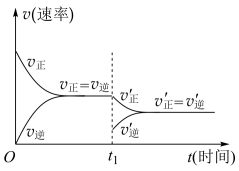
4 . 在N2(g)+3H2(g)  2NH3(g)(正反应为放热反应)的平衡体系中,在t1时刻只改变某一条件,其反应速率随时间变化的曲线如图,根据图象能得出的结论是
2NH3(g)(正反应为放热反应)的平衡体系中,在t1时刻只改变某一条件,其反应速率随时间变化的曲线如图,根据图象能得出的结论是
 2NH3(g)(正反应为放热反应)的平衡体系中,在t1时刻只改变某一条件,其反应速率随时间变化的曲线如图,根据图象能得出的结论是
2NH3(g)(正反应为放热反应)的平衡体系中,在t1时刻只改变某一条件,其反应速率随时间变化的曲线如图,根据图象能得出的结论是
| A.改变条件,平衡向逆反应方向移动 |
| B.t1时刻,改变的条件是减少了NH3的浓度 |
| C.t1时刻,改变的条件是增大了体系的压强 |
| D.达新平衡时,正反应速率增大,逆反应速率减小 |
您最近一年使用:0次
5 . 下列说法正确的是
| A.可逆反应具有的特征是正反应速率和逆反应速率相等 |
| B.在其他条件不变时,升高温度可使化学平衡向放热反应方向移动 |
| C.在其他条件不变时,增大压强一定会破坏有气体存在的反应的平衡状态 |
| D.在其他条件不变时,使用催化剂可以改变化学反应速率,但不能改变化学平衡状态 |
您最近一年使用:0次
名校
6 . 压强变化不会使下列化学反应的平衡发生移动的是( )
A.C(s)+CO2(g) 2CO(g) 2CO(g) | B.3H2(g)+N2(g) 2NH3(g) 2NH3(g) |
C.2SO2(g)+O2(g) 2SO3(g) 2SO3(g) | D.H2(g)+I2(g) 2HI(g) 2HI(g) |
您最近一年使用:0次
2019-09-28更新
|
286次组卷
|
15卷引用:广东省肇庆市实验中学2017-2018学年高二上学期期中考试化学(理)试题
广东省肇庆市实验中学2017-2018学年高二上学期期中考试化学(理)试题(已下线)2010年青海省青海师大附中高二上学期期中考试化学试卷浙江省诸暨市牌头中学2017-2018学年高一下学期期中考试(A)化学试题黑龙江省伊春市第二中学2018-2019学年高二(理)上学期期中考试化学试题广东省广州市2019-2020学年高二上学期期中模拟测试化学试题(一)陕西省咸阳百灵中学2020-2021学年高二上学期期中考试化学试题吉林省白城市第十四中学2021-2022学年高二上学期期中考试化学试卷题(已下线)2011-2012学年湖南省蓝山二中高二上学期期末考试化学试卷宁夏育才中学2017-2018学年高二9月月考化学试题云南省峨山彝族自治县第一中学2017-2018学年高二12月月考(理)化学试题天津市静海区四校2019-2020学年高二上学期9月联考化学试题山西省阳泉市2019-2020学年高二上学期期末考试化学试题海南省万宁市民族中学2019-2020学年度高二上学期期末考试化学试题2.3.1浓度 压强变化对化学平衡的影响 课前黑龙江省伊春市铁力市马永顺中学校2023-2024学年高二上学期期末考试化学试题
名校
7 . 可逆反应A(g)+2B(g) 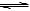 2C(g) ΔΗ<O在达到平衡时,要使C的浓度达到最大值,最适宜的条件是( )
2C(g) ΔΗ<O在达到平衡时,要使C的浓度达到最大值,最适宜的条件是( )
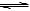 2C(g) ΔΗ<O在达到平衡时,要使C的浓度达到最大值,最适宜的条件是( )
2C(g) ΔΗ<O在达到平衡时,要使C的浓度达到最大值,最适宜的条件是( )| A.低温、高压 | B.高温、低压 |
| C.高温、高压 | D.使用合适的催化剂 |
您最近一年使用:0次
2017-12-08更新
|
125次组卷
|
4卷引用:广东省肇庆市实验中学2017-2018学年高二上学期期中考试化学(理)试题



