名校
解题方法
1 . 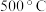 ,将
,将 和
和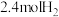 充入体积为
充入体积为 的已装有催化剂的恒容密闭容器中发生合成氨反应
的已装有催化剂的恒容密闭容器中发生合成氨反应 ,“此反应放热,下列说法正确的是
,“此反应放热,下列说法正确的是
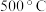 ,将
,将 和
和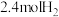 充入体积为
充入体积为 的已装有催化剂的恒容密闭容器中发生合成氨反应
的已装有催化剂的恒容密闭容器中发生合成氨反应 ,“此反应放热,下列说法正确的是
,“此反应放热,下列说法正确的是A.平衡时, 的浓度可能为 的浓度可能为 |
| B.容器内气体的密度不再随时间改变说明该反应已达到平衡状态 |
C.若已知生成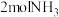 放出 放出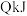 的热量,则该反应达平衡时放出的热量小于 的热量,则该反应达平衡时放出的热量小于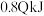 |
D.反应平衡后,向容器中充入一定体积的氨气,使容器中气体总压强增大,则 、 、 均增大 均增大 |
您最近半年使用:0次
名校
2 . 恒温下,反应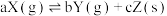 达到平衡状态,把容器容积缩小到原来的一半,且达到新的平衡状态时,X的物质的量浓度从0.1mol·L-1增大到0.19mol·L-1。下列判断中正确的是
达到平衡状态,把容器容积缩小到原来的一半,且达到新的平衡状态时,X的物质的量浓度从0.1mol·L-1增大到0.19mol·L-1。下列判断中正确的是
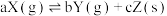 达到平衡状态,把容器容积缩小到原来的一半,且达到新的平衡状态时,X的物质的量浓度从0.1mol·L-1增大到0.19mol·L-1。下列判断中正确的是
达到平衡状态,把容器容积缩小到原来的一半,且达到新的平衡状态时,X的物质的量浓度从0.1mol·L-1增大到0.19mol·L-1。下列判断中正确的是| A.a>b | B.a<b+c | C.a=b+c | D.a<b |
您最近半年使用:0次
3 . I. 300℃时将2molA和2molB两种气体混合于2L密闭容器中,发生反应:3A(g)+B(g) 2C(g)+2D(g)
2C(g)+2D(g)  ,2min末达到平衡,生成0.8molD。
,2min末达到平衡,生成0.8molD。
(1)300℃时,该反应的平衡常数表达式为K=___________ ,已知K300℃<K350℃,则
___________ (填“>”或“<”0)。
(2)在2min末时,B的平衡浓度为___________ 。
(3)若温度不变,缩小容器容积,则A的转化率___________  填“增大”“减小”或“不变”
填“增大”“减小”或“不变” 。
。
Ⅱ.在一定条件下,可逆反应:mA+nB pC达到平衡,若:
pC达到平衡,若:
(4)A、B、C都是气体,减小压强,平衡向正反应方向移动,则,m+n___________ (填“>”“<”或“ ”p)。
”p)。
(5)A、C是气体,而且m+n=p,增大压强可使平衡发生移动,则平衡移动的方向是___________ 。(填“逆向移动”、“正向移动”或“不移动”)
(6)加热后,可使C的质量增加,则正反应是___________ (填“放热”或“吸热”)反应。
 2C(g)+2D(g)
2C(g)+2D(g)  ,2min末达到平衡,生成0.8molD。
,2min末达到平衡,生成0.8molD。(1)300℃时,该反应的平衡常数表达式为K=

(2)在2min末时,B的平衡浓度为
(3)若温度不变,缩小容器容积,则A的转化率
 填“增大”“减小”或“不变”
填“增大”“减小”或“不变” 。
。Ⅱ.在一定条件下,可逆反应:mA+nB
 pC达到平衡,若:
pC达到平衡,若:(4)A、B、C都是气体,减小压强,平衡向正反应方向移动,则,m+n
 ”p)。
”p)。(5)A、C是气体,而且m+n=p,增大压强可使平衡发生移动,则平衡移动的方向是
(6)加热后,可使C的质量增加,则正反应是
您最近半年使用:0次
4 . 探究CH3OH合成反应化学平衡的影响因素,有利于提高CH3OH的产率。以CO2、H2为原料合成CH3OH涉及的主要反应如下:
Ⅰ.CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH1=-49.5kJ·mol-1
Ⅱ.CO(g)+2H2(g)⇌CH3OH(g) ΔH2=-90.4kJ·mol-1
Ⅲ.CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH3=+40.9kJ·mol-1
(1)不同压强下,按照n(CO2)∶n(H2)=1∶3投料,实验测定CO2的平衡转化率和CH3OH的平衡产率随温度的变化关系如图所示。

其中纵坐标表示CO2平衡转化率的是图_____ (填“甲”或“乙”);压强p1、p2、p3由大到小的顺序为_____ ;图乙中T1温度时,三条曲线几乎交于一点的原因是_____ 。
(2)为同时提高CO2的平衡转化率和CH3OH的平衡产率,应选择的反应条件为_____(填标号)。
(3)反应ⅠCO2(g)+3H2(g)=CH3OH(g)+H2O(g)。最近采用真空封管法制备的磷化硼纳米颗粒,在发展非金属催化剂实现CO2电催化还原制备甲醇方向取得重要进展,该反应历程如图所示:
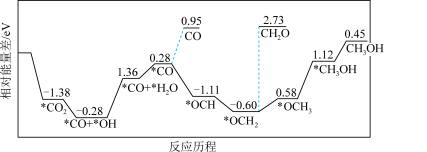
容易得到的副产物有CO和CH2O,其中相对较少的副产物为_____ ;上述合成甲醇的反应速率较慢,要使反应速率加快,主要降低下列变化中_____ (填字母)的能量变化。(双选)
A.*OCH3→*CH3OH B.*CO→*COH C.*OCH2→*OCH3 D.*CO+*OH→*CO+*H2O
Ⅰ.CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH1=-49.5kJ·mol-1
Ⅱ.CO(g)+2H2(g)⇌CH3OH(g) ΔH2=-90.4kJ·mol-1
Ⅲ.CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH3=+40.9kJ·mol-1
(1)不同压强下,按照n(CO2)∶n(H2)=1∶3投料,实验测定CO2的平衡转化率和CH3OH的平衡产率随温度的变化关系如图所示。

其中纵坐标表示CO2平衡转化率的是图
(2)为同时提高CO2的平衡转化率和CH3OH的平衡产率,应选择的反应条件为_____(填标号)。
| A.低温、高压 | B.高温、低压 | C.低温、低压 | D.高温、高压 |
(3)反应ⅠCO2(g)+3H2(g)=CH3OH(g)+H2O(g)。最近采用真空封管法制备的磷化硼纳米颗粒,在发展非金属催化剂实现CO2电催化还原制备甲醇方向取得重要进展,该反应历程如图所示:

容易得到的副产物有CO和CH2O,其中相对较少的副产物为
A.*OCH3→*CH3OH B.*CO→*COH C.*OCH2→*OCH3 D.*CO+*OH→*CO+*H2O
您最近半年使用:0次
解题方法
5 . 下列叙述与对应的图示相符合的是
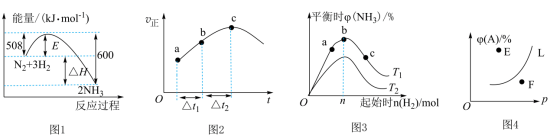

A.图1为 反应过程中的能量变化图,利用勒夏特列原理能解释工业上选择 反应过程中的能量变化图,利用勒夏特列原理能解释工业上选择 左右合成氨比室温更有利 左右合成氨比室温更有利 |
B.图2为在绝热恒容密闭容器中通入 和 和 ,反应 ,反应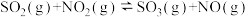 的 的 图,由图可知该反应为放热反应 图,由图可知该反应为放热反应 |
C.图3为合成氨反应中,保持其他条件不变,起始时 用量、反应温度对反应的影响图,则图中温度 用量、反应温度对反应的影响图,则图中温度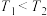 , , 、 、 、 、 三点均处于平衡状态,反应物 三点均处于平衡状态,反应物 的平衡转化率:a<b<c 的平衡转化率:a<b<c |
D.图4为反应 平衡时 平衡时 的体积分数与反应压强的关系图,则 的体积分数与反应压强的关系图,则 点: 点: |
您最近半年使用:0次
6 . N2(g)+3H2(g) 2NH3(g) △H<0,反应达平衡时,下列措施能提高N2转化率的是
2NH3(g) △H<0,反应达平衡时,下列措施能提高N2转化率的是
①降温 ②恒压通入惰性气体 ③增加N2的浓度 ④加压 ⑤催化剂
| A.①④ | B.①②③⑤ | C.②③⑤ | D.③④⑤ |
您最近半年使用:0次
7 . 下列能用勒夏特列原理解释的是
| A.及时分离出氨有利于提高氨的产量 |
| B.H2、I2、HI平衡时的混合气体加压后颜色变深 |
| C.SO2催化氧化成SO3的反应,往往需要使用催化剂 |
| D.红棕色的NO2加压后颜色先变深后变浅 |
您最近半年使用:0次
2024-03-21更新
|
22次组卷
|
2卷引用:海南省三亚市2023-2024学年鲁迅中学高二上学期化学期中测试
8 . t℃时,某一气态平衡体系中含有X、Y、Z、W四种气体物质,此温度下发生反应的平衡常数表达式为: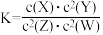 ,有关该平衡体系的说法正确的是
,有关该平衡体系的说法正确的是
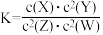 ,有关该平衡体系的说法正确的是
,有关该平衡体系的说法正确的是| A.升高温度,平衡常数K增大,则正反应为吸热反应 |
| B.增大压强,W质量分数增加 |
| C.增大X浓度,平衡向正反应方向移动 |
| D.升高温度,若混合气体的平均相对分子质量变大,则正反应是放热反应 |
您最近半年使用:0次
解题方法
9 . A:一定条件下,某可逆反应在密闭容器中建立化学平衡,在 时刻改变某一个条件,建立新的平衡,其
时刻改变某一个条件,建立新的平衡,其 图像如下:
图像如下:
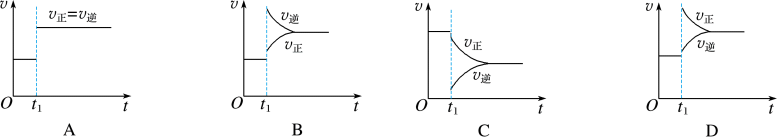
(1)对于反应: ,
, 时刻缩小容器体积,其图像为
时刻缩小容器体积,其图像为___________ (填字母,下同),平衡___________ (填“向正反应方向”“向逆反应方向”或“不”,下同)移动。
(2)对于反应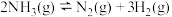 ,
, 时刻增大容器体积,其图像为
时刻增大容器体积,其图像为___________ ,平衡___________ 移动。
(3)对于反应 ,
, 时刻缩小容器体积,其图像为
时刻缩小容器体积,其图像为___________ ,平衡___________ 移动。
B:可逆反应 在不同温度(和)及压强(和)下,产生Z的物质的量n和反应时间t的关系如图所示,根据图像回答下列问题:
在不同温度(和)及压强(和)下,产生Z的物质的量n和反应时间t的关系如图所示,根据图像回答下列问题:
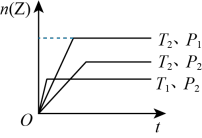
(4)温度 和
和 的关系为
的关系为
___________ (填“>”、“<”或“=”,下同) ,压强
,压强 和
和 的关系为
的关系为
___________  。
。
(5)a___________ 1。
(6)该反应的正反应为___________ (填“吸热”或“放热”反应)。
 时刻改变某一个条件,建立新的平衡,其
时刻改变某一个条件,建立新的平衡,其 图像如下:
图像如下:
(1)对于反应:
 ,
, 时刻缩小容器体积,其图像为
时刻缩小容器体积,其图像为(2)对于反应
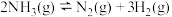 ,
, 时刻增大容器体积,其图像为
时刻增大容器体积,其图像为(3)对于反应
 ,
, 时刻缩小容器体积,其图像为
时刻缩小容器体积,其图像为B:可逆反应
 在不同温度(和)及压强(和)下,产生Z的物质的量n和反应时间t的关系如图所示,根据图像回答下列问题:
在不同温度(和)及压强(和)下,产生Z的物质的量n和反应时间t的关系如图所示,根据图像回答下列问题: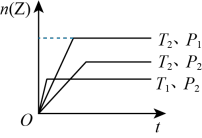
(4)温度
 和
和 的关系为
的关系为
 ,压强
,压强 和
和 的关系为
的关系为
 。
。(5)a
(6)该反应的正反应为
您最近半年使用:0次
解题方法
10 .  时,A、B、C三种气体在恒容密闭容器中反应时,浓度的变化情况如图,回答下列问题。
时,A、B、C三种气体在恒容密闭容器中反应时,浓度的变化情况如图,回答下列问题。
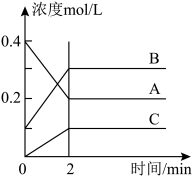
(1)写出该反应的方程式:___________ 。
(2)前 ,A的分解速率为
,A的分解速率为___________ 。
(3)达到平衡后,若增大压强,平衡向___________ 方向移动(填“正”或“逆”或“不移动)。
(4)该反应的平衡常数
___________ 。
(5) 反应达平衡,容器内混合气体的平均相对分子质量比起始时
反应达平衡,容器内混合气体的平均相对分子质量比起始时___________ (填“大”,“小”或“相等”,下同),混合气体密度比起始时___________
(6)在某一时刻采取下列措施能使该反应速率减小的是___________。
 时,A、B、C三种气体在恒容密闭容器中反应时,浓度的变化情况如图,回答下列问题。
时,A、B、C三种气体在恒容密闭容器中反应时,浓度的变化情况如图,回答下列问题。
(1)写出该反应的方程式:
(2)前
 ,A的分解速率为
,A的分解速率为(3)达到平衡后,若增大压强,平衡向
(4)该反应的平衡常数

(5)
 反应达平衡,容器内混合气体的平均相对分子质量比起始时
反应达平衡,容器内混合气体的平均相对分子质量比起始时(6)在某一时刻采取下列措施能使该反应速率减小的是___________。
| A.加催化剂 | B.降低温度 |
| C.容积不变,充入A | D.容积不变,从容器中分离出A |
您最近半年使用:0次



