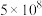1 . 下列实验方法或方案能达到目的的是
| 选项 | 目的 | 实验方法或方案 |
| A | 探究压强对化学平衡的影响 | 2HI |
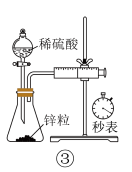
| B | 测定锌与稀硫酸反应的反应速率 |
|
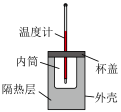
| C | 测定中和反应的反应热 |
|
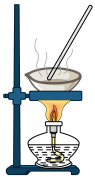
| D | 蒸发AlC13溶液得到AlCl3固体 |
|
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2 . 已知某反应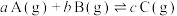 ,在其他条件不变的情况下,改变某一条件后的化学平衡图像如图(T表示温度,p表示压强且
,在其他条件不变的情况下,改变某一条件后的化学平衡图像如图(T表示温度,p表示压强且 ,
, 表示转化率)。下列说法正确的是
表示转化率)。下列说法正确的是
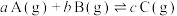 ,在其他条件不变的情况下,改变某一条件后的化学平衡图像如图(T表示温度,p表示压强且
,在其他条件不变的情况下,改变某一条件后的化学平衡图像如图(T表示温度,p表示压强且 ,
, 表示转化率)。下列说法正确的是
表示转化率)。下列说法正确的是
A. , , | B. , , |
C. , , | D. , , |
您最近半年使用:0次
3 . Ⅰ.氮的固定是几百年来科学家一直研究的课题。
(1)下表列举了不同温度下大气固氮和工业固氮的部分化学平衡常数K的值。.
①分析数据可知:大气固氮反应属于__________ (填“吸热”或“放热”)反应。
②分析数据可知:人类不适合大规模模拟大气固氮的原因:__________ 。
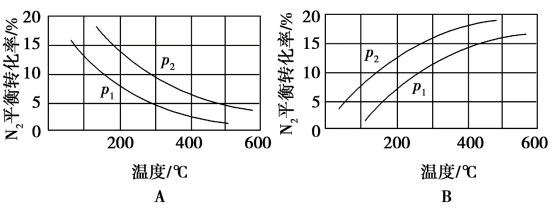
(2)工业固氮反应中,在其他条件相同时,分别测定 的平衡转化率在不同压强(
的平衡转化率在不同压强( 、
、 )下随温度变化的曲线,下图所示的图示中,正确的是
)下随温度变化的曲线,下图所示的图示中,正确的是______ (填“A”或“B”);比较 、
、 的大小关系:
的大小关系:__________ 。
Ⅱ.目前工业合成氨的原理是 。
。
(3)在一定温度下,将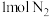 和
和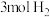 混合置于体积不变的密闭容器中发生反应。
混合置于体积不变的密闭容器中发生反应。
①下列描述能说明反应达到平衡状态的是__________ (填字母)。
A.单位时间内消耗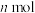 的
的 同时消耗
同时消耗 的
的
B. 、
、 、
、 的浓度相等
的浓度相等
C.混合气体的平均相对分子质量不变
D.混合气体的密度不变
②已知450℃时,某时刻测得 ,
, ,
, ,此时可逆反应
,此时可逆反应__________ 。
A.向正方向进行 B.向逆方向进行 C.处于平衡状态
(1)下表列举了不同温度下大气固氮和工业固氮的部分化学平衡常数K的值。.
| 反应 | 大气固氮 | 工业固氮 | |||
温度/℃ | 27 | 2000 | 25 | 400 | 450 |
平衡常数K |
| 0.1 |
| 0.507 | 0.152 |
②分析数据可知:人类不适合大规模模拟大气固氮的原因:
(2)工业固氮反应中,在其他条件相同时,分别测定
 的平衡转化率在不同压强(
的平衡转化率在不同压强( 、
、 )下随温度变化的曲线,下图所示的图示中,正确的是
)下随温度变化的曲线,下图所示的图示中,正确的是 、
、 的大小关系:
的大小关系:
Ⅱ.目前工业合成氨的原理是
 。
。(3)在一定温度下,将
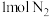 和
和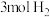 混合置于体积不变的密闭容器中发生反应。
混合置于体积不变的密闭容器中发生反应。①下列描述能说明反应达到平衡状态的是
A.单位时间内消耗
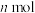 的
的 同时消耗
同时消耗 的
的
B.
 、
、 、
、 的浓度相等
的浓度相等C.混合气体的平均相对分子质量不变
D.混合气体的密度不变
②已知450℃时,某时刻测得
 ,
, ,
, ,此时可逆反应
,此时可逆反应A.向正方向进行 B.向逆方向进行 C.处于平衡状态
您最近半年使用:0次
4 . 反应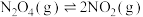
 ,在温度为
,在温度为 、
、 时,平衡体系中
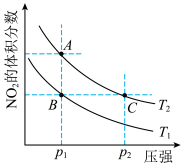
时,平衡体系中 的体积分数随压强的变化曲线如图所示。下列说法正确的是。
的体积分数随压强的变化曲线如图所示。下列说法正确的是。
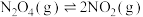
 ,在温度为
,在温度为 、
、 时,平衡体系中
时,平衡体系中 的体积分数随压强的变化曲线如图所示。下列说法正确的是。
的体积分数随压强的变化曲线如图所示。下列说法正确的是。
| A.A、C两点的反应速率:A>C |
| B.A、C两点气体的颜色:A深,C浅 |
| C.A、C两点气体的平均相对分子质量:A>C |
| D.由状态B到状态A,可以用加热的方法 |
您最近半年使用:0次
5 . 对于任何一个化学平衡体系,采取以下措施,一定会使平衡发生移动的是
| A.加入一种反应物 | B.加入催化剂 |
| C.增大体系压强 | D.升高温度 |
您最近半年使用:0次
6 . 下列反应达到平衡后,升高温度和增大压强,平衡移动方向一致的是
A.C(s) + CO2(g) 2CO(g)△H>0 2CO(g)△H>0 |
B.Cl2(g) +H2O(l) HCl(aq)+HClO(aq)△H>0 HCl(aq)+HClO(aq)△H>0 |
C.H2(g) +I2(g) 2HI(g)△H<0 2HI(g)△H<0 |
D.O2(g) +2SO2(g) 2SO3(g)△H<0 2SO3(g)△H<0 |
您最近半年使用:0次
7 . 关于反应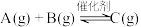
 ,下列说法正确的是
,下列说法正确的是
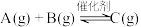
 ,下列说法正确的是
,下列说法正确的是| A.一定是自发反应 |
| B.温度升高,逆反应速率减慢 |
| C.反应物浓度增大,平衡向正反应方向进行 |
| D.催化剂不参与化学反应 |
您最近半年使用:0次
8 . 密闭容器中进行的可逆反应:

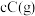 在不同温度(
在不同温度( 和
和 )及压强(
)及压强( 和
和 )下,混合气体中B的质量分数W(B)与反应时间(t)的关系如图所示。下列判断正确的是
)下,混合气体中B的质量分数W(B)与反应时间(t)的关系如图所示。下列判断正确的是



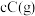 在不同温度(
在不同温度( 和
和 )及压强(
)及压强( 和
和 )下,混合气体中B的质量分数W(B)与反应时间(t)的关系如图所示。下列判断正确的是
)下,混合气体中B的质量分数W(B)与反应时间(t)的关系如图所示。下列判断正确的是
A. , ,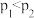 , ,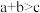 ,正反应为吸热反应 ,正反应为吸热反应 |
B. ,P1< P2, ,P1< P2,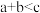 ,正反应为放热反应 ,正反应为放热反应 |
C. , ,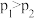 , ,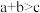 ,正反应为放热反应 ,正反应为放热反应 |
D. , ,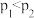 , ,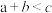 ,正反应为吸热反应 ,正反应为吸热反应 |
您最近半年使用:0次
名校
解题方法
9 . 在恒温条件,体积为 的密闭容器中,充入一定量混合气体发生反应:
的密闭容器中,充入一定量混合气体发生反应: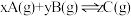 ,达到平衡时,测得A的浓度为
,达到平衡时,测得A的浓度为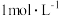 ;将容器的体积扩大到
;将容器的体积扩大到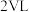 ,再次达到平衡时,测得A的浓度为
,再次达到平衡时,测得A的浓度为 ,下列有关判断正确的是
,下列有关判断正确的是
 的密闭容器中,充入一定量混合气体发生反应:
的密闭容器中,充入一定量混合气体发生反应: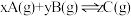 ,达到平衡时,测得A的浓度为
,达到平衡时,测得A的浓度为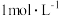 ;将容器的体积扩大到
;将容器的体积扩大到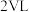 ,再次达到平衡时,测得A的浓度为
,再次达到平衡时,测得A的浓度为 ,下列有关判断正确的是
,下列有关判断正确的是A.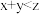 |
| B.平衡向正反应方向移动 |
| C.B的浓度比第1次平衡时大 |
| D.C的体积分数比第1次平衡时低 |
您最近半年使用:0次
10 . 回答下列问题。
(1)在密闭容器中的可逆反应CO(g)+NO2(g) CO2(g)+NO(g)
CO2(g)+NO(g)  <0。达到平衡后:扩大容器体积,平衡
<0。达到平衡后:扩大容器体积,平衡___________ 移动(填“正向”、“逆向”、“不”),c(NO2)将___________ (填“增大”、“减小”、“不变”),反应混合物的颜色将变___________ (填“深”、“浅”、“不变”)。升高温度平衡___________ 移动(填“正向”、“逆向”、“不”),加入催化剂,NO的物质的量___________ (填“增大”、“减小”、“不变”)。
(2)如图所示,在烧杯A、B中均盛有20 ℃的50 mL水,C与D相通,其中充有红棕色气体,存在平衡:2NO2 N2O4(正反应放热)。
N2O4(正反应放热)。

若向A中加入10 g NaOH固体使其溶解,向B中加入50 g硝酸铵固体也使其溶解,则:A、B两烧杯中,A烧杯中溶液温度___________ ,B烧杯中溶液温度___________ 。(填“升高”“降低”或“不变”) ;B、C中气体颜色___________ ,D中气体颜色___________ 。(填“变深”“变浅”或“不变”);在测定NO2的相对分子质量时,较为适宜的条件是___________ (填“较高温度”或“较低温度”)。
(1)在密闭容器中的可逆反应CO(g)+NO2(g)
 CO2(g)+NO(g)
CO2(g)+NO(g)  <0。达到平衡后:扩大容器体积,平衡
<0。达到平衡后:扩大容器体积,平衡(2)如图所示,在烧杯A、B中均盛有20 ℃的50 mL水,C与D相通,其中充有红棕色气体,存在平衡:2NO2
 N2O4(正反应放热)。
N2O4(正反应放热)。
若向A中加入10 g NaOH固体使其溶解,向B中加入50 g硝酸铵固体也使其溶解,则:A、B两烧杯中,A烧杯中溶液温度
您最近半年使用:0次