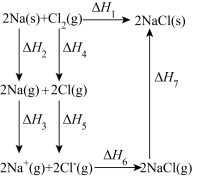
关于反应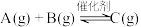
 ,下列说法正确的是
,下列说法正确的是
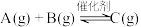
 ,下列说法正确的是
,下列说法正确的是| A.一定是自发反应 |
| B.温度升高,逆反应速率减慢 |
| C.反应物浓度增大,平衡向正反应方向进行 |
| D.催化剂不参与化学反应 |
更新时间:2024-03-24 14:09:29
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】工业制硫酸的关键反应为 。T℃时,向
。T℃时,向 恒容密闭容器中按照物质的量之比
恒容密闭容器中按照物质的量之比 通入
通入 和
和 ,测得容器内某些物质的量随时间变化如图。下列说法正确的是
,测得容器内某些物质的量随时间变化如图。下列说法正确的是
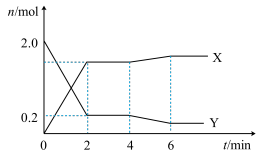
 。T℃时,向
。T℃时,向 恒容密闭容器中按照物质的量之比
恒容密闭容器中按照物质的量之比 通入
通入 和
和 ,测得容器内某些物质的量随时间变化如图。下列说法正确的是
,测得容器内某些物质的量随时间变化如图。下列说法正确的是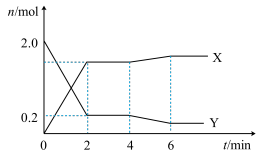
A.用 表示 表示 内的平均反应速率为 内的平均反应速率为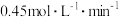 |
B.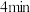 时改变的条件可能是降温或增加 时改变的条件可能是降温或增加 的量 的量 |
| C.T℃,正反应的化学平衡常数K为810 |
D. 时,若再加入 时,若再加入 和 和 各 各 ,平衡逆向移动 ,平衡逆向移动 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法不正确的是
| A.NH3的熔、沸点比ⅤA族其他元素氢化物的都高 |
| B.向碘的四氯化碳溶液中加入浓的KI溶液,溶液紫色会变浅 |
| C.尿素(CO(NH2)2)的熔、沸点比醋酸的高 |
| D.含1 mol[Ti(NH3)5Cl]Cl2的水溶液中加入足量AgNO3溶液,产生2 mol白色沉淀 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】烧水壶沸腾时,开水滴到灼热的煤球上会发反应: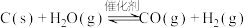
 。现将炭粉和
。现将炭粉和 在恒温恒容的密闭容器中,反应达到平衡时,下列叙述正确的是
在恒温恒容的密闭容器中,反应达到平衡时,下列叙述正确的是
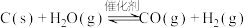
 。现将炭粉和
。现将炭粉和 在恒温恒容的密闭容器中,反应达到平衡时,下列叙述正确的是
在恒温恒容的密闭容器中,反应达到平衡时,下列叙述正确的是A.充入一定量的氖气, 减少 减少 |
B.更换高效催化剂,平衡时, 的产率增大 的产率增大 |
C.再加入一定量的炭粉, 的体积分数增大 的体积分数增大 |
D.再充入一定量的 , , 转化率减小 转化率减小 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列事实不能用勒夏特列原理解释的是
A.氯水中存在的平衡:Cl2+H2O H++Cl-+HClO,当加入适当的NaHCO3(s)后,溶液颜色变浅 H++Cl-+HClO,当加入适当的NaHCO3(s)后,溶液颜色变浅 |
B.在K2Cr2O7溶液中存在如下平衡, +H2O +H2O 2 2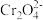 +2H+,若向K2Cr2O7溶液中滴入5~15滴浓硫酸,溶液颜色橙色加深 +2H+,若向K2Cr2O7溶液中滴入5~15滴浓硫酸,溶液颜色橙色加深 |
C.对于反应体系CO(g)+NO2(g)  NO(g)+CO2(g),给平衡体系增大压强可使颜色变深 NO(g)+CO2(g),给平衡体系增大压强可使颜色变深 |
D.对于反应2NO2(g)  N2O4(g) ΔH<0,平衡体系升高温度颜色变深 N2O4(g) ΔH<0,平衡体系升高温度颜色变深 |
您最近半年使用:0次
【推荐1】下列关于反应方向、速率和平衡的说法正确的是
| A.一般来说,温度升高,反应速率加快;活化能大的反应,升高温度后比活化能小的反应速率增大的幅度更大 |
| B.一般来说,放热越多的反应,反应速率也越快 |
| C.对于存在竞争的主反应和副反应,主副产物的占比只与反应的时间有关 |
| D.氢气和氧气在常温下混合后没有明显反应现象,需要点燃才能够反应,故该反应在常温下不自发 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】相同的温度和压强条件下,有关下列两个自发反应的说法不正确的是
注:其中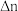 表示反应方程式中气体系数差;
表示反应方程式中气体系数差;
| 反应 | 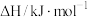 | 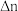 |  |
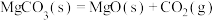 | 117.6 | 1 | a |
 | 177.9 | 1 | b |
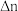 表示反应方程式中气体系数差;
表示反应方程式中气体系数差;A.因为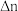 相同,所以a与b大小相近 相同,所以a与b大小相近 |
B.热分解温度: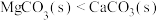 |
C. |
D.两个反应的 和 和 都大于零 都大于零 |
您最近半年使用:0次

 zC(g)达平衡时,A的浓度为0.5mol/L。若保持温度不变,将容器的容积扩大到原来的2倍,达新平衡时A的浓度为0.2mol/L。下列判断正确的是
zC(g)达平衡时,A的浓度为0.5mol/L。若保持温度不变,将容器的容积扩大到原来的2倍,达新平衡时A的浓度为0.2mol/L。下列判断正确的是