解题方法
1 .  时,A、B、C三种气体在恒容密闭容器中反应时,浓度的变化情况如图,回答下列问题。
时,A、B、C三种气体在恒容密闭容器中反应时,浓度的变化情况如图,回答下列问题。
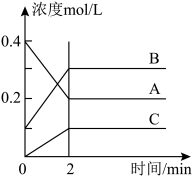
(1)写出该反应的方程式:___________ 。
(2)前 ,A的分解速率为
,A的分解速率为___________ 。
(3)达到平衡后,若增大压强,平衡向___________ 方向移动(填“正”或“逆”或“不移动)。
(4)该反应的平衡常数
___________ 。
(5) 反应达平衡,容器内混合气体的平均相对分子质量比起始时
反应达平衡,容器内混合气体的平均相对分子质量比起始时___________ (填“大”,“小”或“相等”,下同),混合气体密度比起始时___________
(6)在某一时刻采取下列措施能使该反应速率减小的是___________。
 时,A、B、C三种气体在恒容密闭容器中反应时,浓度的变化情况如图,回答下列问题。
时,A、B、C三种气体在恒容密闭容器中反应时,浓度的变化情况如图,回答下列问题。
(1)写出该反应的方程式:
(2)前
 ,A的分解速率为
,A的分解速率为(3)达到平衡后,若增大压强,平衡向
(4)该反应的平衡常数

(5)
 反应达平衡,容器内混合气体的平均相对分子质量比起始时
反应达平衡,容器内混合气体的平均相对分子质量比起始时(6)在某一时刻采取下列措施能使该反应速率减小的是___________。
| A.加催化剂 | B.降低温度 |
| C.容积不变,充入A | D.容积不变,从容器中分离出A |
您最近一年使用:0次
23-24高二上·全国·课时练习
2 . 对于反应H2(g)+I2(g) 2HI(g),增大压强,平衡是否发生移动
2HI(g),增大压强,平衡是否发生移动________ ?为什么________ ?
 2HI(g),增大压强,平衡是否发生移动
2HI(g),增大压强,平衡是否发生移动
您最近一年使用:0次
3 . 一定条件下,某可逆反应在密闭容器中建立化学平衡,在 时刻改变某一个条件,建立新的平衡,其
时刻改变某一个条件,建立新的平衡,其 图像如下:
图像如下:
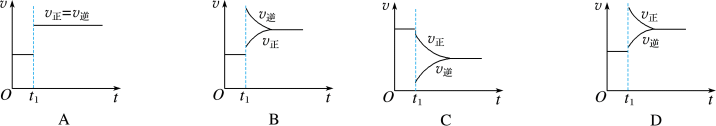
(1)对于反应 ,
, 时刻缩小容器体积,其图像为
时刻缩小容器体积,其图像为___________ (填字母),平衡___________ (填“向正反应方向”、“向逆反应方向”或“不”)移动。
(2)对于反应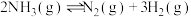 ,
, 时刻增大容器体积,其图像为
时刻增大容器体积,其图像为___________ (填字母),平衡___________ (填“向正反应方向”、“向逆反应方向”或“不”)移动。
(3)对于反应 ,
, 时刻缩小容器体积,其图像为
时刻缩小容器体积,其图像为___________ (填字母),平衡___________ (填“向正反应方向”、“向逆反应方向”或“不”)移动。
 时刻改变某一个条件,建立新的平衡,其
时刻改变某一个条件,建立新的平衡,其 图像如下:
图像如下:
(1)对于反应
 ,
, 时刻缩小容器体积,其图像为
时刻缩小容器体积,其图像为(2)对于反应
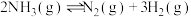 ,
, 时刻增大容器体积,其图像为
时刻增大容器体积,其图像为(3)对于反应
 ,
, 时刻缩小容器体积,其图像为
时刻缩小容器体积,其图像为
您最近一年使用:0次
2023-08-30更新
|
652次组卷
|
2卷引用:第二章 化学反应速率与化学平衡 第二节 化学平衡 第3课时 影响化学平衡的因素
解题方法
4 . 在一定条件下,可逆反应:mA+nB pC达到平衡,若:
pC达到平衡,若:
(1)A、B、C都是气体,减小压强,平衡向正反应方向移动,则m+n和p的关系是___________ 。
(2)A、C是气体,增加B的量,平衡不移动,则B为___________ 态。
(3)A、C是气体,而且m+n=p,增大压强可使平衡发生移动,则平衡移动的方向是___________ 。
 pC达到平衡,若:
pC达到平衡,若:(1)A、B、C都是气体,减小压强,平衡向正反应方向移动,则m+n和p的关系是
(2)A、C是气体,增加B的量,平衡不移动,则B为
(3)A、C是气体,而且m+n=p,增大压强可使平衡发生移动,则平衡移动的方向是
您最近一年使用:0次
解题方法
5 . 压强变化对化学平衡的影响规律
增大压强,平衡向___________ 的方向移动;
减小压强,平衡向___________ 的方向移动。
对于反应前后气体分子数目不变的反应,增大压强时,改变反应体系的压强,平衡___________ 移动。
增大压强,平衡向
减小压强,平衡向
对于反应前后气体分子数目不变的反应,增大压强时,改变反应体系的压强,平衡
您最近一年使用:0次
2023-07-15更新
|
125次组卷
|
2卷引用:2.3.1浓度 压强变化对化学平衡的影响 课前
6 . 对于只有固体或液体参加的反应,体系压强的改变能使化学平衡状态发生变化吗_______ ?
您最近一年使用:0次
7 . 一定条件下,某可逆反应在密闭容器中建立化学平衡,在t1时刻改变某一个条件,建立新的平衡,其v-t图像如下:

(1)对于反应:2SO2(g)+O2(g) 2SO3(g),t1时刻缩小容器体积,其图像为
2SO3(g),t1时刻缩小容器体积,其图像为________ (填字母,下同),平衡_________ (填“向正反应方向”“向逆反应方向”或“不”,下同)移动。
(2)对于反应2NH3(g) N2(g)+3H2(g),t1时刻增大容器体积,其图像为
N2(g)+3H2(g),t1时刻增大容器体积,其图像为________ ,平衡__________________ 移动。
(3)对于反应H2(g)+I2(g) 2HI(g),t1时刻缩小容器体积,其图像为
2HI(g),t1时刻缩小容器体积,其图像为________ ,平衡________ 移动。

(1)对于反应:2SO2(g)+O2(g)
 2SO3(g),t1时刻缩小容器体积,其图像为
2SO3(g),t1时刻缩小容器体积,其图像为(2)对于反应2NH3(g)
 N2(g)+3H2(g),t1时刻增大容器体积,其图像为
N2(g)+3H2(g),t1时刻增大容器体积,其图像为(3)对于反应H2(g)+I2(g)
 2HI(g),t1时刻缩小容器体积,其图像为
2HI(g),t1时刻缩小容器体积,其图像为
您最近一年使用:0次
2022-09-27更新
|
986次组卷
|
4卷引用:第3课时 压强对化学平衡的影响 勒·夏特列原理
21-22高二·全国·课前预习
8 . 在其他条件不变的情况下,压强对化学平衡的影响规律
Δvg=(化学方程式中气态反应产物化学式前系数之和)-(化学方程式中气态反应物化学式前系数之和)。
(1)Δvg=0:改变压强,化学平衡___________ ;
(2)Δvg≠0:改变压强,化学平衡向___________ 方向移动。
Δvg=(化学方程式中气态反应产物化学式前系数之和)-(化学方程式中气态反应物化学式前系数之和)。
(1)Δvg=0:改变压强,化学平衡
(2)Δvg≠0:改变压强,化学平衡向
您最近一年使用:0次



