1 . 用α粒子撞击铋-209合成了砹-211。所得样品中砹-211的浓度<10-8mol/L,砹-211同位素半衰期较长,足以用它来研究砹的化学性质。
(1)写出合成砹的核反应方程式_______ 。
(2)已知室温下用CCl4萃取I2分配系数为 (CCl4)/
(CCl4)/ (H2O)=84,预计用CCl4萃取。AtI的分配系数
(H2O)=84,预计用CCl4萃取。AtI的分配系数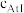 (CCl4)/
(CCl4)/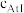 (H2O)
(H2O)_______ 84(填>,<或=);理由是_______ 。
(3)已知I2+I-⇌I 的平衡常数K=800,可推断AtI+I-⇌AtI
的平衡常数K=800,可推断AtI+I-⇌AtI 的平衡常数K
的平衡常数K_______ 800填>,<或=);依据是_______ 。
(4)在AtI中加入I2和I-的混合溶液,滴加AgNO3溶液,发现所得沉淀中只有AgI而没有共沉淀的AgAt(如果有AgAt,必然会被共沉淀),然而在上述产物中加入Pb(IO3)2却发现有砹的共沉淀。写出有关化学方程式_______ ,解释上述实验现象_______ 。
(5)已知室温下ICH2COOH的pKa=3.12,由此可推断AtCH2COOH的pKa_______ 3.12(填>,<或=);理由是:_______ 。
(1)写出合成砹的核反应方程式
(2)已知室温下用CCl4萃取I2分配系数为
 (CCl4)/
(CCl4)/ (H2O)=84,预计用CCl4萃取。AtI的分配系数
(H2O)=84,预计用CCl4萃取。AtI的分配系数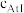 (CCl4)/
(CCl4)/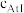 (H2O)
(H2O)(3)已知I2+I-⇌I
 的平衡常数K=800,可推断AtI+I-⇌AtI
的平衡常数K=800,可推断AtI+I-⇌AtI 的平衡常数K
的平衡常数K(4)在AtI中加入I2和I-的混合溶液,滴加AgNO3溶液,发现所得沉淀中只有AgI而没有共沉淀的AgAt(如果有AgAt,必然会被共沉淀),然而在上述产物中加入Pb(IO3)2却发现有砹的共沉淀。写出有关化学方程式
(5)已知室温下ICH2COOH的pKa=3.12,由此可推断AtCH2COOH的pKa
您最近一年使用:0次
解题方法
2 . 题将0.0167 mol I2和0.0167 mol H2置于预先抽真空的特制1 L密闭容器中,加热到1500K,体系达平衡,总压强为4.56 bar(1 bar= 100kPa),体系中存在如下反应关系:
① I2(g) 2I(g) Kp1 =2.00
2I(g) Kp1 =2.00
② I2(g)+ H2(g) 2HI(g) Kp2
2HI(g) Kp2
③HI(g) I(g)+H(g) Kp3= 8.0×10-6
I(g)+H(g) Kp3= 8.0×10-6
④ H2(g) 2H(g) Kp4
2H(g) Kp4
(1)计算1500 K体系中I2(g)和H2(g)未分解时的分压(R= 8.314J·mol-1·K-1)_____ 。
(2)计算1500 K平衡体系中除H(g)之外所有物种的分压_____ 。
(3)计算Kp2_____ 。
(4)计算Kp4. (若未算出Kp2,可设Kp2= 10.0)_____ 。
为使处理过程简洁方便,计算中请务必使用如下约定符号,在平衡表达式中默认各分压项均除以标准分压。
① I2(g)
 2I(g) Kp1 =2.00
2I(g) Kp1 =2.00② I2(g)+ H2(g)
 2HI(g) Kp2
2HI(g) Kp2③HI(g)
 I(g)+H(g) Kp3= 8.0×10-6
I(g)+H(g) Kp3= 8.0×10-6④ H2(g)
 2H(g) Kp4
2H(g) Kp4(1)计算1500 K体系中I2(g)和H2(g)未分解时的分压(R= 8.314J·mol-1·K-1)
(2)计算1500 K平衡体系中除H(g)之外所有物种的分压
(3)计算Kp2
(4)计算Kp4. (若未算出Kp2,可设Kp2= 10.0)
为使处理过程简洁方便,计算中请务必使用如下约定符号,在平衡表达式中默认各分压项均除以标准分压。
| 体系 总压 | I2(g)起 始分压 | I2(g)平 衡分压 | I(g)平衡 分压 | H2(g)起 始分压 | H2(g)平 衡分压 | H(g)平 衡分压 | HI (g)平 衡分压 |
| pt | x0 | x1 | x2 | y0 | y1 | y2 | z |
您最近一年使用:0次
3 . 已知:
H2S水溶液的酸式解离常数K1=1.1 × 10-7,K2=1.3 ×10-13;ZnS的溶度积常数 Ksp = 2.5×10-22;CuS Ksp = 6.3×10-36。
NO + 4H++ 3e- ⇌ NO + 2H2O E
+ 4H++ 3e- ⇌ NO + 2H2O E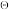 = 0.957V
= 0.957V
S+2H++2e- ⇌H2S E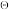 = 0.142V
= 0.142V
S+2e- ⇌ S2- E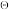 =-0.476V
=-0.476V
(1)ZnS 可以溶于稀盐酸,反应式为ZnS + 2H+⇌ Zn2++ H2S,拟将0.010 molZnS溶于1升盐酸中,求所需盐酸的最低浓度________ 。
(2) CuS 可以溶于HNO3,反应式为3CuS+2NO +8H+ ⇌3Cu2++2NO+3 S+4 H2O,求该反应的平衡常数K
+8H+ ⇌3Cu2++2NO+3 S+4 H2O,求该反应的平衡常数K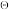
________ 。
H2S水溶液的酸式解离常数K1=1.1 × 10-7,K2=1.3 ×10-13;ZnS的溶度积常数 Ksp = 2.5×10-22;CuS Ksp = 6.3×10-36。
NO
 + 4H++ 3e- ⇌ NO + 2H2O E
+ 4H++ 3e- ⇌ NO + 2H2O E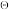 = 0.957V
= 0.957VS+2H++2e- ⇌H2S E
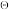 = 0.142V
= 0.142VS+2e- ⇌ S2- E
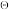 =-0.476V
=-0.476V(1)ZnS 可以溶于稀盐酸,反应式为ZnS + 2H+⇌ Zn2++ H2S,拟将0.010 molZnS溶于1升盐酸中,求所需盐酸的最低浓度
(2) CuS 可以溶于HNO3,反应式为3CuS+2NO
 +8H+ ⇌3Cu2++2NO+3 S+4 H2O,求该反应的平衡常数K
+8H+ ⇌3Cu2++2NO+3 S+4 H2O,求该反应的平衡常数K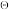
您最近一年使用:0次
4 . I.肌红蛋白(Mb)是由肽链和血红素辅基组成的可结合氧的蛋白,广泛存在于肌肉中。肌红蛋白与氧气的结合度(α)与氧分压P(O2)密切相关,存在如下平衡:Mb(aq)+O2(g) MbO2(aq)(a)其中,kA和kD分别是正向和逆向反应的速率常数。37°C,反应达平衡时测得的一组实验数据如图所示。
MbO2(aq)(a)其中,kA和kD分别是正向和逆向反应的速率常数。37°C,反应达平衡时测得的一组实验数据如图所示。

(1)计算37°C下反应(a)的平衡常数K_______ 。
(2)导出平衡时结合度(α)随氧分压变化的表达式_______ 。若空气中氧分压为20.0kPa,计算人正常呼吸时Mb与氧气的最大结合度_______ 。
(3)研究发现,正向反应速率v正=kA(Mb)P(O2);逆向反应速率v逆=kD(MbO2)。已知kD=60s-1,计算速率常数kA=_______ 。当保持氧分压为20.0kPa,计算结合度达50%所需时间_______ 。(提示:对于v逆=kD(MbO2),MbO2分解50%所需时间为t=0.693/kD)
II.Mb含有一个Fe(II),呈顺磁性,与O2结合后形成的MbO2是抗磁性的。MbO2中的铁周围的配位场可近似为八面体场。
(4)这一过程中Fe(II)的价态是否发生改变_______ ,简述原因_______ 。
(5)写出MbO2中铁离子在八面体场中的价电子排布_______ 。
(6)结合O2前后铁离子的半径是不变、变大还是变小_______ ,简述原因_______ 。
(7)O2分子呈顺磁性,它与Mb结合后,价电子排布是否发生变化___ ,简述原因____ 。
 MbO2(aq)(a)其中,kA和kD分别是正向和逆向反应的速率常数。37°C,反应达平衡时测得的一组实验数据如图所示。
MbO2(aq)(a)其中,kA和kD分别是正向和逆向反应的速率常数。37°C,反应达平衡时测得的一组实验数据如图所示。
(1)计算37°C下反应(a)的平衡常数K
(2)导出平衡时结合度(α)随氧分压变化的表达式
(3)研究发现,正向反应速率v正=kA(Mb)P(O2);逆向反应速率v逆=kD(MbO2)。已知kD=60s-1,计算速率常数kA=
II.Mb含有一个Fe(II),呈顺磁性,与O2结合后形成的MbO2是抗磁性的。MbO2中的铁周围的配位场可近似为八面体场。
(4)这一过程中Fe(II)的价态是否发生改变
(5)写出MbO2中铁离子在八面体场中的价电子排布
(6)结合O2前后铁离子的半径是不变、变大还是变小
(7)O2分子呈顺磁性,它与Mb结合后,价电子排布是否发生变化
您最近一年使用:0次



