名校
1 . 已知反应A(g)+B(g)⇌C(g)+D(g)的平衡常数K值与温度的关系如表所示。830℃时,向一个2L的密闭容器中充入0.20molA和0.20molB,10s末达平衡。下列说法不正确 的是
| 温度/℃ | 700 | 830 | 1200 |
| K值 | 1.7 | 1.0 | 0.4 |
| A.达到平衡后,B的转化率为50% |
| B.该反应为吸热反应,升高温度,平衡正向移动 |
| C.反应初始至平衡,A的平均反应速率v(A)=0.005mol·L-1·s-1 |
| D.容器体积减小为原来的一半,平衡不移动,正、逆反应速率均增大 |
您最近一年使用:0次
2022-10-26更新
|
897次组卷
|
12卷引用:第二章 化学反应速率与化学平衡(B卷·能力提升练)【单元测试】2022-2023学年高二化学分层训练AB卷(人教版2019选择性必修1)
(已下线)第二章 化学反应速率与化学平衡(B卷·能力提升练)【单元测试】2022-2023学年高二化学分层训练AB卷(人教版2019选择性必修1)(已下线)第12练 用“三段式”模型突破化学平衡的计算-2022年【暑假分层作业】高二化学(2023届一轮复习通用)(已下线)考点21 化学反应速率-备战2023年高考化学一轮复习考点帮(全国通用)甘肃省庆阳第六中学2022-2023学年高二上学期第一次月考化学试题湖北省沙市中学2022-2023学年高二上学期第二次月考化学试题新疆乌鲁木齐市第八十中学2022-2023学年高二上学期期中考试化学试题浙江省杭师大附中2022-2023学年高二上学期期中考试 化学试题辽宁省铁岭市昌图县第一高级中学2022-2023学年高一下学期期末考试化学试题福建省福州第三中学2022-2023学年高二上学期半期考试化学试题广东省六校2022届高三下学期第六次联考化学试题湖北省荆、荆、襄、宜四地七校考试联盟2022-2023学年高二上学期期中联考化学试题广东省高州市第七中学等三校2022-2023学年高二上学期11月月考化学试题
名校
解题方法
2 . 三氯氢硅SiHCl3是制备硅烷、多晶硅的重要原料。对于反应2SiHCl3(g) SiH2Cl2(g)+SiCl4(g)采用大孔弱碱性阴离子交换树脂催化剂,在323 K和343 K时SiHCl3的转化率随时间变化的结果如图所示。
SiH2Cl2(g)+SiCl4(g)采用大孔弱碱性阴离子交换树脂催化剂,在323 K和343 K时SiHCl3的转化率随时间变化的结果如图所示。
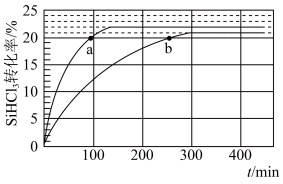
(1)343 K时反应的平衡转化率ɑ=_______ %。平衡常数K343K=_______ (保留2位小数)。
(2)在343 K下,要提高SiHCl3转化率,可采取的措施是_______ ;要缩短反应达到平衡的时间,可采取的措施有_______ 。
(3)比较a、b处反应速率大小:va_______ vb(填“大于”“小于”或“等于”)。反应速率v=v正−v逆=k正x2(SiHCl3)−k逆x(SiH2Cl2)x(SiCl4),k正、k逆分别为正、逆反应速率常数,x为物质的量分数,计算a处 =
=_______ (保留1位小数)。
 SiH2Cl2(g)+SiCl4(g)采用大孔弱碱性阴离子交换树脂催化剂,在323 K和343 K时SiHCl3的转化率随时间变化的结果如图所示。
SiH2Cl2(g)+SiCl4(g)采用大孔弱碱性阴离子交换树脂催化剂,在323 K和343 K时SiHCl3的转化率随时间变化的结果如图所示。
(1)343 K时反应的平衡转化率ɑ=
(2)在343 K下,要提高SiHCl3转化率,可采取的措施是
(3)比较a、b处反应速率大小:va
 =
=
您最近一年使用:0次
2022-05-18更新
|
1615次组卷
|
13卷引用:高中必刷题高二选择性必修1第二章 化学反应速率与化学平衡 第二章素养检测
高中必刷题高二选择性必修1第二章 化学反应速率与化学平衡 第二章素养检测山西省临汾市2020届高三上学期第二次月考化学试题(已下线)专题十一 化学反应速率和化学平衡(真题汇编)-2020年高考二轮模块化复习之《化学基本原理》名师讲案与提分特训鲁科版(2019)高二选择性必修第一册第2章 化学反应的方向、限度与速率 高考挑战区 过高考(已下线)考点17 化学反应速率及其影响因素-备战2022年高考化学一轮复习考点帮(全国通用)山东省临沂市兰陵县2021-2022学年高二上学期期中考试化学试题安徽省青阳县第一中学2021-2022学年高二下学期5月月考化学试题(已下线)考点21 化学反应速率-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)化学反应速率和化学平衡黑龙江省大庆市第四中学2020届高三下学期4月月考理综化学试题(已下线)考点17 化学反应速率及其影响因素-备战2022年高考化学一轮复习考点帮(浙江专用)山东省临沂市兰山区、罗庄区2021-2022学年高二上学期中考试化学试题浙江省浙东北联盟(ZDB)2023-2024学年高二上学期期中考试化学试题
3 . 在密闭容器中发生反应CO2(g) + H2(g)  CO(g) + H2O(g),其平衡常数(K)和温度(T)的关系如下表所示。
CO(g) + H2O(g),其平衡常数(K)和温度(T)的关系如下表所示。
(1)该反应的平衡常数表达式K=___________ ;由上表可知该反应为___________ 反应(填“吸热”或“放热”)。
(2)830℃时,向容器中充入2mol CO2、8mol H2,保持温度不变,反应达到平衡后,其平衡常数___________ 1.0(填“大于”“小于”或“等于”),此时CO2的物质的量为___________ 。
(3)下列有利于提高平衡时CO2转化率的措施有___________ (填字母)。
a.使用催化剂 b.升温 c.增大 CO2和 H2的投料比
(4)若1200℃时,在某时刻反应混合物中CO2、H2、CO、 H2O的浓度分别为2mol/L、2mol/L、4mol/L、4mol/L,则此时反应的平衡移动方向为___________ (填“正反应方向”“逆反应方向”或“不移动”)。
(5)实验发现,其它条件不变,在相同时间内,向上述反应体系中投入一定量的CaO,H2的体积分数增大,实验结果如图所示。
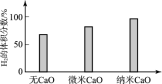
(已知:1微米 = 10-6米,1纳米= 10-9米)。
投入纳米CaO比微米CaO时,H2的体积分数更高的原因是___________ 。
 CO(g) + H2O(g),其平衡常数(K)和温度(T)的关系如下表所示。
CO(g) + H2O(g),其平衡常数(K)和温度(T)的关系如下表所示。| T/ ℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(2)830℃时,向容器中充入2mol CO2、8mol H2,保持温度不变,反应达到平衡后,其平衡常数
(3)下列有利于提高平衡时CO2转化率的措施有
a.使用催化剂 b.升温 c.增大 CO2和 H2的投料比
(4)若1200℃时,在某时刻反应混合物中CO2、H2、CO、 H2O的浓度分别为2mol/L、2mol/L、4mol/L、4mol/L,则此时反应的平衡移动方向为
(5)实验发现,其它条件不变,在相同时间内,向上述反应体系中投入一定量的CaO,H2的体积分数增大,实验结果如图所示。

(已知:1微米 = 10-6米,1纳米= 10-9米)。
投入纳米CaO比微米CaO时,H2的体积分数更高的原因是
您最近一年使用:0次
名校
解题方法
4 . 能源开发和利用是科学研究的热点课题。
(1)几个有关CO的热化学方程式如下:
I.CO(g)+2H2(g) CH3OH(g) △H1
CH3OH(g) △H1
II.2CH3OH(g) CH3OCH3(g)+H2O(g) △H2
CH3OCH3(g)+H2O(g) △H2
III.CO(g)+H2O(g) CO2(g)+H2(g) △H3
CO2(g)+H2(g) △H3
则3CO(g)+3H2(g) CH3OCH3(g)+CO2(g) △H=
CH3OCH3(g)+CO2(g) △H=___________ (用含△H1、△H2、△H3的代数表示)。
(2)在1 L恒容密闭容器中充入一定量CH3OH发生反应:2CH3OH(g) CH3OCH3(g)+H2O(g) △H,测得CH3OH的浓度与温度的关系如图所示:
CH3OCH3(g)+H2O(g) △H,测得CH3OH的浓度与温度的关系如图所示:
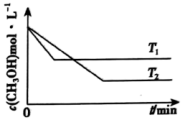
①△H___________ (填“>”“<”或“=”)0,说明理由___________ 。
②在T1时达到平衡后,再向容器中充入少量甲醇蒸气,CH3OH的平衡转化率___________ (填“增大”“减小”或“不变”)。
(3)工业上,利用水煤气合成CH3OH的反应表示如下:2H2(g)+CO(g) CH3OH(g) △H=-91.0 kJ·mol-1,向1 L的恒容密容器中加入0.1 mol H2和0.05 mol CO在一定温度下发生上述反应,10 min后反应达到平衡状态,测得放出的热量为3.64 kJ。
CH3OH(g) △H=-91.0 kJ·mol-1,向1 L的恒容密容器中加入0.1 mol H2和0.05 mol CO在一定温度下发生上述反应,10 min后反应达到平衡状态,测得放出的热量为3.64 kJ。
①从反应开始恰好平衡状态时,H2的平均反应速率v(H2)为___________ 。
②在温度不变条件下,上述反应达到平衡后再向容器中充入0.01 mol H2和0.05 mol CH3OH(g)时,平衡___________ (填“向左移动”、“向右移动”或“不移动”)。
(4)探究CH3OH合成反应化学平衡的影响因素,有利于提高CH3OH的产率。以CO2、H2为原料合成CH3OH涉及的主要反应如下:
I.CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H=-49.5 kJ·mol-1
CH3OH(g)+H2O(g) △H=-49.5 kJ·mol-1
II.CO(g)+2H2(g) CH3OH(g) △H2=-90.4 kJ·mol-1
CH3OH(g) △H2=-90.4 kJ·mol-1
III.CO2(g)+H2(g) CO(g)+H2O(g) △H3
CO(g)+H2O(g) △H3
一定条件下,向体积为V L的恒容密闭容器中通入1 mol CO2和3 mol H2发生上述反应,达到平衡时,容器中CH3OH(g)为a mol,CO为b mol,此时H2O(g)的浓度为___________ mol·L-1(用含a、b、V的代数式表示,下同),反应III的平衡常数为___________ 。
(1)几个有关CO的热化学方程式如下:
I.CO(g)+2H2(g)
 CH3OH(g) △H1
CH3OH(g) △H1II.2CH3OH(g)
 CH3OCH3(g)+H2O(g) △H2
CH3OCH3(g)+H2O(g) △H2III.CO(g)+H2O(g)
 CO2(g)+H2(g) △H3
CO2(g)+H2(g) △H3则3CO(g)+3H2(g)
 CH3OCH3(g)+CO2(g) △H=
CH3OCH3(g)+CO2(g) △H=(2)在1 L恒容密闭容器中充入一定量CH3OH发生反应:2CH3OH(g)
 CH3OCH3(g)+H2O(g) △H,测得CH3OH的浓度与温度的关系如图所示:
CH3OCH3(g)+H2O(g) △H,测得CH3OH的浓度与温度的关系如图所示:
①△H
②在T1时达到平衡后,再向容器中充入少量甲醇蒸气,CH3OH的平衡转化率
(3)工业上,利用水煤气合成CH3OH的反应表示如下:2H2(g)+CO(g)
 CH3OH(g) △H=-91.0 kJ·mol-1,向1 L的恒容密容器中加入0.1 mol H2和0.05 mol CO在一定温度下发生上述反应,10 min后反应达到平衡状态,测得放出的热量为3.64 kJ。
CH3OH(g) △H=-91.0 kJ·mol-1,向1 L的恒容密容器中加入0.1 mol H2和0.05 mol CO在一定温度下发生上述反应,10 min后反应达到平衡状态,测得放出的热量为3.64 kJ。①从反应开始恰好平衡状态时,H2的平均反应速率v(H2)为
②在温度不变条件下,上述反应达到平衡后再向容器中充入0.01 mol H2和0.05 mol CH3OH(g)时,平衡
(4)探究CH3OH合成反应化学平衡的影响因素,有利于提高CH3OH的产率。以CO2、H2为原料合成CH3OH涉及的主要反应如下:
I.CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H=-49.5 kJ·mol-1
CH3OH(g)+H2O(g) △H=-49.5 kJ·mol-1II.CO(g)+2H2(g)
 CH3OH(g) △H2=-90.4 kJ·mol-1
CH3OH(g) △H2=-90.4 kJ·mol-1III.CO2(g)+H2(g)
 CO(g)+H2O(g) △H3
CO(g)+H2O(g) △H3一定条件下,向体积为V L的恒容密闭容器中通入1 mol CO2和3 mol H2发生上述反应,达到平衡时,容器中CH3OH(g)为a mol,CO为b mol,此时H2O(g)的浓度为
您最近一年使用:0次
2021-07-02更新
|
1679次组卷
|
7卷引用:第2章 化学反应速率和化学平衡(提分小卷)-【单元测试】2021-2022学年高二化学尖子生选拔卷(人教版选修4)
(已下线)第2章 化学反应速率和化学平衡(提分小卷)-【单元测试】2021-2022学年高二化学尖子生选拔卷(人教版选修4)(已下线)第二章 化学反应速率与化学平衡(B卷·能力提升练)【单元测试】2022-2023学年高二化学分层训练AB卷(人教版2019选择性必修1)广西河池市九校2020-2021学年高二下学期第二次联考化学试题(已下线)2.2.3 影响化学平衡的因素(素养提优B练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)河南宏力学校2021-2022学年高二上学期期中考试化学试题浙江省杭师大附中2022-2023学年高二上学期期中考试 化学试题重庆市缙云教育联盟2021-2022学年高三10月质量检测化学试题
5 . 在密闭容器中,给一氧化碳和水蒸气的气体混合物加热,在催化剂存在下发生反应:CO(g)+ (g)
(g)
 (g)+
(g)+ (g)。在500℃时,平衡常数K=9,若反应开始时,一氧化碳和水蒸气的浓度都是0.02mol/L,则在此条件下CO的转化率为
(g)。在500℃时,平衡常数K=9,若反应开始时,一氧化碳和水蒸气的浓度都是0.02mol/L,则在此条件下CO的转化率为
 (g)
(g)
 (g)+
(g)+ (g)。在500℃时,平衡常数K=9,若反应开始时,一氧化碳和水蒸气的浓度都是0.02mol/L,则在此条件下CO的转化率为
(g)。在500℃时,平衡常数K=9,若反应开始时,一氧化碳和水蒸气的浓度都是0.02mol/L,则在此条件下CO的转化率为| A.25% | B.50% | C.75% | D.80% |
您最近一年使用:0次
2021-06-19更新
|
1673次组卷
|
32卷引用:人教版高中化学选修4第二章《化学反应速率与化学平衡》测试卷
人教版高中化学选修4第二章《化学反应速率与化学平衡》测试卷2014-2015陕西省西安市庆安高级中学高二上学期期末化学试卷2014-2015陕西省西安市七十中高二上学期期末考试化学试卷2016-2017学年黑龙江哈尔滨六中高二上期中化学试卷2016-2017学年黑龙江牡丹江中学高二上期中理化学卷安徽省滁州市民办高中2017-2018学年高二下学期第一次联考化学试题山西省朔州市平鲁区李林中学2018-2019学年高二上学期第一次月考化学试题【全国百强校】黑龙江省牡丹江市第一高级中学2018-2019学年高二(理)上学期期中考试化学试题安徽省合肥市第九中学2018-2019学年高二上学期期中考试化学试题【全国百强校】内蒙古巴彦淖尔一中2018-2019学年高二上学期期中考试化学试题湖南省涟源一中2018-2019学年高二上学期第二次月考化学试题河北省鹿泉第一中学2019-2020学年高二9月月考化学试题湖南省长沙市长郡中学2018-2019学年高二上学期期末考试化学试题山西省阳泉市2019-2020学年高二上学期期末考试化学试题黑龙江省安达市第七中学2019-2020学年高二3月月考化学试题人教版(2019)高二选择性必修第一册 第二章 化学反应速率与化学平衡 第二节 化学平衡 方法帮河南省安阳市滑县实验学校2020-2021学年高二上学期期中考试化学试题(普通班)四川省成都市实验外国语学校(西区)2019-2020 学年高二上学期期中考试化学试题(已下线)2.3.3 化学平衡常数-2021-2022学年高二化学课后培优练(人教版选修4)山西省大同市浑源县第七中学2020-2021学年高二上学期第一次月考化学试题(已下线)专题25 关于化学平衡的计算-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)江西省南昌市知行中学2021-2022学年高二上学期期中化学试题河南宏力学校2021-2022学年高二上学期期中考试化学试题内蒙古赤峰学院附属中学2023-2024学年高二上学期12月期中考试化学试题2015-2016学年湖北航天高中、安陆二中等五校高二上期中化学试卷2015-2016学年贵州省思南中学高二上二次月考化学试卷湖北省宜昌市葛洲坝中学2017-2018学年高二9月月考化学试题湖南省醴陵市第一中学2018-2019学年高二上学期入学考试化学试题【全国百强校】黑龙江省双鸭山市第一中学2018-2019学年高二上学期第一次月考化学试题新疆石河子第二中学2019-2020学年高二上学期第一次阶段考试化学试题云南省西双版纳傣族自治州勐腊县第一中学2019-2020学年高二上学期期末考试化学试题江西省宜春市丰城市2022-2023学年高二上学期1月期末化学试题
解题方法
6 . 850K时,在一密闭反应器中充入一定量的SO2和O2,当反应达到平衡后测得SO2、O2、SO3的浓度分别为0.0020 mol• L-1、0.0025 mol• L-1、0.0020 mol• L-1.则该温度下反应的2SO2+O2 2SO3平衡常数为:
2SO3平衡常数为:
 2SO3平衡常数为:
2SO3平衡常数为:| A.25 | B.0.0025 | C.40 | D.400 |
您最近一年使用:0次
2021-01-13更新
|
1155次组卷
|
5卷引用:第二章 化学反应速率与化学平衡(A卷·知识通关练)【单元测试】2022-2023学年高二化学分层训练AB卷(人教版2019选择性必修1)
(已下线)第二章 化学反应速率与化学平衡(A卷·知识通关练)【单元测试】2022-2023学年高二化学分层训练AB卷(人教版2019选择性必修1)(已下线)2.2.2 化学平衡常数(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)(已下线)2.2.1 化学平衡常数-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)上海市市北中学2022-2023学年高二上学期期中考试(等级)化学试题福建省莆田第十五中学2019-2020学年高二上学期期末考试化学试题
7 . 一定量的CO2与足量的碳在体积可变的恒压密闭容器中反应:C(s)+CO2(g) 2CO(g)。平衡时,体系中气体体积分数与温度的关系如下图所示:
2CO(g)。平衡时,体系中气体体积分数与温度的关系如下图所示:
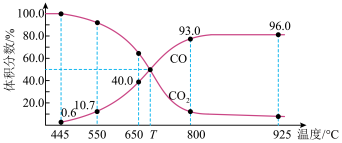
已知:气体分压(P分)=气体总压(P总)×体积分数。下列说法正确的是
 2CO(g)。平衡时,体系中气体体积分数与温度的关系如下图所示:
2CO(g)。平衡时,体系中气体体积分数与温度的关系如下图所示:
已知:气体分压(P分)=气体总压(P总)×体积分数。下列说法正确的是
| A.925℃时,用平衡分压代替平衡浓度表示的化学平衡常数Kp=24.0P总 |
| B.550℃时,若充入惰性气体,v正,v逆均减小,平衡不移动 |
| C.T℃时,若充入等体积的CO2和CO,平衡向逆反应方向移动 |
| D.650℃时,反应达平衡后CO2的转化率为25.0% |
您最近一年使用:0次
2020-11-24更新
|
322次组卷
|
4卷引用:选择性必修1 专题2 第三单元综合训练
8 . 一定温度下,将2molA和2molB两种气体混合放入体积为2L的密闭刚性容器中,发生反应3A(g)+B(g) xC(g)+2D(g),2min末反应达到平衡,生成0.8molD,并测得C的物质的量浓度为0.4mol·L-1,下列说法正确的是( )
xC(g)+2D(g),2min末反应达到平衡,生成0.8molD,并测得C的物质的量浓度为0.4mol·L-1,下列说法正确的是( )
| A.此温度下该反应的平衡常数K等于0.5 |
| B.A的平衡转化率为40% |
| C.x的值为1 |
| D.A和B的平衡转化率相等 |
您最近一年使用:0次
2020-11-18更新
|
3994次组卷
|
34卷引用:第2章 化学反应速率和化学平衡(选拔卷)-【单元测试】2021-2022学年高二化学尖子生选拔卷(人教版选修4)
(已下线)第2章 化学反应速率和化学平衡(选拔卷)-【单元测试】2021-2022学年高二化学尖子生选拔卷(人教版选修4)(已下线)第二章 化学反应速率与化学平衡(B卷·能力提升练)【单元测试】2022-2023学年高二化学分层训练AB卷(人教版2019选择性必修1)北京首都师范大学附属中学2020-2021学年高二上学期期中考试化学试题内蒙古阿荣旗第一中学2020-2021学年高二上学期期中考试化学试题安徽省毫州市涡阳第—中学2021-2022学年高二上学期第一次教学质量检测化学试题北京市第十四中学2021-2022学年高二上学期期中考试化学试题(已下线)2.2.2 化学平衡常数(素养提优B练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)四川省宜宾市第一中学2021-2022学年高二上学期期中联考化学试题 安徽省合肥八中2021-2022学年高二上学期课后限时作业III暨第三次月考化学试题(已下线)第27练 化学平衡-2023年高考化学一轮复习小题多维练(全国通用)(已下线)2.2.1 化学平衡常数-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)山东省济南市莱芜第四中学2021-2022学年高二上学期第一次质量检测化学试题广东省广州市第二中学2022-2023学年高二上学期期中考试化学试题安徽省舒城晓天中学2022-2023学年高二上学期第一次质量检测化学试题河南省南乐县第一高级中学2021-2022学年高二上学期9月半月考化学试题广东省广州大学附属中学2022-2023学年高二上学期期中考试化学试题广东省惠州市实验中学2022-2023学年高二上学期期中考试化学试题河南宏力学校2021-2022学年高二上学期期中考试化学试题河南省商丘市宁陵县高级中学2023-2024学年高二上学期第一次考试化学试题四川省成都市第八中学校2022-2023学年高二上学期11月期中考试化学试题陕西省西安中学2023-2024学年高二上学期11月期中考试化学试题广东省肇庆市第一中学2023-2024学年高二上学期期中考试化学试题河北省石家庄市辛集市2023-2024学年高二上学期2月期末考试化学试题河南省济源高级中学2023-2024学年高二上学期开学考试 化学试题山东省滕州市第五中学2021-2022学年高二上学期第一次单元测试化学试题云南省马关县第一中学2021-2022学年高二下学期开学考试化学试题山东省潍坊实验中学2022-2023学年高二上学期第一次单元过关检测化学试题广东省深圳市教育联盟2022-2023学年高二上学期联考化学试题 浙江省金华市横店高中2022-2023学年高二上学期10月份检测化学试题福建省上杭县才溪中学2022-2023学年高二上学期10月月考化学试题山东省新泰市第一中学老校区(新泰中学)2023-2024学年高二上学期第一次质量检测化学试题吉林省辽源市田家炳高中友好学校七十六届期末联考2023-2024学年高二上学期1月期末化学试题云南省曲靖二中云师高级中学 第二中学 兴教学校2023-2024学年高二上学期12月期中联考化学试题重庆十八中两江实验中学校2022-2023学年高二上学期第一次月考化学试题
解题方法
9 . (1)Deacon发明的直接氧化法为:4HCl(g)+O2(g) 2Cl2(g)+2H2O(g)。如图为刚性容器中,进料浓度比c(HCl)∶c(O2)分别等于1∶1、4∶1、7∶1时HCl平衡转化率随温度变化的关系:
2Cl2(g)+2H2O(g)。如图为刚性容器中,进料浓度比c(HCl)∶c(O2)分别等于1∶1、4∶1、7∶1时HCl平衡转化率随温度变化的关系:

可知反应平衡常数K(300℃)______________ K(400℃)(填“大于”或“小于”)。设HCl初始浓度为c0,根据进料浓度比c(HCl)∶c(O2)=1∶1的数据计算K(400℃)=______________ (列出计算式)。按化学计量比进料可以保持反应物高转化率,同时降低产物分离的能耗。进料浓度比c(HCl)∶c(O2)过高的不利影响是______________ 。
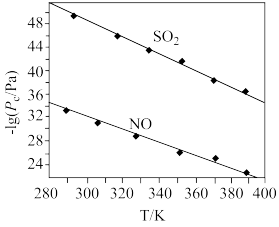
(2)在不同温度下,NaClO2溶液脱硫、脱硝的反应中SO2和NO的平衡分压pc如图所示。
①由图分析可知,反应温度升高,脱硫、脱硝反应的平衡常数均______________ (填“增大”、“不变”或“减小”)。
②反应 +2
+2 =2
=2 +Cl﹣的平衡常数K表达式为
+Cl﹣的平衡常数K表达式为______________ 。
 2Cl2(g)+2H2O(g)。如图为刚性容器中,进料浓度比c(HCl)∶c(O2)分别等于1∶1、4∶1、7∶1时HCl平衡转化率随温度变化的关系:
2Cl2(g)+2H2O(g)。如图为刚性容器中,进料浓度比c(HCl)∶c(O2)分别等于1∶1、4∶1、7∶1时HCl平衡转化率随温度变化的关系:

可知反应平衡常数K(300℃)
(2)在不同温度下,NaClO2溶液脱硫、脱硝的反应中SO2和NO的平衡分压pc如图所示。
①由图分析可知,反应温度升高,脱硫、脱硝反应的平衡常数均
②反应
 +2
+2 =2
=2 +Cl﹣的平衡常数K表达式为
+Cl﹣的平衡常数K表达式为
您最近一年使用:0次
2020-11-06更新
|
202次组卷
|
3卷引用:选择性必修1 专题2 第三单元综合训练
选择性必修1 专题2 第三单元综合训练(已下线)2.4 化学反应的调控(素养提优B练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)湖南省常德外国语学校2020-2021学年高二上学期期中考试化学试题
名校
解题方法
10 . 合成氨反应 ,在
,在 时,
时, ,
, 。
。
(1)从平衡常数来看,合成氨反应的限度已经很大了,为什么还需要使用催化剂?_______ 。
(2) 、
、 时,在
时,在 的密闭容器中充入
的密闭容器中充入 、
、 和
和 ,开始的瞬间,反应向
,开始的瞬间,反应向_________ (填“正”或“逆”)反应方向进行,反应进行 后体系
后体系_________ (填“吸收”或“放出”)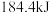 能量,容器内压强与初始压强之比为
能量,容器内压强与初始压强之比为_________ 。
(3)从开始至 时,用
时,用 表示该反应的平均反应速率为
表示该反应的平均反应速率为_________ 。
 ,在
,在 时,
时, ,
, 。
。(1)从平衡常数来看,合成氨反应的限度已经很大了,为什么还需要使用催化剂?
(2)
 、
、 时,在
时,在 的密闭容器中充入
的密闭容器中充入 、
、 和
和 ,开始的瞬间,反应向
,开始的瞬间,反应向 后体系
后体系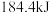 能量,容器内压强与初始压强之比为
能量,容器内压强与初始压强之比为(3)从开始至
 时,用
时,用 表示该反应的平均反应速率为
表示该反应的平均反应速率为
您最近一年使用:0次
2020-09-19更新
|
282次组卷
|
5卷引用:第二章 化学反应速率与化学平衡(基础过关)-2020-2021学年高二化学单元测试定心卷(人教版2019选择性必修一)
(已下线)第二章 化学反应速率与化学平衡(基础过关)-2020-2021学年高二化学单元测试定心卷(人教版2019选择性必修一)鲁科版(2019)选择性必修1 第2章 化学反应的方向、限度与速率 第4节 化学反应条件的优化—工业合成氨人教版(2019)高二选择性必修第一册 第二章 化学反应速率与化学平衡 第四节 化学反应的调控 方法帮海南省海口市第四中学2020-2021学年高二上学期第一次月考化学试题湖北随州市第一中学2020-2021学年高二上学期期中考试化学试题



