(1)Deacon发明的直接氧化法为:4HCl(g)+O2(g) 2Cl2(g)+2H2O(g)。如图为刚性容器中,进料浓度比c(HCl)∶c(O2)分别等于1∶1、4∶1、7∶1时HCl平衡转化率随温度变化的关系:
2Cl2(g)+2H2O(g)。如图为刚性容器中,进料浓度比c(HCl)∶c(O2)分别等于1∶1、4∶1、7∶1时HCl平衡转化率随温度变化的关系:

可知反应平衡常数K(300℃)______________ K(400℃)(填“大于”或“小于”)。设HCl初始浓度为c0,根据进料浓度比c(HCl)∶c(O2)=1∶1的数据计算K(400℃)=______________ (列出计算式)。按化学计量比进料可以保持反应物高转化率,同时降低产物分离的能耗。进料浓度比c(HCl)∶c(O2)过高的不利影响是______________ 。
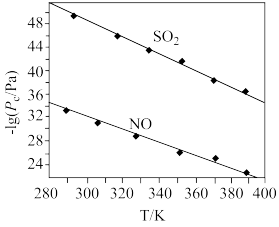
(2)在不同温度下,NaClO2溶液脱硫、脱硝的反应中SO2和NO的平衡分压pc如图所示。
①由图分析可知,反应温度升高,脱硫、脱硝反应的平衡常数均______________ (填“增大”、“不变”或“减小”)。
②反应 +2
+2 =2
=2 +Cl﹣的平衡常数K表达式为
+Cl﹣的平衡常数K表达式为______________ 。
 2Cl2(g)+2H2O(g)。如图为刚性容器中,进料浓度比c(HCl)∶c(O2)分别等于1∶1、4∶1、7∶1时HCl平衡转化率随温度变化的关系:
2Cl2(g)+2H2O(g)。如图为刚性容器中,进料浓度比c(HCl)∶c(O2)分别等于1∶1、4∶1、7∶1时HCl平衡转化率随温度变化的关系:

可知反应平衡常数K(300℃)
(2)在不同温度下,NaClO2溶液脱硫、脱硝的反应中SO2和NO的平衡分压pc如图所示。
①由图分析可知,反应温度升高,脱硫、脱硝反应的平衡常数均
②反应
 +2
+2 =2
=2 +Cl﹣的平衡常数K表达式为
+Cl﹣的平衡常数K表达式为
20-21高二上·湖南常德·期中 查看更多[3]
(已下线)2.4 化学反应的调控(素养提优B练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)选择性必修1 专题2 第三单元综合训练湖南省常德外国语学校2020-2021学年高二上学期期中考试化学试题
更新时间:2020-11-06 18:24:31
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】在100℃时,将0.1mol的四氧化二氮气体充入1 L抽空的密闭容器中,发生反应,隔一定时间对该容器内的物质进行分析,得到如下数据:
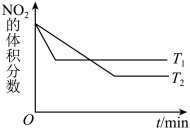
(1)该反应的化学方程式为______________________ ,表中c2_____ c3_____ a______ b(选填“>”、“<”、“==”)。
(2)20 s时四氧化二氮的浓度c1=____________ mol·l—1依据图象可以判断该反应的 ΔH___ 0(填“>”或“<”)
| 浓度 时间(S) | 0 | 20 | 40 | 60 | 80 | 100 |
| c(N2O4)/mol·L—1 | 0.1 | c1 | 0.05 | c3 | a | b |
| c(NO2)/mol·L—1 | 0 | 0.06 | c2 | 0.12 | 0.12 | 0.12 |

(1)该反应的化学方程式为
(2)20 s时四氧化二氮的浓度c1=
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐2】钾是—种活泼的金属,工业上通常用金属钠和氯化钾在高温下反应制取。该反应为:Na(l)+KCl(l) NaCl(l)+K(g)(正反应吸热)
NaCl(l)+K(g)(正反应吸热)
该反应的平衡常数可表示为:K=c(K),各物质的沸点与压强的关系见上表。
(1)在常压下金属钾转变为气态从反应混合物中分离的最低温度约为_______ ,而反应的最高温度应低于_______ 。
(2)在制取钾的过程中,为了提高原料的转化率可以采取的措施是___________ 。
(3)常压下,当反应温度升高到900℃时,该反应的平衡常数可表示为:K=_____ 。
 NaCl(l)+K(g)(正反应吸热)
NaCl(l)+K(g)(正反应吸热)压强(kPa) | 13.33 | 53.32 | 101.3 |
K的沸点(℃) | 590 | 710 | 770 |
Na的沸点(℃) | 700 | 830 | 890 |
KCl的沸点(℃) | 1437 | ||
NaCl的沸点(℃) | 1465 |
该反应的平衡常数可表示为:K=c(K),各物质的沸点与压强的关系见上表。
(1)在常压下金属钾转变为气态从反应混合物中分离的最低温度约为
(2)在制取钾的过程中,为了提高原料的转化率可以采取的措施是
(3)常压下,当反应温度升高到900℃时,该反应的平衡常数可表示为:K=
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐1】在某2L的密闭容器中加入0.1mol碘单质和足量钨(W),在943K时,发生反应W(s)+I2(g)⇌WI2(g),当I2的转化率为20%时,达化学平衡状态;
(1)反应从开始至平衡状态过程中用时20s,其平均反应速率v(WI2)为_________________ ;
(2)943K时,该反应的平衡常数K=_______________ ;
(3)若起始时,加入的碘为0.2mol(其他条件不变)达平衡时容器中气体的体积比V(I2):V(WI2)=____________ ;
(4)在上述(1)平衡状态下,同时增加I2(g)和WI2(g)各0.02mol(其他条件不变),化学平衡向____________ (填“正反应”或“逆反应”)方向移动,判断的依据是____________ 。
(1)反应从开始至平衡状态过程中用时20s,其平均反应速率v(WI2)为
(2)943K时,该反应的平衡常数K=
(3)若起始时,加入的碘为0.2mol(其他条件不变)达平衡时容器中气体的体积比V(I2):V(WI2)=
(4)在上述(1)平衡状态下,同时增加I2(g)和WI2(g)各0.02mol(其他条件不变),化学平衡向
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐2】合成氨的捷姆金和佩热夫速率方程式为γ=k1p(N2)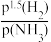 -k2
-k2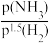 ,γ为反应的瞬时总速率,为正反应和逆反应速率之差,k1、k2是正、逆反应速率常数。合成氨反应N2+3H2
,γ为反应的瞬时总速率,为正反应和逆反应速率之差,k1、k2是正、逆反应速率常数。合成氨反应N2+3H2 2NH3的平衡常数Kp=
2NH3的平衡常数Kp=_____ (用k1,k2表示)(注:Kp用各物质平衡分压来表示)。
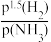 -k2
-k2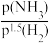 ,γ为反应的瞬时总速率,为正反应和逆反应速率之差,k1、k2是正、逆反应速率常数。合成氨反应N2+3H2
,γ为反应的瞬时总速率,为正反应和逆反应速率之差,k1、k2是正、逆反应速率常数。合成氨反应N2+3H2 2NH3的平衡常数Kp=
2NH3的平衡常数Kp=
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】甲醇是结构最为简单的饱和一元醇,又称“木醇”或“木精”。甲醇是一碳化学基础的原料和优质的燃料,主要应用于精细化工、塑料、能源等领域。已知甲醇制备的有关化学反应如下:
反应①:
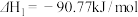
反应②:
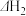
反应③:
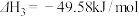
(1)若500℃时三个反应的平衡常数依次为K1、K2、K3,已知500℃时K1、K2的值分别为2.5、1.0,并测得该温度下反应③在某时刻,H2(g)、CO2(g)、CH3OH(g)、H2O(g)的浓度(mol/L)分别为0.8、0.1、0.3、0.15,则此时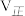
__________ 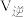 (填“>”、“=”或“<”)
(填“>”、“=”或“<”)
(2)在3L容积可变的密闭容器中发生反应②,c(CO)随反应时间t变化如图中曲线Ⅰ所示。若在t0时刻分别改变一个条件,曲线Ⅰ变为曲线Ⅱ和曲线III。当曲线Ⅰ变为曲线Ⅱ时,改变的条件是____________ 。当通过改变压强使曲线Ⅰ变为曲线III时,曲线III达到平衡时容器的体积为___________ 。
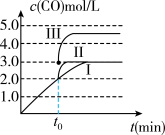
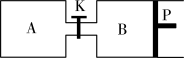
(3)在另一温度下按反应③合成甲醇的反应,如图关闭K,向A容器中充入1molCO2和4molH2,向B容器中充入1.2molCO2和4.8molH2,两容器分别发生上述反应。已知起始时容器A和B的体积均为aL,反应达到平衡时容器B的体积为0.9aL,维持其他条件不变,若打开K一段时间后重新达到平衡,容器B的体积为__________ L(不考虑温度的变化,P为可自由滑动活塞,不考虑活塞的摩擦力)。
反应①:

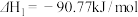
反应②:

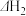
反应③:

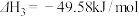
(1)若500℃时三个反应的平衡常数依次为K1、K2、K3,已知500℃时K1、K2的值分别为2.5、1.0,并测得该温度下反应③在某时刻,H2(g)、CO2(g)、CH3OH(g)、H2O(g)的浓度(mol/L)分别为0.8、0.1、0.3、0.15,则此时
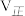
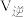 (填“>”、“=”或“<”)
(填“>”、“=”或“<”)(2)在3L容积可变的密闭容器中发生反应②,c(CO)随反应时间t变化如图中曲线Ⅰ所示。若在t0时刻分别改变一个条件,曲线Ⅰ变为曲线Ⅱ和曲线III。当曲线Ⅰ变为曲线Ⅱ时,改变的条件是

(3)在另一温度下按反应③合成甲醇的反应,如图关闭K,向A容器中充入1molCO2和4molH2,向B容器中充入1.2molCO2和4.8molH2,两容器分别发生上述反应。已知起始时容器A和B的体积均为aL,反应达到平衡时容器B的体积为0.9aL,维持其他条件不变,若打开K一段时间后重新达到平衡,容器B的体积为

您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐1】在2 L密闭容器内,800℃时反应:2NO(g)+O2(g) 2NO2(g)体系中,n(NO)随时间的变化如下表:
2NO2(g)体系中,n(NO)随时间的变化如下表:
800℃,反应达到平衡时,NO的物质的量浓度是____________ ;升高温度,NO的浓度增大,则该反应是____________ (填“放热”或“吸热”)反应。
 2NO2(g)体系中,n(NO)随时间的变化如下表:
2NO2(g)体系中,n(NO)随时间的变化如下表:| 时间/s | 0 | 1 | 2 | 3 | 4 |
| n(NO)/mol | 0.020 | 0.01 | 0.008 | 0.007 | 0.007 |
800℃,反应达到平衡时,NO的物质的量浓度是
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐2】在100℃时,将0.1mol的四氧化二氮气体充入1 L抽空的密闭容器中,发生反应,隔一定时间对该容器内的物质进行分析,得到如下数据:

(1)该反应的化学方程式为______________________ ,表中c2_____ c3_____ a______ b(选填“>”、“<”、“==”)。
(2)20 s时四氧化二氮的浓度c1=____________ mol·l—1依据图象可以判断该反应的 ΔH___ 0(填“>”或“<”)
| 浓度 时间(S) | 0 | 20 | 40 | 60 | 80 | 100 |
| c(N2O4)/mol·L—1 | 0.1 | c1 | 0.05 | c3 | a | b |
| c(NO2)/mol·L—1 | 0 | 0.06 | c2 | 0.12 | 0.12 | 0.12 |

(1)该反应的化学方程式为
(2)20 s时四氧化二氮的浓度c1=
您最近半年使用:0次

 2C(g)+xD(g),达到平衡时,生成了2molC,经测定,D的浓度为0.5mol·L-1,试计算:(写出简单的计算过程)
2C(g)+xD(g),达到平衡时,生成了2molC,经测定,D的浓度为0.5mol·L-1,试计算:(写出简单的计算过程)

