合成氨的捷姆金和佩热夫速率方程式为γ=k1p(N2)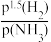 -k2
-k2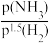 ,γ为反应的瞬时总速率,为正反应和逆反应速率之差,k1、k2是正、逆反应速率常数。合成氨反应N2+3H2
,γ为反应的瞬时总速率,为正反应和逆反应速率之差,k1、k2是正、逆反应速率常数。合成氨反应N2+3H2 2NH3的平衡常数Kp=
2NH3的平衡常数Kp=_____ (用k1,k2表示)(注:Kp用各物质平衡分压来表示)。
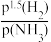 -k2
-k2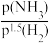 ,γ为反应的瞬时总速率,为正反应和逆反应速率之差,k1、k2是正、逆反应速率常数。合成氨反应N2+3H2
,γ为反应的瞬时总速率,为正反应和逆反应速率之差,k1、k2是正、逆反应速率常数。合成氨反应N2+3H2 2NH3的平衡常数Kp=
2NH3的平衡常数Kp=
2023高三·全国·专题练习 查看更多[1]
(已下线)专题18 速率方程及其应用-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)
更新时间:2023-02-01 19:33:18
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】化学平衡常数:在一定温度下,当一个可逆反应达到化学平衡时,生成物___________ 与反应物___________ 的比值是一个常数,用符号___________ 表示。
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】温度为 ,在三个容积均为
,在三个容积均为 的恒容密闭容器中仅发生反应
的恒容密闭容器中仅发生反应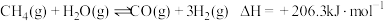 ,该反应中,正反应速率为
,该反应中,正反应速率为 ,逆反应速率为
,逆反应速率为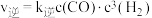 ,
, 、
、 为速率常数,受温度影响。已知
为速率常数,受温度影响。已知 时,
时, ,则该温度下,平衡常数
,则该温度下,平衡常数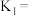
_______ ;当温度改变为 时,若
时,若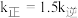 ,则
,则
_______ (填“>”“=”或“<”) 。
。
 ,在三个容积均为
,在三个容积均为 的恒容密闭容器中仅发生反应
的恒容密闭容器中仅发生反应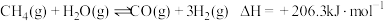 ,该反应中,正反应速率为
,该反应中,正反应速率为 ,逆反应速率为
,逆反应速率为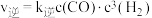 ,
, 、
、 为速率常数,受温度影响。已知
为速率常数,受温度影响。已知 时,
时, ,则该温度下,平衡常数
,则该温度下,平衡常数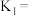
 时,若
时,若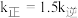 ,则
,则
 。
。
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】工业合成氨的反应为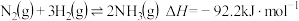 ,其部分工艺流程如图所示。
,其部分工艺流程如图所示。

反应体系中各组分的部分性质如表所示。
回答下列问题:
(1)该反应的化学平衡常数表达式K=_________ 。随着温度升高,K值________ (填“增大”“减小”或“不变”)。
(2)合成氨反应的平衡常数很小,所以在工业上将气体循环利用,即反应后通过把混合气体的温度降低到_________ ,将________ 分离出来;继续循环利用的气体是_________ 。
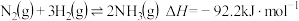 ,其部分工艺流程如图所示。
,其部分工艺流程如图所示。
反应体系中各组分的部分性质如表所示。
| 气体 |  |  |  |
| 熔点/℃ | 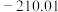 |  | 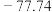 |
| 沸点/℃ | 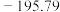 | 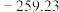 | 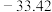 |
(1)该反应的化学平衡常数表达式K=
(2)合成氨反应的平衡常数很小,所以在工业上将气体循环利用,即反应后通过把混合气体的温度降低到
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】回答下列问题:
(1)某温度下在容积为2L密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图。
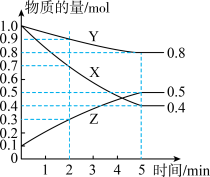
①该反应的化学方程式是_______ 。
②4min时,υ正_______ υ逆(填“>”“<”或“=")。
③若上述反应分别在甲、乙、丙三个相同的密闭容器中进行,经相同时间后,测得三个容器中的反应速率分别为甲:υ(X)=0.3mol·L-1·s-1,乙:υ(Y)=0.12mol·L-1·s-1,丙:υ(Z)=9.6mol·L-1·min-1.则甲、乙、丙三个容器中反应速率由快到慢的顺序为_______ 。
④下列措施能增大该反应速率的是_______ (选填字母)
A.升高温度 B.恒容条件下充入Ar气
C.减小Z的浓度 D.将反应容器体积缩小
(2)反应2NO(g)+O2(g)⇌2NO2(g),在一定温度下 密闭容器内,能说明该反应已经达到化学平衡状态的是
密闭容器内,能说明该反应已经达到化学平衡状态的是_______ 。
a.2υ逆(NO)=υ正(O2)
b.容器内压强保持不变
c.υ(NO2)=2υ(O2)
d.容器内的密度保持不变
e.容器内混合气体平均相对分子质量不变
f.c(NO):c(O2):c(NO2)=2:1:2
g.容器内气体颜色不变
(3)常见的烟道气中除去SO2的方法之一:2CO(g)+SO2(g)⇌2CO2(g)+S(l) (ΔH<0),该反应的平衡常数表达式为_______ 。若在2L的密闭容器中进行上述反应,经测定在5min内气体的质量减少了1.6g,则0~5min的平均反应速率υ(SO2)=_______ 。
(1)某温度下在容积为2L密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图。

①该反应的化学方程式是
②4min时,υ正
③若上述反应分别在甲、乙、丙三个相同的密闭容器中进行,经相同时间后,测得三个容器中的反应速率分别为甲:υ(X)=0.3mol·L-1·s-1,乙:υ(Y)=0.12mol·L-1·s-1,丙:υ(Z)=9.6mol·L-1·min-1.则甲、乙、丙三个容器中反应速率由快到慢的顺序为
④下列措施能增大该反应速率的是
A.升高温度 B.恒容条件下充入Ar气
C.减小Z的浓度 D.将反应容器体积缩小
(2)反应2NO(g)+O2(g)⇌2NO2(g),在一定温度下
 密闭容器内,能说明该反应已经达到化学平衡状态的是
密闭容器内,能说明该反应已经达到化学平衡状态的是a.2υ逆(NO)=υ正(O2)
b.容器内压强保持不变
c.υ(NO2)=2υ(O2)
d.容器内的密度保持不变
e.容器内混合气体平均相对分子质量不变
f.c(NO):c(O2):c(NO2)=2:1:2
g.容器内气体颜色不变
(3)常见的烟道气中除去SO2的方法之一:2CO(g)+SO2(g)⇌2CO2(g)+S(l) (ΔH<0),该反应的平衡常数表达式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】高炉炼铁中发生的反应有:FeO(s) + CO(g)=Fe(s) + CO2(g) △H < 0
(1)该反应的平衡常数表达式K=_______ 。
(2)已知1100℃时,K=0.263温度升高,平衡常数K_______ (增大,减少或不变)。
(3)1100℃时,测得高炉中c(CO2)=0.025mol/L,c(CO)=0.1mol/L,在这种情况下该反应是否处于平衡状态_______ (填是或否),此时反应速率是v正_______ v逆(填>,<,=)。
(1)该反应的平衡常数表达式K=
(2)已知1100℃时,K=0.263温度升高,平衡常数K
(3)1100℃时,测得高炉中c(CO2)=0.025mol/L,c(CO)=0.1mol/L,在这种情况下该反应是否处于平衡状态
您最近一年使用:0次
【推荐3】在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)⇌CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
回答下列问题:
(1)该反应的化学平衡常数表达式为K=___________ 。
(2)能判断该反应是否达到化学平衡状态的依据是___________
(3)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为____ ℃。
| t℃ | 700 | 800 | 830 | 1000 |
| K | 0.6 | 0.9 | 1.0 | 1.7 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K=
(2)能判断该反应是否达到化学平衡状态的依据是
a.容器中压强不变 b.混合气体中c(CO)不变
c. 正(H2)=
正(H2)= 逆(H2O) d.c(CO2)=c(CO)
逆(H2O) d.c(CO2)=c(CO)
(3)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】300℃时,将2 molA和2 molB两种气体混合于2 L密闭容器中,发生如下反应:3A(g)+B(g)  2C(g)+2D(s) △H=Q,4 min未达到平衡,生成0.8 molD。
2C(g)+2D(s) △H=Q,4 min未达到平衡,生成0.8 molD。
(1)300℃时,该反应的平衡常数表达式为:K=_______ 。已知K300℃<K350℃,则△H_______ 0(填“>”“=”或“<”)。
(2)在4 min末时,B的平衡浓度为_______ ,C的平均反应速率为_______ ,A的转化率为_______ 。
(3)若温度不变,缩小容器容积,则A的转化率_______ (填“增大”、“减小”或“不变”),原因是_______ 。
(4)4 min末若保持容器容积不变,再向其中充入1 mol He,B的反应速率会_______ (填“加快” “减慢” 或“不变”)。
(5)温度对此反应的正、逆反应速率影响的曲线(如图所示)中,正确的是_______ 。
A. B.
B. 
C. D.
D.
(6)300℃时,在2 L的该反应容器中进行上述反应,一段时间后,测得A、B、C、D物质的量分别为2 mol、1 mol、2 mol、2 mol,则此时反应υ(A)正_______ υ(A)逆(填 “>”、“<”“=”或“不能确定”)。
 2C(g)+2D(s) △H=Q,4 min未达到平衡,生成0.8 molD。
2C(g)+2D(s) △H=Q,4 min未达到平衡,生成0.8 molD。(1)300℃时,该反应的平衡常数表达式为:K=
(2)在4 min末时,B的平衡浓度为
(3)若温度不变,缩小容器容积,则A的转化率
(4)4 min末若保持容器容积不变,再向其中充入1 mol He,B的反应速率会
(5)温度对此反应的正、逆反应速率影响的曲线(如图所示)中,正确的是
A.
 B.
B. 
C.
 D.
D.
(6)300℃时,在2 L的该反应容器中进行上述反应,一段时间后,测得A、B、C、D物质的量分别为2 mol、1 mol、2 mol、2 mol,则此时反应υ(A)正
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】(1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示___________ ,K值大小与温度的关系是:温度升高,K值_________ (填一定增大、一定减小、或可能增大也可能减小)。
(2)对于可逆反应CO(g) +H2O(g) CO2(g)+H2(g) △H<0在850℃时,KC=1 该反应的平衡常数K的表达式为K=
CO2(g)+H2(g) △H<0在850℃时,KC=1 该反应的平衡常数K的表达式为K=______ ;若温度为900℃,达到平衡后KC_____ 1 (填“>“<”=)
(2)对于可逆反应CO(g) +H2O(g)
 CO2(g)+H2(g) △H<0在850℃时,KC=1 该反应的平衡常数K的表达式为K=
CO2(g)+H2(g) △H<0在850℃时,KC=1 该反应的平衡常数K的表达式为K=
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】合成氨工业在国民经济中占有重要地位。N2(g)+3H2(g) 2NH3(g),∆H<0是合成氨工业的重要反应。在一定温度下,向容积为1L的密闭容器中充入0.5molN2和1.3molH2,反应过程中H2的浓度随时间变化如图所示:
2NH3(g),∆H<0是合成氨工业的重要反应。在一定温度下,向容积为1L的密闭容器中充入0.5molN2和1.3molH2,反应过程中H2的浓度随时间变化如图所示:
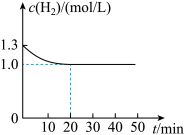
请回答:
(1)20min内,v(N2)=_____ mol/(L·min)。
(2)升高温度,平衡向_____ (填“正”或“逆")反应方向移动。
(3)平衡时,N2的转化率是______ ;
(4)该温度下,合成氨反应的化学平衡常数数值为________ ;
 2NH3(g),∆H<0是合成氨工业的重要反应。在一定温度下,向容积为1L的密闭容器中充入0.5molN2和1.3molH2,反应过程中H2的浓度随时间变化如图所示:
2NH3(g),∆H<0是合成氨工业的重要反应。在一定温度下,向容积为1L的密闭容器中充入0.5molN2和1.3molH2,反应过程中H2的浓度随时间变化如图所示:
请回答:
(1)20min内,v(N2)=
(2)升高温度,平衡向
(3)平衡时,N2的转化率是
(4)该温度下,合成氨反应的化学平衡常数数值为
您最近一年使用:0次



