1 . 已知: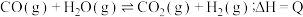 ,其平衡常数随温度变化如下表所示。
,其平衡常数随温度变化如下表所示。
(1)上述反应的化学平衡常数表达式为
___________ 。
(2) 时,向体积为
时,向体积为 反应器中通入一定量的
反应器中通入一定量的 和
和 ,发生上述反应,
,发生上述反应, 和
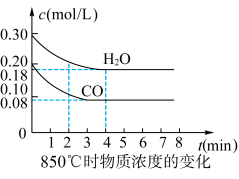
和 浓度变化如图所示,则
浓度变化如图所示,则 时,平均反应速率
时,平均反应速率
___________ 。
(3)若在 时进行,且
时进行,且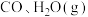 的起始浓度均为
的起始浓度均为 ,该条件下,
,该条件下, 的最大转化率为
的最大转化率为___________
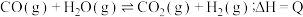 ,其平衡常数随温度变化如下表所示。
,其平衡常数随温度变化如下表所示。温度 | 400 | 500 | 850 |
| 平衡常数 | 9.94 | 9 | 1 |
(1)上述反应的化学平衡常数表达式为

(2)
 时,向体积为
时,向体积为 反应器中通入一定量的
反应器中通入一定量的 和
和 ,发生上述反应,
,发生上述反应, 和
和 浓度变化如图所示,则
浓度变化如图所示,则 时,平均反应速率
时,平均反应速率

(3)若在
 时进行,且
时进行,且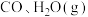 的起始浓度均为
的起始浓度均为 ,该条件下,
,该条件下, 的最大转化率为
的最大转化率为
您最近一年使用:0次
解题方法
2 . 顺1,2二甲基环丙烷和反1,2二甲基环丙烷可发生如下转化:

该反应的速率方程可表示为:v(正)=k(正)·c(顺)和v(逆)=k(逆)·c(反),k(正)和k(逆)在一定温度时为常数,分别称作正、逆反应速率常数。已知:t1温度下,k(正)=0.006 s-1,k(逆)=0.002 s-1,该温度下反应的平衡常数值K=_______ 。

该反应的速率方程可表示为:v(正)=k(正)·c(顺)和v(逆)=k(逆)·c(反),k(正)和k(逆)在一定温度时为常数,分别称作正、逆反应速率常数。已知:t1温度下,k(正)=0.006 s-1,k(逆)=0.002 s-1,该温度下反应的平衡常数值K=
您最近一年使用:0次
解题方法
3 . 一定条件下,将 与
与 以体积比1∶2置于恒温、恒容的密闭容器中,发生反应
以体积比1∶2置于恒温、恒容的密闭容器中,发生反应
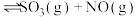 ,测得反应达到平衡时
,测得反应达到平衡时 与
与 的体积比为1∶5,则反应的平衡常数
的体积比为1∶5,则反应的平衡常数
_______ 。
 与
与 以体积比1∶2置于恒温、恒容的密闭容器中,发生反应
以体积比1∶2置于恒温、恒容的密闭容器中,发生反应
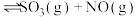 ,测得反应达到平衡时
,测得反应达到平衡时 与
与 的体积比为1∶5,则反应的平衡常数
的体积比为1∶5,则反应的平衡常数
您最近一年使用:0次
解题方法
4 . 将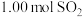 和
和 通入1.00 L的密闭容器中,1000 K时,反应达到平衡,测得平衡时
通入1.00 L的密闭容器中,1000 K时,反应达到平衡,测得平衡时 的物质的量浓度为
的物质的量浓度为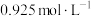 。计算该温度下反应
。计算该温度下反应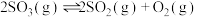 的平衡常数。
的平衡常数。_______
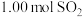 和
和 通入1.00 L的密闭容器中,1000 K时,反应达到平衡,测得平衡时
通入1.00 L的密闭容器中,1000 K时,反应达到平衡,测得平衡时 的物质的量浓度为
的物质的量浓度为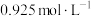 。计算该温度下反应
。计算该温度下反应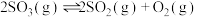 的平衡常数。
的平衡常数。
您最近一年使用:0次
5 . 一定温度下,在10L密闭容器中加入5molSO2和3molO2,发生反应:2SO2(g)+O2(g) 2SO3(g),10min时,反应达到平衡状态,此时有3molSO2发生了反应。
2SO3(g),10min时,反应达到平衡状态,此时有3molSO2发生了反应。
(1)反应生成了____ molSO3,v(SO2)=____ 。
(2)平衡时SO3的浓度是____ ,SO2的转化率是____ 。
(3)平衡时容器内气体的总物质的量为___ mol。
(4)物质的浓度不再改变标志着该反应已达平衡,下列还可以说明该反应已达平衡的是___ (填序号)。
①体系内压强不再改变
②容器内气体的密度不再改变
③混合气体的平均相对分子质量不再改变
④v正(SO3)=2v逆(O2)
⑤n(SO3):n(O2):n(SO2)=2:1:2
(5)该温度下,SO3(g) SO2(g)+
SO2(g)+ O2(g)的平衡常数K=
O2(g)的平衡常数K=___ 。
 2SO3(g),10min时,反应达到平衡状态,此时有3molSO2发生了反应。
2SO3(g),10min时,反应达到平衡状态,此时有3molSO2发生了反应。(1)反应生成了
(2)平衡时SO3的浓度是
(3)平衡时容器内气体的总物质的量为
(4)物质的浓度不再改变标志着该反应已达平衡,下列还可以说明该反应已达平衡的是
①体系内压强不再改变
②容器内气体的密度不再改变
③混合气体的平均相对分子质量不再改变
④v正(SO3)=2v逆(O2)
⑤n(SO3):n(O2):n(SO2)=2:1:2
(5)该温度下,SO3(g)
 SO2(g)+
SO2(g)+ O2(g)的平衡常数K=
O2(g)的平衡常数K=
您最近一年使用:0次
2022-04-11更新
|
532次组卷
|
2卷引用:广东省揭阳华侨高级中学2021-2022学年高二上学期第一次阶段考试化学试题
解题方法
6 . 在密闭容器中将NO2加热到某温度时,进行如下的反应:2NO2 2NO+O2,反应5分钟后达平衡,测得平衡时各组分的浓度分别为:c(NO2)=0.06 mol/L,c(NO)=0.24 mol/L。
2NO+O2,反应5分钟后达平衡,测得平衡时各组分的浓度分别为:c(NO2)=0.06 mol/L,c(NO)=0.24 mol/L。
列式计算:
(1)NO2的转化率为多少?_______
(2)该温度下反应的平衡常数。_______
(3)在这5分钟内,用O2来表示的平均反应速率是多少?_______
 2NO+O2,反应5分钟后达平衡,测得平衡时各组分的浓度分别为:c(NO2)=0.06 mol/L,c(NO)=0.24 mol/L。
2NO+O2,反应5分钟后达平衡,测得平衡时各组分的浓度分别为:c(NO2)=0.06 mol/L,c(NO)=0.24 mol/L。列式计算:
(1)NO2的转化率为多少?
(2)该温度下反应的平衡常数。
(3)在这5分钟内,用O2来表示的平均反应速率是多少?
您最近一年使用:0次
7 . 利用I2O5可消除CO污染,其反应为:I2O5(s)+5CO(g) 5CO2(g)+I2(s)。在不同温度下,向装有足量I2O5固体的2L恒容密闭容器中通入2molCO,测得CO2气体的体积分数φ(CO2)随时间t的变化曲线如图所示。
5CO2(g)+I2(s)。在不同温度下,向装有足量I2O5固体的2L恒容密闭容器中通入2molCO,测得CO2气体的体积分数φ(CO2)随时间t的变化曲线如图所示。
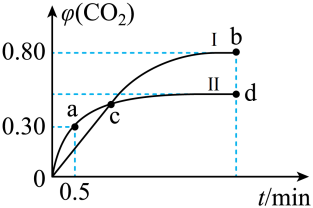
(1)曲线Ⅱ0~0.5min内的平均反应速率v(CO)═___________ 。
(2)b点时,CO的转化率为___________ 。
(3)b点和d点的化学平衡常数:Kb___________ Kd(填“>”、“<”或“═”)。
 5CO2(g)+I2(s)。在不同温度下,向装有足量I2O5固体的2L恒容密闭容器中通入2molCO,测得CO2气体的体积分数φ(CO2)随时间t的变化曲线如图所示。
5CO2(g)+I2(s)。在不同温度下,向装有足量I2O5固体的2L恒容密闭容器中通入2molCO,测得CO2气体的体积分数φ(CO2)随时间t的变化曲线如图所示。
(1)曲线Ⅱ0~0.5min内的平均反应速率v(CO)═
(2)b点时,CO的转化率为
(3)b点和d点的化学平衡常数:Kb
您最近一年使用:0次
解题方法
8 . 工业合成氨反应为:N2(g)+3H2(g) 2 NH3(g),在773K时分别将2 mol N2和6 mol H2充入一个固定容积为1 L的密闭容器中,随着反应的进行,气体混合物中n(H2)、n(NH3)与反应时间t的关系如下表:
2 NH3(g),在773K时分别将2 mol N2和6 mol H2充入一个固定容积为1 L的密闭容器中,随着反应的进行,气体混合物中n(H2)、n(NH3)与反应时间t的关系如下表:
计算:
(1)前10分钟内平均反应速率v(N2)=______ 。
(2)该温度下此反应的平衡常数K=_____ 。
(3)该温度下,若向同容积的另一容器中投入的N2、H2、NH3浓度分别为3mol·L-1、3mol·L-1、3mol·L-1,通过计算判断此时v正和v逆相对大小____ 。
 2 NH3(g),在773K时分别将2 mol N2和6 mol H2充入一个固定容积为1 L的密闭容器中,随着反应的进行,气体混合物中n(H2)、n(NH3)与反应时间t的关系如下表:
2 NH3(g),在773K时分别将2 mol N2和6 mol H2充入一个固定容积为1 L的密闭容器中,随着反应的进行,气体混合物中n(H2)、n(NH3)与反应时间t的关系如下表:| t/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| n(H2)/mol | 6.00 | 4.50 | 3.60 | 3.30 | 3.03 | 3.00 | 3.00 |
| n(NH3)/mol | 0 | 1.00 | 1.60 | 1.80 | 1.98 | 2.00 | 2.00 |
计算:
(1)前10分钟内平均反应速率v(N2)=
(2)该温度下此反应的平衡常数K=
(3)该温度下,若向同容积的另一容器中投入的N2、H2、NH3浓度分别为3mol·L-1、3mol·L-1、3mol·L-1,通过计算判断此时v正和v逆相对大小
您最近一年使用:0次
名校
解题方法
9 . (1)一定温度下,在密闭容器中通入一定量的NO2,发生反应:2NO2(g) 2NO(g)+O2(g),达到化学平衡时,测得混合气中NO2浓度为0.06mol·L-1,O2的浓度为0.12mol·L-1。
2NO(g)+O2(g),达到化学平衡时,测得混合气中NO2浓度为0.06mol·L-1,O2的浓度为0.12mol·L-1。
则:①该可逆反应的平衡常数K=___ (请用数字计算式表达)。
②此时NO2的转化率____ 。
(2)在容积为2L的密闭容器中进行如下反应:A(g)+2B(g) 3C(g)+nD(g),开始时A为4mol,B为6mol,5min末时测得C的物质的量为3mol,用D表示的化学反应速率v(D)为0.2mol/(L·min)。
3C(g)+nD(g),开始时A为4mol,B为6mol,5min末时测得C的物质的量为3mol,用D表示的化学反应速率v(D)为0.2mol/(L·min)。
计算:①5min末A的物质的量浓度为___ ;
②前5min内用B表示的化学反应速率v(B)为___ ;
③化学方程式中n值为___ 。
 2NO(g)+O2(g),达到化学平衡时,测得混合气中NO2浓度为0.06mol·L-1,O2的浓度为0.12mol·L-1。
2NO(g)+O2(g),达到化学平衡时,测得混合气中NO2浓度为0.06mol·L-1,O2的浓度为0.12mol·L-1。则:①该可逆反应的平衡常数K=
②此时NO2的转化率
(2)在容积为2L的密闭容器中进行如下反应:A(g)+2B(g)
 3C(g)+nD(g),开始时A为4mol,B为6mol,5min末时测得C的物质的量为3mol,用D表示的化学反应速率v(D)为0.2mol/(L·min)。
3C(g)+nD(g),开始时A为4mol,B为6mol,5min末时测得C的物质的量为3mol,用D表示的化学反应速率v(D)为0.2mol/(L·min)。计算:①5min末A的物质的量浓度为
②前5min内用B表示的化学反应速率v(B)为
③化学方程式中n值为
您最近一年使用:0次
解题方法
10 . 在一个容积为500ml的密闭容器中,充入10molH2和4molCO。在一定温度和一定压强下,发生如下反应:2H2(g)+CO(g) CH3OH(g),经过5分钟后达到平衡状态。若此时测得CH3OH蒸气的浓度为2mol/L,求:
CH3OH(g),经过5分钟后达到平衡状态。若此时测得CH3OH蒸气的浓度为2mol/L,求:
(1)以H2的浓度变化表示该反应的速率______________ ;
(2)达到平衡时CO的转化率______________ ;
(3)该温度下的K______________ 。
 CH3OH(g),经过5分钟后达到平衡状态。若此时测得CH3OH蒸气的浓度为2mol/L,求:
CH3OH(g),经过5分钟后达到平衡状态。若此时测得CH3OH蒸气的浓度为2mol/L,求:(1)以H2的浓度变化表示该反应的速率
(2)达到平衡时CO的转化率
(3)该温度下的K
您最近一年使用:0次



