名校
解题方法
1 . 甲烷、水蒸气催化重整是工业制备氢气的方法之一,其反应为 。在压强为p和不同温度下,平衡体系中氢气的体积分数与甲烷、水蒸气的投料比[用
。在压强为p和不同温度下,平衡体系中氢气的体积分数与甲烷、水蒸气的投料比[用 表示]的变化关系如图所示。
表示]的变化关系如图所示。 。
。
下列说法错误的是
 。在压强为p和不同温度下,平衡体系中氢气的体积分数与甲烷、水蒸气的投料比[用
。在压强为p和不同温度下,平衡体系中氢气的体积分数与甲烷、水蒸气的投料比[用 表示]的变化关系如图所示。
表示]的变化关系如图所示。
 。
。下列说法错误的是
| A.该反应中正反应的活化能大于逆反应的活化能 |
B.向平衡体系中加入适量的 ,可提高氢气的产率 ,可提高氢气的产率 |
C.M点甲烷的平衡转化率为 |
D.在压强为p和600℃时,若向反应器中充入 和 和 ,平衡时氢气的体积分数小于 ,平衡时氢气的体积分数小于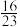 |
您最近一年使用:0次
解题方法
2 . CO、CO2的回收与利用是科学家研究的热点课题,可利用CO、CO2制备甲烷、甲醇、二甲醚等。
(1)CO2加氢制备甲烷:CO2(g)+4H2(g)=CH4(g)+2H2O(g) ΔH=-164.7kJ•mol-1。已知ΔH=ΔfH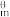 (生成物)- ΔfH
(生成物)- ΔfH (反应物),298K时,几种气态物质的标准摩尔生成焓如表:
(反应物),298K时,几种气态物质的标准摩尔生成焓如表:
则x=_______ 。
(2)H2和CO合成甲烷的反应为2CO(g)+2H2(g) CH4(g)+CO2(g)。T℃时,将等物质的量的CO和H2充入恒压(200kPa)的密闭容器中。已知v逆=K逆•p(CH4)•p(CO2),其中p为分压,该温度下K逆=5.0×10-4。反应达平衡时测得v正=
CH4(g)+CO2(g)。T℃时,将等物质的量的CO和H2充入恒压(200kPa)的密闭容器中。已知v逆=K逆•p(CH4)•p(CO2),其中p为分压,该温度下K逆=5.0×10-4。反应达平衡时测得v正= kPa•s-1,则该温度下反应的Kp=
kPa•s-1,则该温度下反应的Kp=_______ (用组分的分压计算的平衡常数)。
(3)二氧化碳催化加氢制甲醇:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH<0,反应在起始物
CH3OH(g)+H2O(g) ΔH<0,反应在起始物 =3时,不同条件下达到平衡,体系中甲醇的物质的量分数为x(CH3OH),在t=250℃下的x(CH3OH)~p、在p=5×105Pa下的x(CH3OH)~t如图。
=3时,不同条件下达到平衡,体系中甲醇的物质的量分数为x(CH3OH),在t=250℃下的x(CH3OH)~p、在p=5×105Pa下的x(CH3OH)~t如图。
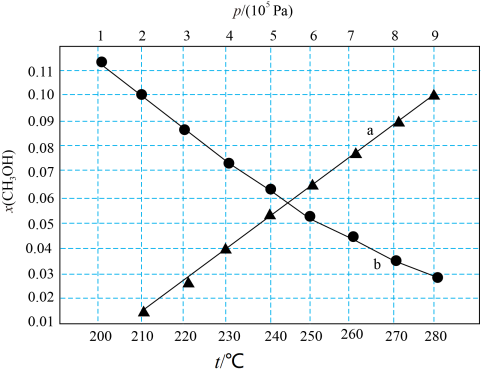
①图中对应等温过程的曲线是_______ 。
②当x(CH3OH)=0.10时,CO2的平衡转化率约为_______ 。
③当x(CH3OH)=0.10时,反应条件可能为_______ 或_______ 。
(4)甲醇脱水制得二甲醚的反应为2CH3OH(g) CH3OCH3(g)+H2O(g),当T=500K时,反应平衡常数Kc≈9,在密闭容器中加入一定量CH3OH,反应到达平衡状态时,体系中CH3OCH3(g)的物质的量分数
CH3OCH3(g)+H2O(g),当T=500K时,反应平衡常数Kc≈9,在密闭容器中加入一定量CH3OH,反应到达平衡状态时,体系中CH3OCH3(g)的物质的量分数_______ (填字母)。
a.< b.=
b.= c.>
c.> d.无法确定
d.无法确定
(1)CO2加氢制备甲烷:CO2(g)+4H2(g)=CH4(g)+2H2O(g) ΔH=-164.7kJ•mol-1。已知ΔH=ΔfH
 (生成物)- ΔfH
(生成物)- ΔfH (反应物),298K时,几种气态物质的标准摩尔生成焓如表:
(反应物),298K时,几种气态物质的标准摩尔生成焓如表:| 物质 | CO2(g) | H2O(g) | CH4(g) | H2(g) |
ΔfH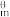 /(kJ•mol-1) /(kJ•mol-1) | -393.5 | -241.8 | x | 0 |
(2)H2和CO合成甲烷的反应为2CO(g)+2H2(g)
 CH4(g)+CO2(g)。T℃时,将等物质的量的CO和H2充入恒压(200kPa)的密闭容器中。已知v逆=K逆•p(CH4)•p(CO2),其中p为分压,该温度下K逆=5.0×10-4。反应达平衡时测得v正=
CH4(g)+CO2(g)。T℃时,将等物质的量的CO和H2充入恒压(200kPa)的密闭容器中。已知v逆=K逆•p(CH4)•p(CO2),其中p为分压,该温度下K逆=5.0×10-4。反应达平衡时测得v正= kPa•s-1,则该温度下反应的Kp=
kPa•s-1,则该温度下反应的Kp=(3)二氧化碳催化加氢制甲醇:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH<0,反应在起始物
CH3OH(g)+H2O(g) ΔH<0,反应在起始物 =3时,不同条件下达到平衡,体系中甲醇的物质的量分数为x(CH3OH),在t=250℃下的x(CH3OH)~p、在p=5×105Pa下的x(CH3OH)~t如图。
=3时,不同条件下达到平衡,体系中甲醇的物质的量分数为x(CH3OH),在t=250℃下的x(CH3OH)~p、在p=5×105Pa下的x(CH3OH)~t如图。
①图中对应等温过程的曲线是
②当x(CH3OH)=0.10时,CO2的平衡转化率约为
③当x(CH3OH)=0.10时,反应条件可能为
(4)甲醇脱水制得二甲醚的反应为2CH3OH(g)
 CH3OCH3(g)+H2O(g),当T=500K时,反应平衡常数Kc≈9,在密闭容器中加入一定量CH3OH,反应到达平衡状态时,体系中CH3OCH3(g)的物质的量分数
CH3OCH3(g)+H2O(g),当T=500K时,反应平衡常数Kc≈9,在密闭容器中加入一定量CH3OH,反应到达平衡状态时,体系中CH3OCH3(g)的物质的量分数a.<
 b.=
b.= c.>
c.> d.无法确定
d.无法确定
您最近一年使用:0次
3 . 甲醇是重要的工业原料,应用前景广阔。甲醇可由二氧化碳与氢气合成,恒容密闭容器内发生反应如下: 。研究温度对甲醇产率的影响如图所示,下列说法正确的是
。研究温度对甲醇产率的影响如图所示,下列说法正确的是

 。研究温度对甲醇产率的影响如图所示,下列说法正确的是
。研究温度对甲醇产率的影响如图所示,下列说法正确的是
| A.平衡后向体系内加入CO2,平衡正向移动,CO2的转化率增大 |
| B.正反应放热 |
| C.使用催化剂能提高甲醇的产率 |
| D.缩小体积,增大压强,平衡正向移动,平衡常数增大 |
您最近一年使用:0次
名校
4 . 已知在密闭容器中进行可逆反应: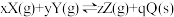
 ,下列对有关该反应的图象判断正确的是
,下列对有关该反应的图象判断正确的是
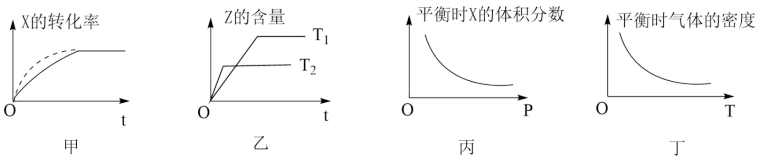
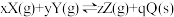
 ,下列对有关该反应的图象判断正确的是
,下列对有关该反应的图象判断正确的是
| A.甲中虚线表示使用了合适的催化剂 |
B.由乙可判断温度: , , |
C.由丙可推知: |
D.由丁可推出: |
您最近一年使用:0次
2022-01-02更新
|
364次组卷
|
2卷引用:甘肃省武威市民勤县第一中学2023-2024学高二下学期开学考试化学试题
名校
解题方法
5 . 下列叙述与图像相符的是
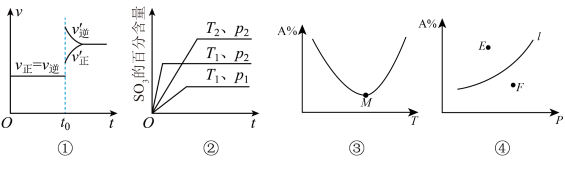

A.图①表示反应2SO2(g)+O2(g) 2SO3(g)达到平衡后在t0时刻充入了一定量的SO3 2SO3(g)达到平衡后在t0时刻充入了一定量的SO3 |
B.图②可满足反应2SO2(g)+O2(g) 2SO3(g) ΔH<0 2SO3(g) ΔH<0 |
C.图③表示反应aA(g)+bB(g) cC(g),在容器中充入1molA和1molB,经过相同时间容器中A的百分含量随温度的变化,可知反应ΔH>0 cC(g),在容器中充入1molA和1molB,经过相同时间容器中A的百分含量随温度的变化,可知反应ΔH>0 |
D.图④表示反应aA(g)+bB(g) cC(g)平衡时A的百分含量随压强的变化,可知E点v(逆)>v(正) cC(g)平衡时A的百分含量随压强的变化,可知E点v(逆)>v(正) |
您最近一年使用:0次
2021-11-23更新
|
840次组卷
|
9卷引用:甘肃省张掖市2022-2023学年高二下学期第一次全市联考化学试题
甘肃省张掖市2022-2023学年高二下学期第一次全市联考化学试题浙江省杭州地区(含周边)重点中学2021-2022学年高二上学期期中联考化学试题浙江省金华第一中学2021-2022学年高一上学期领军班期末联考化学试题(已下线)专题24 化学平衡图像题的突破-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)浙江省金华一中(领军班)2021-2022学年高一上学期期末化学试题北京市第五十五中学2021-2022学年高二上学期期中考试化学试题北京市第五十五中学2022-2023学年高二上学期期中考试化学试题河南省兰考县第二高级中学2021-2022学年高二上学期第三次考试化学试题北京市第一○一中学2023-2024学年高二上学期期中练习化学试题



