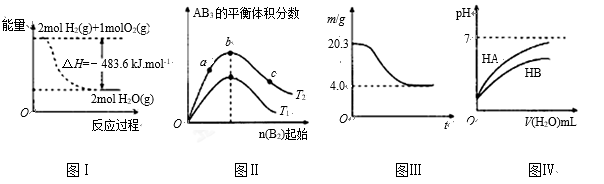
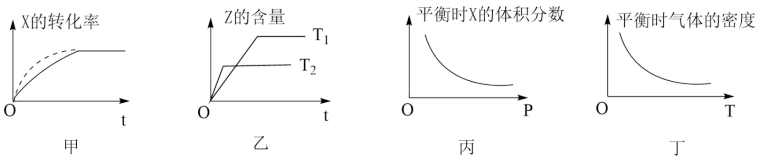
已知在密闭容器中进行可逆反应: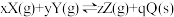
 ,下列对有关该反应的图象判断正确的是
,下列对有关该反应的图象判断正确的是
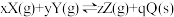
 ,下列对有关该反应的图象判断正确的是
,下列对有关该反应的图象判断正确的是
| A.甲中虚线表示使用了合适的催化剂 |
B.由乙可判断温度: , , |
C.由丙可推知: |
D.由丁可推出: |
更新时间:2022-01-02 19:57:42
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列现象或操作不适宜用勒夏特列原理解释的是
| A.实验室可用CaO和浓氨水快速制取氨气 |
| B.FeCl3溶液中加Fe粉,颜色由棕黄色变为浅绿色 |
| C.新制氯水放置一段时间颜色变浅 |
| D.锅炉水垢中含有CaSO4,常先加Na2CO3再加酸处理 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列事实不能 用勒夏特列原理解释的是
①由H2(g)、I2(g)、HI(g)组成的平衡体系,加压后颜色变深
②对新制氯水进行光照后,溶液的pH逐渐减小
③加催化剂,使N2和H2在一定条件下更快转化为NH3
④在含有Fe(SCN)3的红色溶液中加铁粉,振荡静置,溶液颜色变浅或褪去
⑤实验室制取CO2时,粉碎大理石有利于CO2的生成
⑥向含有酚酞的氨水中加入氯化铵固体后,溶液红色变浅
①由H2(g)、I2(g)、HI(g)组成的平衡体系,加压后颜色变深
②对新制氯水进行光照后,溶液的pH逐渐减小
③加催化剂,使N2和H2在一定条件下更快转化为NH3
④在含有Fe(SCN)3的红色溶液中加铁粉,振荡静置,溶液颜色变浅或褪去
⑤实验室制取CO2时,粉碎大理石有利于CO2的生成
⑥向含有酚酞的氨水中加入氯化铵固体后,溶液红色变浅
| A.①②③ | B.②④⑥ | C.①③⑤ | D.③④⑤ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】纳米级材料Cu2O有非常优良的催化性能。工业上在高温条件下用炭粉还原CuO制得: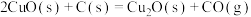
 。下列说法正确的是
。下列说法正确的是
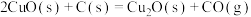
 。下列说法正确的是
。下列说法正确的是| A.该反应在任何温度下均可自发进行 |
| B.该反应的平衡常数K=c(CO) |
| C.其他条件相同,加入更多的炭粉,可以提高CuO的平衡转化率 |
| D.反应中生成22.4L,转移的电子数目为2×6.02×1023 |
您最近一年使用:0次
【推荐1】根据下列图示所得出的结论正确的是
A.下图是在不同温度下三个恒容容器中反应2H2(g)+CO(g)⇌CH3OH(g) △H<0的平衡曲线,曲线X对应的温度相对较高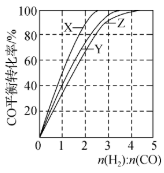 |
B.下图是一定温度下三种碳酸盐MCO3(M:Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线,a点可表示MgCO3的过饱和溶液,且c(Mg2+)>c(CO32-)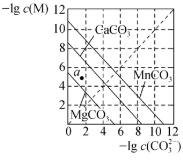 |
C.下图为MOH和ROH两种一元碱水溶液在常温下分别加水稀释时pH值的变化曲线,可知ROH是强碱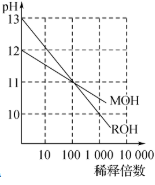 |
D.下图为两个1L容器中各投入1molCH4和1molCO2所发生反应CH4(g)+CO2(g)⇌2CO(g)+2H2(g)的平衡曲线,N点化学平衡常数K=1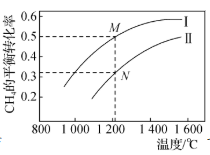 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在2 L的恒容密闭容器中充入2 mol SO2和1 mol O2,发生反应:2SO2(g) + O2(g) 2SO3(g),下列有关说法正确的是( )
2SO3(g),下列有关说法正确的是( )
 2SO3(g),下列有关说法正确的是( )
2SO3(g),下列有关说法正确的是( )A.由图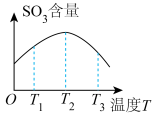 可知:该反应的△H<0 可知:该反应的△H<0 |
B.在图 中的t1时充入少量氩气,容器内压强增大,平衡右移 中的t1时充入少量氩气,容器内压强增大,平衡右移 |
C.图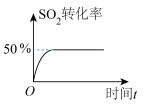 所示条件下,平衡常数为2 所示条件下,平衡常数为2 |
D.图 中的y可以表示平衡常数或混合气体平均摩尔质量 中的y可以表示平衡常数或混合气体平均摩尔质量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
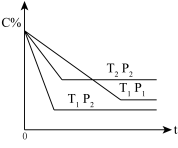
【推荐3】已知某可逆反应:mA(g)+nB(g) xC(g) ΔΗ=Q kJ•mol-1,在密闭容器中进行,表示反应在不同时间t,温度T和压强P与C在混合气体中的百分含量(C%)的关系曲线,则( )
xC(g) ΔΗ=Q kJ•mol-1,在密闭容器中进行,表示反应在不同时间t,温度T和压强P与C在混合气体中的百分含量(C%)的关系曲线,则( )
 xC(g) ΔΗ=Q kJ•mol-1,在密闭容器中进行,表示反应在不同时间t,温度T和压强P与C在混合气体中的百分含量(C%)的关系曲线,则( )
xC(g) ΔΗ=Q kJ•mol-1,在密闭容器中进行,表示反应在不同时间t,温度T和压强P与C在混合气体中的百分含量(C%)的关系曲线,则( )
| A.T1>T2,P1>P2,m+n>x,Q>0 | B.T1<T2,P1<P2,m+n<x,Q>0 |
| C.T1>T2,P1<P2,m+n<x,Q<0 | D.T1<T2,P1<P2,m+n>x,Q<0 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】乙烯的产量是衡量一个国家石油化工发展水平的重要标志。一定条件下CO2和H2合成乙烯的反应为2CO2(g) + 6H2(g) 4H2O(g) + CH2=CH2(g) ΔH= a kJ∙mol-1。向恒容密闭容器中充入体积比为1:3的CO2和H2,测得不同温度下CO2的平衡转化率及催化剂的催化效率如图所示。下列有关说法正确的是
4H2O(g) + CH2=CH2(g) ΔH= a kJ∙mol-1。向恒容密闭容器中充入体积比为1:3的CO2和H2,测得不同温度下CO2的平衡转化率及催化剂的催化效率如图所示。下列有关说法正确的是

 4H2O(g) + CH2=CH2(g) ΔH= a kJ∙mol-1。向恒容密闭容器中充入体积比为1:3的CO2和H2,测得不同温度下CO2的平衡转化率及催化剂的催化效率如图所示。下列有关说法正确的是
4H2O(g) + CH2=CH2(g) ΔH= a kJ∙mol-1。向恒容密闭容器中充入体积比为1:3的CO2和H2,测得不同温度下CO2的平衡转化率及催化剂的催化效率如图所示。下列有关说法正确的是
| A.M点的平衡常数比N点的小 |
| B.温度低于250℃时,乙烯的产率随温度升高而增大 |
| C.保持N点温度不变,向容器中再充入一定量的H2,CO2的转化率可能会增大到50% |
| D.其他条件不变,若不使用催化剂,则250℃时CO2的平衡转化率可能位于M1点 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】在三个恒容密闭容器中按下表相应量充入气体,发生2N2O(g) 2N2(g)+O2(g),容器I、II、III中N2O转化率如图所示:
2N2(g)+O2(g),容器I、II、III中N2O转化率如图所示:
下列说法正确的是
 2N2(g)+O2(g),容器I、II、III中N2O转化率如图所示:
2N2(g)+O2(g),容器I、II、III中N2O转化率如图所示:| 容器 | 容积/L | 起始物质的量/mol | 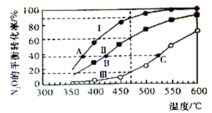 | ||
| N2O | N2 | O2 | |||
| I | V1 | 0.1 | 0 | 0 | |
| II | 1.0 | 0.1 | 0 | 0 | |
| III | V3 | 0.1 | 0 | 0 | |
| A.该反应的正反应为放热反应 |
| B.V1>1.0>V3 |
| C.相同温度下,反应从初始到平衡,平均反应速率:v(I)>v(II) |
| D.图中A、B、C三点处容器内压强:p(I)A>p(II)B>p(III)C |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列图示与对应的叙述相符的是
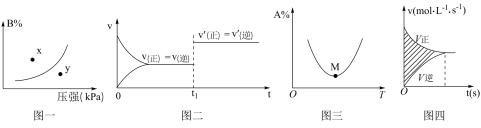

A.图一表示反应:  ,在一定温度下,平衡时B的体积分数(B%)与压强变化的关系如图所示,反应速率x点比y点时的快 ,在一定温度下,平衡时B的体积分数(B%)与压强变化的关系如图所示,反应速率x点比y点时的快 |
B.图二是可逆反应  的速率时间图像,在 的速率时间图像,在 时刻改变条件一定是加入催化剂 时刻改变条件一定是加入催化剂 |
C.图三表示对于化学反应 ,A的百分含量与温度(T)的变化情况,则升高温度,该反应平衡常数增大 ,A的百分含量与温度(T)的变化情况,则升高温度,该反应平衡常数增大 |
D.图四所示图中的阴影部分面积的含义是( ) ) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】可逆反应m A(s)+n B(g) e C(g)+f D(g),反应过程中,当其他条件不变时,C的体积分数φ(C)在不同温度和不同压强的条件下随时间的变化如图所示。下列叙述正确的是
e C(g)+f D(g),反应过程中,当其他条件不变时,C的体积分数φ(C)在不同温度和不同压强的条件下随时间的变化如图所示。下列叙述正确的是
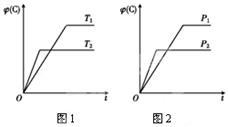
 e C(g)+f D(g),反应过程中,当其他条件不变时,C的体积分数φ(C)在不同温度和不同压强的条件下随时间的变化如图所示。下列叙述正确的是
e C(g)+f D(g),反应过程中,当其他条件不变时,C的体积分数φ(C)在不同温度和不同压强的条件下随时间的变化如图所示。下列叙述正确的是
| A.平衡后,若使用催化剂,C的体积分数将增大 |
| B.平衡后,若温度升高,化学平衡向正反应方向移动 |
| C.平衡后,增加A的质量化学平衡向正反应方向移动 |
| D.化学方程式中,化学计量数的关系为n<e +f |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】某化学研究小组在探究外界条件对mA(g)+nB(g)⇌pC(g)的速率和平衡的影响时,画出了如下图像。下列判断正确的是
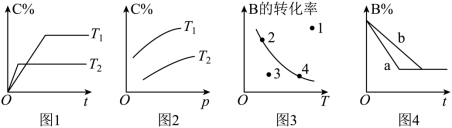

| A.由图1可知,T1<T2,化学平衡常数K(T1)<K(T2) |
| B.由图2可知,m+n<p |
| C.图3中,表示v(正)>v(逆)的是点1 |
| D.图4中,a曲线可能使用了催化剂 |
您最近一年使用:0次