1 . H2还原CO2制CH4的部分反应如下:
Ⅰ: ∆H1=+41 kJ·mol-1
∆H1=+41 kJ·mol-1
Ⅱ: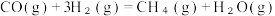 ∆H2=-246 kJ·mol-1
∆H2=-246 kJ·mol-1
控制起始时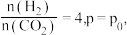 恒容条件下,若只发生反应Ⅰ、Ⅱ,平衡时各物质的物质的量分数随温度的变化如图所示。M 点(380℃)为 CH4曲线和H2曲线的交点。
恒容条件下,若只发生反应Ⅰ、Ⅱ,平衡时各物质的物质的量分数随温度的变化如图所示。M 点(380℃)为 CH4曲线和H2曲线的交点。
Ⅰ:
 ∆H1=+41 kJ·mol-1
∆H1=+41 kJ·mol-1Ⅱ:
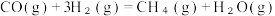 ∆H2=-246 kJ·mol-1
∆H2=-246 kJ·mol-1控制起始时
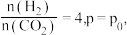 恒容条件下,若只发生反应Ⅰ、Ⅱ,平衡时各物质的物质的量分数随温度的变化如图所示。M 点(380℃)为 CH4曲线和H2曲线的交点。
恒容条件下,若只发生反应Ⅰ、Ⅱ,平衡时各物质的物质的量分数随温度的变化如图所示。M 点(380℃)为 CH4曲线和H2曲线的交点。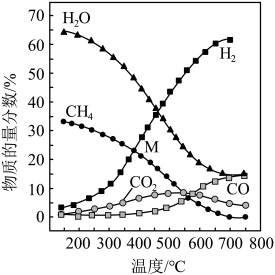
| A.温度低于400℃时,反应Ⅱ几乎完全反应 |
B.300℃时, 若按 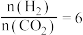 投料,CH4曲线下移 投料,CH4曲线下移 |
C.M点时,平衡分压 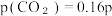 0 0 |
| D.600℃时,当容器内气体总压不变,反应Ⅰ达到平衡状态 |
您最近一年使用:0次
解题方法
2 . 一定温度下,Xe与F2通入恒压容器中发生反应:①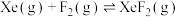
 ,②
,②
 ,③
,③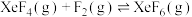
 ,不同投料比
,不同投料比 条件下,平衡时产物(
条件下,平衡时产物( 、
、 、
、 )的物质的量分别如图所示。当
)的物质的量分别如图所示。当 时,认为Xe完全反应。已知a、c对应的
时,认为Xe完全反应。已知a、c对应的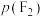 分别为16kPa和225kPa。下列说法正确的是
分别为16kPa和225kPa。下列说法正确的是
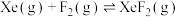
 ,②
,②
 ,③
,③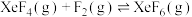
 ,不同投料比
,不同投料比 条件下,平衡时产物(
条件下,平衡时产物( 、
、 、
、 )的物质的量分别如图所示。当
)的物质的量分别如图所示。当 时,认为Xe完全反应。已知a、c对应的
时,认为Xe完全反应。已知a、c对应的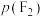 分别为16kPa和225kPa。下列说法正确的是
分别为16kPa和225kPa。下列说法正确的是
A.曲线x代表产物 的物质的量 的物质的量 |
B. |
C.反应 的 的 |
D.当 最多时, 最多时, kPa kPa |
您最近一年使用:0次
3 . 关于反应
 ,下列叙述与图像不相符的是
,下列叙述与图像不相符的是

 ,下列叙述与图像不相符的是
,下列叙述与图像不相符的是
| A.图1表示不同温度下,反应相同时间时A的百分含量,可知M点该反应处于平衡状态 |
B.图2表示反应在一定温度下B的平衡转化率 与压强变化的关系,则x点是非平衡状态,且x点体系中B的百分含量有增大的趋势 与压强变化的关系,则x点是非平衡状态,且x点体系中B的百分含量有增大的趋势 |
C.图3为C的百分含量,由图可知该反应的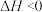 ,且 ,且 |
| D.图4所示图中的阴影部分面积的含义是该物质物质的量的变化量 |
您最近一年使用:0次
4 . 在 ℃,
℃, 下,向1L的密闭容器中充入1mol
下,向1L的密闭容器中充入1mol 和一定物质的量的
和一定物质的量的 发生反应:
发生反应: ,平衡时
,平衡时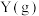 的物质的量分数与初始投料比
的物质的量分数与初始投料比 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是
 ℃,
℃, 下,向1L的密闭容器中充入1mol
下,向1L的密闭容器中充入1mol 和一定物质的量的
和一定物质的量的 发生反应:
发生反应: ,平衡时
,平衡时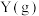 的物质的量分数与初始投料比
的物质的量分数与初始投料比 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是
A.随着 的增大, 的增大, 的转化率逐渐增大 的转化率逐渐增大 |
B.e点: |
C.a点时,该反应的平衡常数为 |
D.a点,平衡后再投入1mol 和1mol 和1mol ,达到新平衡时, ,达到新平衡时,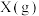 的产率增大 的产率增大 |
您最近一年使用:0次
名校
解题方法
5 . 甲烷、水蒸气催化重整是工业制备氢气的方法之一,其反应为 。在压强为p和不同温度下,平衡体系中氢气的体积分数与甲烷、水蒸气的投料比[用
。在压强为p和不同温度下,平衡体系中氢气的体积分数与甲烷、水蒸气的投料比[用 表示]的变化关系如图所示。
表示]的变化关系如图所示。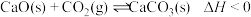 。
。
下列说法错误的是
 。在压强为p和不同温度下,平衡体系中氢气的体积分数与甲烷、水蒸气的投料比[用
。在压强为p和不同温度下,平衡体系中氢气的体积分数与甲烷、水蒸气的投料比[用 表示]的变化关系如图所示。
表示]的变化关系如图所示。
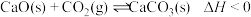 。
。下列说法错误的是
| A.该反应中正反应的活化能大于逆反应的活化能 |
B.向平衡体系中加入适量的 ,可提高氢气的产率 ,可提高氢气的产率 |
C.M点甲烷的平衡转化率为 |
D.在压强为p和600℃时,若向反应器中充入 和 和 ,平衡时氢气的体积分数小于 ,平衡时氢气的体积分数小于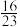 |
您最近一年使用:0次
名校
6 . 下图(左)表示1-甲基萘(1-MN)加氢饱和反应网络,四个加氢反应均为放热反应(用反应1、2、3、4表示)。下图(右)表示反应温度(T)对平衡时反应体系中有机化合物物质的量分数(x/%)的影响(6MPa,1-MN和 体积比为1∶5条件下)。下列说法
体积比为1∶5条件下)。下列说法不正确 的是
 体积比为1∶5条件下)。下列说法
体积比为1∶5条件下)。下列说法 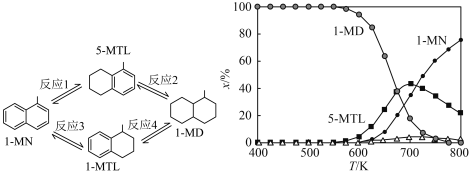
| A.800K反应2和反应4生成1-MD的程度很小 |
| B.600K到800K,反应1的平衡常数逐渐减小 |
| C.700K反应1的平衡常数小于反应3的平衡常数 |
| D.600K到650K,反应2中5-MTL增加的量大于反应1中5-MTL减少的量 |
您最近一年使用:0次
名校
7 . 在500℃、60.0MPa条件下合成氨,原料气投料比与平衡时 体积分数的关系如图所示。
体积分数的关系如图所示。
 体积分数的关系如图所示。
体积分数的关系如图所示。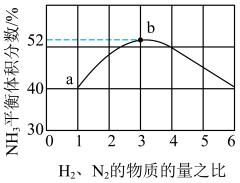
A.按a点的投料比进行反应,当 的体积分数不变时达到平衡状态 的体积分数不变时达到平衡状态 |
B.a点的平衡体系中, |
C.b点的平衡体系中, 的体积分数为36% 的体积分数为36% |
| D.b点混合气体的平均相对分子质量约为11.33 |
您最近一年使用:0次
2024-03-06更新
|
91次组卷
|
2卷引用:安徽省淮北市树人高级中学2023-2024学年上学期高二11月期中考试化学试题
名校
8 . 对于可逆反应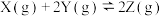
 ,下列图像中正确的是
,下列图像中正确的是
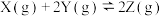
 ,下列图像中正确的是
,下列图像中正确的是 | 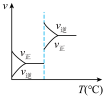 |  | 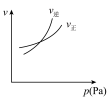 |
| A.反应体系中X的体积分数与时间的关系图 | B.正逆反应速率与温度的关系图 | C.不同温度下X的转化率与时间的关系图 | D.正逆反应速率与压强的关系图 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-11-12更新
|
200次组卷
|
3卷引用:安徽省合肥市第一中学2023-2024学年高二上学期期中考试化学试题
名校
解题方法
9 . 下列对应图像的叙述正确的是
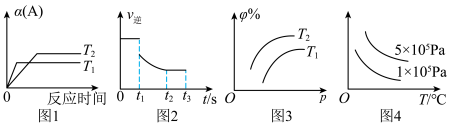

A.对于反应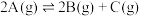  ,若图1中 ,若图1中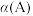 表示A的转化率,则温度 表示A的转化率,则温度 、 、 |
B.图2可表示 在 在 s时扩大容器体积, s时扩大容器体积, 随时间变化的曲线 随时间变化的曲线 |
C.对于反应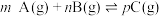 ,若图3表示A的体积分数与压强、温度的关系,则 ,若图3表示A的体积分数与压强、温度的关系,则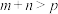 |
D.图4中纵坐标可表示反应  在不同温度、不同压强下的平衡常数 在不同温度、不同压强下的平衡常数 |
您最近一年使用:0次
10 . 下列有关图像的描述不正确的是
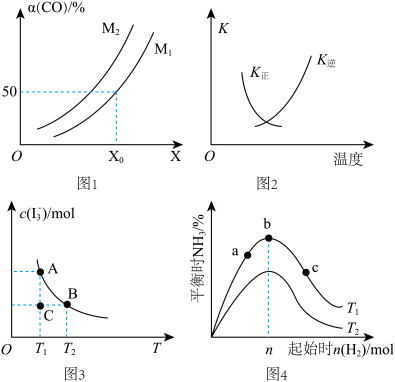

A.图1可表示反应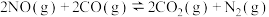  的CO的平衡转化率与温度、压强之间的关系,则X代表压强, 的CO的平衡转化率与温度、压强之间的关系,则X代表压强,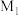 与 与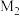 代表不同温度,且 代表不同温度,且 |
B.图2可表示反应  的正、逆反应平衡常数K随温度的变化曲线 的正、逆反应平衡常数K随温度的变化曲线 |
C.若图3表示反应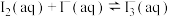 平衡时 平衡时 与T的关系,则C点状态: 与T的关系,则C点状态: |
D.若图4表示工业合成氨反应改变起始时 对平衡的影响,则 对平衡的影响,则 ,a、b、c三点所处的平衡状态中,b点 ,a、b、c三点所处的平衡状态中,b点 的转化率最高 的转化率最高 |
您最近一年使用:0次



