名校
1 . 设 为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是
 为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是A.标准状况下, 含c分子数为 含c分子数为 |
B.1LpH=1的硫酸溶液含氢离子数为 |
C.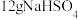 固体含阴离子数为 固体含阴离子数为 |
D.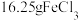 完全溶于沸水后,生成 完全溶于沸水后,生成 胶粒的数目为 胶粒的数目为 |
您最近一年使用:0次
2024-02-25更新
|
549次组卷
|
4卷引用:四川省内江市第六中学2023-2024学年高三下学期入学考试理综试题-高中化学
四川省内江市第六中学2023-2024学年高三下学期入学考试理综试题-高中化学2024届陕西省安康市高三下学期一模考试理科综合试题-高中化学(已下线)专题01 基本概念-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)2024届陕西省西安博爱国际学校高三下学期第一次模拟考试理科综合试卷-高中化学
2 . 常温下,0.10 mol/L HCOONH4溶液中部分微粒( 、
、 、HCOOH、
、HCOOH、 )的
)的 (可通入加入NaOH或HCl调节溶液pH)关系如图所示。
(可通入加入NaOH或HCl调节溶液pH)关系如图所示。 ,
,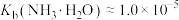 。下列说法正确的是
。下列说法正确的是


 、
、 、HCOOH、
、HCOOH、 )的
)的 (可通入加入NaOH或HCl调节溶液pH)关系如图所示。
(可通入加入NaOH或HCl调节溶液pH)关系如图所示。 ,
,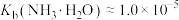 。下列说法正确的是
。下列说法正确的是

A.曲线②和③分别表示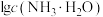 和 和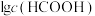 随pH的变化 随pH的变化 |
| B.溶液中M点对应的pH=7 |
C.HCOONH4的水解平衡常数 约为 约为 |
D.原溶液中 |
您最近一年使用:0次
2024-02-25更新
|
146次组卷
|
2卷引用:湖北省新高考协作体2023-2024学年高三下学期2月收心考试化学试题
3 . 某工厂采用如下工艺处理镍钴矿硫酸浸取液含( 、
、 、
、 、
、 、
、 和
和 )。实现镍、钴、镁元素的回收。
)。实现镍、钴、镁元素的回收。
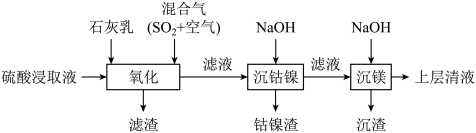
已知:
回答下列问题:
(1)用硫酸浸取镍钴矿时,提高浸取速率的方法为___________ (答出一条即可)。
(2)“氧化”中,混合气在金属离子的催化作用下产生具有强氧化性的过一硫酸( ),
), 中S的化合价为+6,其中过氧键的数目为
中S的化合价为+6,其中过氧键的数目为___________ 。
(3)“氧化”中,用石灰乳调节pH=4, 被
被 氧化为
氧化为 ,该反应的化学方程式为
,该反应的化学方程式为___________ ;滤渣的成分为 、
、
___________ (填化学式)。
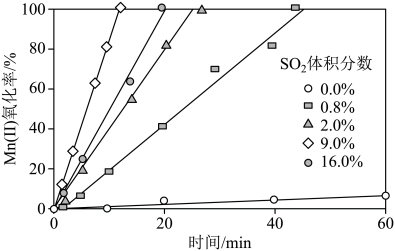
(4)“氧化”中保持空气通入速率不变,Mn(Ⅱ)氧化率与时间的关系如下。 体积分数为
体积分数为___________ 时,Mn(Ⅱ)氧化速率最大;继续增大 体积分数时,Mn(Ⅱ)氧化速率减小的原因是
体积分数时,Mn(Ⅱ)氧化速率减小的原因是___________ 。
(5)“沉钴镍”中得到的Co(Ⅱ)在空气中可被氧化成棕色的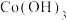 ,该反应的化学方程式为
,该反应的化学方程式为___________ 。
(6)“沉镁”中为使 沉淀完全(溶液中剩余离子浓度小于
沉淀完全(溶液中剩余离子浓度小于 mol/L),需控制pH不低于
mol/L),需控制pH不低于___________ 。
 、
、 、
、 、
、 、
、 和
和 )。实现镍、钴、镁元素的回收。
)。实现镍、钴、镁元素的回收。
已知:
| 物质 |  |  |  |  |
 |  |  |  | 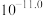 |
(1)用硫酸浸取镍钴矿时,提高浸取速率的方法为
(2)“氧化”中,混合气在金属离子的催化作用下产生具有强氧化性的过一硫酸(
 ),
), 中S的化合价为+6,其中过氧键的数目为
中S的化合价为+6,其中过氧键的数目为(3)“氧化”中,用石灰乳调节pH=4,
 被
被 氧化为
氧化为 ,该反应的化学方程式为
,该反应的化学方程式为 、
、
(4)“氧化”中保持空气通入速率不变,Mn(Ⅱ)氧化率与时间的关系如下。
 体积分数为
体积分数为 体积分数时,Mn(Ⅱ)氧化速率减小的原因是
体积分数时,Mn(Ⅱ)氧化速率减小的原因是
(5)“沉钴镍”中得到的Co(Ⅱ)在空气中可被氧化成棕色的
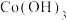 ,该反应的化学方程式为
,该反应的化学方程式为(6)“沉镁”中为使
 沉淀完全(溶液中剩余离子浓度小于
沉淀完全(溶液中剩余离子浓度小于 mol/L),需控制pH不低于
mol/L),需控制pH不低于
您最近一年使用:0次
2023-10-08更新
|
134次组卷
|
2卷引用:山西省运城市2023-2024学年高三上学期开学考试化学试题
解题方法
4 . 设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.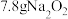 中所含阴离子数为 中所含阴离子数为 |
B. 和 和 在一定条件下充分反应生成的 在一定条件下充分反应生成的 分子数为 分子数为 |
C.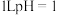 的 的 溶液中 溶液中 数目为 数目为 |
D.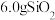 中的 中的 共价键的数目为 共价键的数目为 |
您最近一年使用:0次
名校
解题方法
5 . NA为阿伏加德罗常数的值。下列说法错误的是
| A.物质的量均为1mol的-OH和-CH3,所含电子数均为9NA |
| B.常温常压下,28g丁烯和环戊烷(C5H10)混合物中含有共价键数目为6NA |
| C.标准状况下,4.48L氯仿(CHC13)所含氯原子数目为0.6NA |
| D.1LpH=2的硫酸溶液中H+的数目为0.01NA |
您最近一年使用:0次
2023-09-07更新
|
111次组卷
|
2卷引用:河北省秦皇岛市部分学校2023-2024学年高三上学期开学联考化学试题
6 .  为阿伏加德罗常数的值。关于实验室制乙炔反应
为阿伏加德罗常数的值。关于实验室制乙炔反应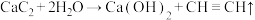 ,下列说法不正确的是
,下列说法不正确的是
 为阿伏加德罗常数的值。关于实验室制乙炔反应
为阿伏加德罗常数的值。关于实验室制乙炔反应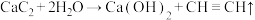 ,下列说法不正确的是
,下列说法不正确的是A. 与 与 所含电子数均为 所含电子数均为 |
B. 乙炔分子中含有的 乙炔分子中含有的 键数目为 键数目为 |
C.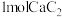 和 和 中含有的阴离子数目相同 中含有的阴离子数目相同 |
D.常温下, 的 的 中含有的阴离子数目为 中含有的阴离子数目为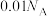 |
您最近一年使用:0次
7 . 关于化学计量问题(设 为阿伏加德罗常数的值)的表述,下列说法中正确的是
为阿伏加德罗常数的值)的表述,下列说法中正确的是
 为阿伏加德罗常数的值)的表述,下列说法中正确的是
为阿伏加德罗常数的值)的表述,下列说法中正确的是A.向溶质为0.1mol的 溶液中通入0.2mol 溶液中通入0.2mol , , 和 和 均被氧化 均被氧化 |
B.常温下, 乙二酸溶液的 乙二酸溶液的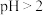 ,则含 ,则含 的数目大于0.01mol 的数目大于0.01mol |
C.1mol熔融的 中含有的离子数目为 中含有的离子数目为 |
| D.1mol带有乙基支链的链状烃中,主链所含有的碳原子数最少为5mol |
您最近一年使用:0次
名校
8 . 设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.在标准状况下, 分子中含氯原子数目为 分子中含氯原子数目为 |
B.1LpH均为2的硫酸和醋酸溶液,氢离子数均为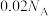 |
C.64g铜与足量硫粉加热充分反应,转移电子数为 |
D.30g由乙酸和葡萄糖组成的混合物中含氢原子个数为 |
您最近一年使用:0次
2023-02-08更新
|
128次组卷
|
2卷引用:吉林省通化市梅河口市第五中学2023-2024学年高三上学期开学考试化学试题
9 . 从含铅烟灰(主要化学成分为PbO、Fe2O3、In2O3和In2S3)中分离回收铟和锡的工艺流程如图。
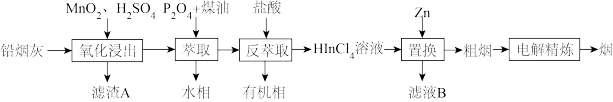
已知:①“萃取”时发生反应:In3++3H2A2(有机液)→In(HA2)3(有机液)+3H+;
Fe3++3H2A2(有机液) →Fe(HA2)3(有机液)+3H+
②“反萃取”时发生反应:In(HA2)3(有机液)+4HCl→3(HA2)3(有机液)+HInCl4。
回答下列问题:
(1)“浸出”过程中硫元素最终均以硫酸根的形式存在于浸出液中,请写出In2S3发生反应的化学方程式____ 。
(2)滤渣A的主要成分除含过量MnO2外,还有___ (填化学式)。
(3)“萃取”过程中的萃取剂可用H2A2表示,使In3+进入有机相,萃取过程发生的化学反应方程式为:In3++3H2A2 In(HA2)3+3H+,平衡常数为K=9.96。“萃取”过程中萃取剂和浸出液的用量比、萃取时间和萃取率(E%)的关系如表所示。“萃取”时萃取率的高低受溶液的pH影响很大,已知pH与萃取率的关系符合如下公式:lg
In(HA2)3+3H+,平衡常数为K=9.96。“萃取”过程中萃取剂和浸出液的用量比、萃取时间和萃取率(E%)的关系如表所示。“萃取”时萃取率的高低受溶液的pH影响很大,已知pH与萃取率的关系符合如下公式:lg =lgK-lg
=lgK-lg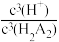 。当pH=2.30时,萃取率为50%,若将萃取率提升到95%,应调节溶液的pH=
。当pH=2.30时,萃取率为50%,若将萃取率提升到95%,应调节溶液的pH=___ (已知lg19=1.28,忽略萃取剂浓度的变化,结果保留三位有效数字)。
(4)盐酸的浓度与铟、铁的反萃取率的关系如图所示。则“反萃取”过程中应选择盐酸的最佳浓度为____ 。

(5)“置换”后所得浊液,需要经过过滤、洗涤、干燥等操作得到粗铟,在洗涤操作中,检验粗铟已洗涤干净的方法为___ 。
(6)电解精炼铟时阳极材料应选用____ ,随着电解的不断进行,电解液中c(In3+)会逐渐____ (“减小”或“不变”)。

已知:①“萃取”时发生反应:In3++3H2A2(有机液)→In(HA2)3(有机液)+3H+;
Fe3++3H2A2(有机液) →Fe(HA2)3(有机液)+3H+
②“反萃取”时发生反应:In(HA2)3(有机液)+4HCl→3(HA2)3(有机液)+HInCl4。
回答下列问题:
(1)“浸出”过程中硫元素最终均以硫酸根的形式存在于浸出液中,请写出In2S3发生反应的化学方程式
(2)滤渣A的主要成分除含过量MnO2外,还有
(3)“萃取”过程中的萃取剂可用H2A2表示,使In3+进入有机相,萃取过程发生的化学反应方程式为:In3++3H2A2
 In(HA2)3+3H+,平衡常数为K=9.96。“萃取”过程中萃取剂和浸出液的用量比、萃取时间和萃取率(E%)的关系如表所示。“萃取”时萃取率的高低受溶液的pH影响很大,已知pH与萃取率的关系符合如下公式:lg
In(HA2)3+3H+,平衡常数为K=9.96。“萃取”过程中萃取剂和浸出液的用量比、萃取时间和萃取率(E%)的关系如表所示。“萃取”时萃取率的高低受溶液的pH影响很大,已知pH与萃取率的关系符合如下公式:lg =lgK-lg
=lgK-lg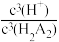 。当pH=2.30时,萃取率为50%,若将萃取率提升到95%,应调节溶液的pH=
。当pH=2.30时,萃取率为50%,若将萃取率提升到95%,应调节溶液的pH=(4)盐酸的浓度与铟、铁的反萃取率的关系如图所示。则“反萃取”过程中应选择盐酸的最佳浓度为

(5)“置换”后所得浊液,需要经过过滤、洗涤、干燥等操作得到粗铟,在洗涤操作中,检验粗铟已洗涤干净的方法为
(6)电解精炼铟时阳极材料应选用
您最近一年使用:0次
解题方法
10 . 硼及其化合物在工业上有许多用途.以铁硼矿(主要成分为 和
和 ,还有少量
,还有少量 、
、 、
、 、
、 和
和 等)为原料制备硼酸
等)为原料制备硼酸 的工艺流程如下:
的工艺流程如下:

已知相关高子形成氢氧化物开始沉淀至沉淀完全时的pH范围如下:
 :7.6~9.6
:7.6~9.6  :2.7~3.7
:2.7~3.7  :3.4~4.7
:3.4~4.7  :9.6~11.1
:9.6~11.1
请回答下列问题:
(1)写出 与硫酸反应的化学方程式:
与硫酸反应的化学方程式:_______ 。
(2)为提高浸出速率,除适当增加硫酸浓度外,还可采取的措施有_______ (写出两条)。
(3)“浸渣”中的物质是_______ (化学式)。
(4)“净化除杂”需先加 溶液,其作用用离子方程式表示为
溶液,其作用用离子方程式表示为_______ ,然后再调节溶液的pH约为5,其目的是_______ 。
(5)硼的重要化合物 与水反应生成硼酸和氢气,在某温度下
与水反应生成硼酸和氢气,在某温度下 与水反应后得
与水反应后得 溶液,其pH值为
溶液,其pH值为_______ (已知该温度下硼酸的电离常数 )。
)。
 和
和 ,还有少量
,还有少量 、
、 、
、 、
、 和
和 等)为原料制备硼酸
等)为原料制备硼酸 的工艺流程如下:
的工艺流程如下:
已知相关高子形成氢氧化物开始沉淀至沉淀完全时的pH范围如下:
 :7.6~9.6
:7.6~9.6  :2.7~3.7
:2.7~3.7  :3.4~4.7
:3.4~4.7  :9.6~11.1
:9.6~11.1请回答下列问题:
(1)写出
 与硫酸反应的化学方程式:
与硫酸反应的化学方程式:(2)为提高浸出速率,除适当增加硫酸浓度外,还可采取的措施有
(3)“浸渣”中的物质是
(4)“净化除杂”需先加
 溶液,其作用用离子方程式表示为
溶液,其作用用离子方程式表示为(5)硼的重要化合物
 与水反应生成硼酸和氢气,在某温度下
与水反应生成硼酸和氢气,在某温度下 与水反应后得
与水反应后得 溶液,其pH值为
溶液,其pH值为 )。
)。
您最近一年使用:0次



