解题方法
1 . 下列化学用语或图示表达不正确 的是
A.NaOH的电子式: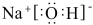 | B.基态Cu原子的价层电子排布式: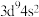 |
C.乙醇的分子式: | D.乙炔的分子空间填充模型: |
您最近一年使用:0次
名校
解题方法
2 . 下列性质的比较中,不正确的是
A.电负性: | B.第一电离能: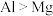 |
C.微粒半径: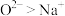 | D.酸性: |
您最近一年使用:0次
3 . 下列物质的应用不涉及氧化还原反应的是
| A.次氯酸钠作纸张的漂白剂 | B.铁粉作食品保鲜的吸氧剂 |
| C.过氧化钠作呼吸面具的供氧剂 | D.碳酸氢钠作面食的膨松剂 |
您最近一年使用:0次
名校
解题方法
4 . 常温下,下列各组离子在指定溶液中可能大量共存的是
A.0.1mol•L-1的NaClO溶液中:H+、Fe2+、Cl-、SO |
B.加入铝粉能生成H2的溶液中:Na+、Mg2+、NO 、Cl- 、Cl- |
C.滴加几滴KSCN溶液显红色的溶液中:H+、Mg2+、SO 、Cl- 、Cl- |
D. =1.0×1012的溶液中:Na+、Mg2+、NO =1.0×1012的溶液中:Na+、Mg2+、NO 、HCO 、HCO |
您最近一年使用:0次
名校
解题方法
5 . 下列有机化合物的命名不正确的是
| A.CH2Cl-CH=CH2 3-氯丙烯 | B. 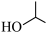 甲基-1-丙醇 甲基-1-丙醇 |
C. 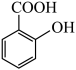 2-羟基苯甲酸 2-羟基苯甲酸 | D. 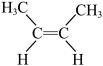 顺-2-丁烯 顺-2-丁烯 |
您最近一年使用:0次
名校
6 . 唐代张九龄诗句“松叶堪为酒,春来酿几多”涉及淀粉、麦芽糖、葡萄糖、乙醇等化学物质,下列有关说法错误的是
| A.淀粉、乙醇所含元素种类相同 |
| B.淀粉、麦芽糖都能发生水解反应,最终生成葡萄糖 |
| C.葡萄糖、麦芽糖都能被新制的Cu(OH)2氧化 |
| D.蔗糖和麦芽糖、淀粉和纤维素都互为同分异构体 |
您最近一年使用:0次
7 . 铁元素的常见价态有+2、+3价,实验室可用赤血盐(K3[Fe(CN)6])溶液检验Fe2+,黄血盐(K4[Fe(CN)6])溶液检验Fe3+。Fe2O3是重要的化工原料,Au/Fe2O3可用作反应CO(g)+H2O(g)=CO2(g)+H2(g)的催化剂。硫铁矿烧渣中含有大量Fe2O3,工业上常用于制取绿矾(FeSO4·7H2O)。
1.下列有关铁及其化合物的说法正确的是
2.在指定条件下,下列有关铁单质的转化不能实现的是
3.对于反应CO(g)+H2O(g)=CO2(g)+H2(g),下列有关说法不正确的是
4.由硫铁矿烧渣(主要含Fe2O3、Al2O3、SiO2)制取绿矾的流程如下:
1.下列有关铁及其化合物的说法正确的是

| A.Fe元素位于周期表的第ⅥB族 |
| B.绿矾中Fe2+核外有6个未成对电子 |
| C.赤血盐是含有配位键的离子化合物 |
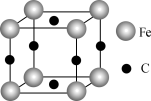
| D.若黄血盐受热分解产物之一的晶胞结构如图所示,则其化学式为Fe4C3 |
A.Fe(s)  FeCl3(s) FeCl3(s) | B.Fe(s)  Fe2O3(s) Fe2O3(s) |
C.Fe(s) 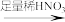 Fe(NO3)3(aq) Fe(NO3)3(aq) | D.Fe(s) 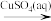 FeSO4(aq) FeSO4(aq) |
| A.加入催化剂Au/Fe2O3,反应的焓变ΔH不变 |
| B.升高温度,反应体系的活化分子百分数增多 |
| C.向固定容积的反应体系中充入氦气,反应速率加快 |
D.其他条件相同,增大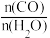 ,反应的平衡常数K不变 ,反应的平衡常数K不变 |
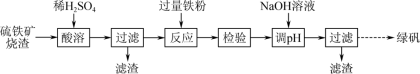
| A.“酸溶”时先将烧渣粉碎并不断搅拌,可提高铁元素的浸出率 |
| B.“反应”时发生的主要反应为2Fe3++Fe=3Fe2+ |
| C.“检验”时可用K4[Fe(CN)6]溶液检验上一步“反应”是否进行完全 |
| D.将第二次“过滤”所得滤液加热,经蒸发结晶可以制得绿矾 |
您最近一年使用:0次
解题方法
8 . 高纯硫酸锰主要应用于三元锂电池正极材料的合成,一种使用高硫锰矿和软锰矿(主要成分为 )制备硫酸锰的工艺如图:
)制备硫酸锰的工艺如图: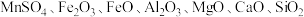 ;离子浓度
;离子浓度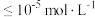 ,可认为离子沉淀完全。
,可认为离子沉淀完全。
(1)原料高硫锰矿与软锰矿按一定比例焙烧,焙烧前需要将二者粉碎的原因是___________ 。
(2)加入硫酸浸出后获得的浸渣1主要成分为___________ 。
(3)氧化时发生反应的离子方程式为___________ 。
(4)氟化除杂是除去 和
和 的重要方法,某
的重要方法,某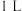 溶液中
溶液中 和
和 的浓度分别为
的浓度分别为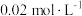 、
、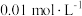 ,若使溶液中的
,若使溶液中的 和
和 沉淀完全,加入的
沉淀完全,加入的 的质量至少是
的质量至少是___________  (保留小数点后1位);若溶液的
(保留小数点后1位);若溶液的 浓度过大,将导致
浓度过大,将导致 、
、 沉淀不完全,原因是
沉淀不完全,原因是___________ 。(已知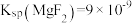 、
、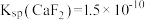 )
)
(5)沉锰时发生反应的离子方程式为___________ 。
(6)一种在硫酸溶液中电解锂离子电池正极材料 获得
获得 的装置如图,则阴极电极反应式为
的装置如图,则阴极电极反应式为___________ 。
 )制备硫酸锰的工艺如图:
)制备硫酸锰的工艺如图: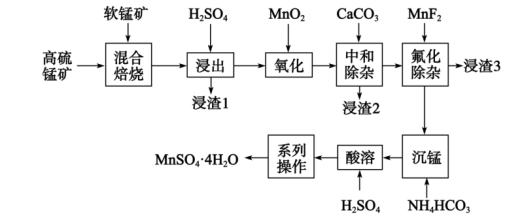
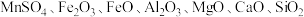 ;离子浓度
;离子浓度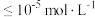 ,可认为离子沉淀完全。
,可认为离子沉淀完全。(1)原料高硫锰矿与软锰矿按一定比例焙烧,焙烧前需要将二者粉碎的原因是
(2)加入硫酸浸出后获得的浸渣1主要成分为
(3)氧化时发生反应的离子方程式为
(4)氟化除杂是除去
 和
和 的重要方法,某
的重要方法,某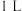 溶液中
溶液中 和
和 的浓度分别为
的浓度分别为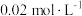 、
、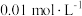 ,若使溶液中的
,若使溶液中的 和
和 沉淀完全,加入的
沉淀完全,加入的 的质量至少是
的质量至少是 (保留小数点后1位);若溶液的
(保留小数点后1位);若溶液的 浓度过大,将导致
浓度过大,将导致 、
、 沉淀不完全,原因是
沉淀不完全,原因是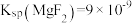 、
、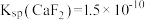 )
)(5)沉锰时发生反应的离子方程式为
(6)一种在硫酸溶液中电解锂离子电池正极材料
 获得
获得 的装置如图,则阴极电极反应式为
的装置如图,则阴极电极反应式为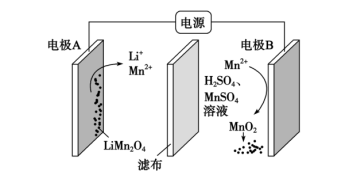
您最近一年使用:0次
解题方法
9 . 镁是一种在生产生活中有着重要用途的金属,回答下列问题:
(1)镁(I)在生物体中起催化、调节和信号传导等作用,图中物质Ⅰ是一种新型 比率荧光传感器,除
比率荧光传感器,除 外,在其他金属阳离子存在下,荧光比没有明显变化。
外,在其他金属阳离子存在下,荧光比没有明显变化。 同周期,基态原子有4个未成对电子的元素有
同周期,基态原子有4个未成对电子的元素有___________ 种。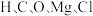 电负性由大到小的顺序为
电负性由大到小的顺序为___________ 。
②物质Ⅰ中N的杂化类型有___________ ,物质Ⅱ中 键角大于水中
键角大于水中 键角,原因是
键角,原因是___________ 。物质Ⅱ中配体数与配位键数之比为___________ 。
(2)一种含镁、镍、碳3种元素的超导材料,结构中有两种八面体空隙,一种完全由镍原子构成,另一种由镍原子和镁原子共同构成,碳原子只填充在由镍原子构成的八面体空隙中,其立方晶胞在xy、xz、yz平面投影相同,如图所示, 分别代表三种原子,
分别代表三种原子, 为
为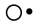 两种原子投影的重合。
两种原子投影的重合。___________ 。
②晶胞中镍原子和碳原子最近的距离为 ,阿伏伽德罗常数的值为
,阿伏伽德罗常数的值为 ,则晶胞密度为
,则晶胞密度为___________  。
。
(1)镁(I)在生物体中起催化、调节和信号传导等作用,图中物质Ⅰ是一种新型
 比率荧光传感器,除
比率荧光传感器,除 外,在其他金属阳离子存在下,荧光比没有明显变化。
外,在其他金属阳离子存在下,荧光比没有明显变化。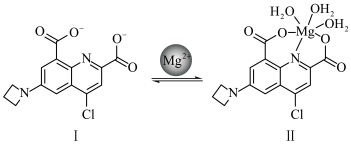
 同周期,基态原子有4个未成对电子的元素有
同周期,基态原子有4个未成对电子的元素有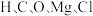 电负性由大到小的顺序为
电负性由大到小的顺序为②物质Ⅰ中N的杂化类型有
 键角大于水中
键角大于水中 键角,原因是
键角,原因是(2)一种含镁、镍、碳3种元素的超导材料,结构中有两种八面体空隙,一种完全由镍原子构成,另一种由镍原子和镁原子共同构成,碳原子只填充在由镍原子构成的八面体空隙中,其立方晶胞在xy、xz、yz平面投影相同,如图所示,
 分别代表三种原子,
分别代表三种原子, 为
为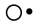 两种原子投影的重合。
两种原子投影的重合。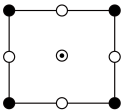
②晶胞中镍原子和碳原子最近的距离为
 ,阿伏伽德罗常数的值为
,阿伏伽德罗常数的值为 ,则晶胞密度为
,则晶胞密度为 。
。
您最近一年使用:0次
10 . 以钢铁厂锌灰(主要成分为 ,含少量的
,含少量的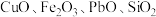 等)为原料制备高纯氧化锌的工艺流程如下:
等)为原料制备高纯氧化锌的工艺流程如下:
 ,含少量的
,含少量的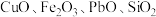 等)为原料制备高纯氧化锌的工艺流程如下:
等)为原料制备高纯氧化锌的工艺流程如下: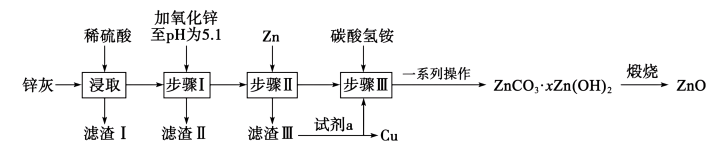
A.滤渣I的主要成分是 |
| B.加入试剂a的目的是提取铜中的锌 |
C.氢氧化铁的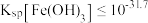 |
D.若取步骤III后的固体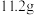 煅烧,得到产品 煅烧,得到产品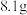 ,则 ,则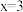 |
您最近一年使用:0次



