名校
1 . 某兴趣小组对NaOH溶液和稀盐酸混合后的有关问题进行了如下探究:
查阅资料:如表是实验室里盐酸、NaOH试剂瓶标签上的部分说明:
实验探究:
(1)配制溶液:甲同学配制100mL1.5mol·L-1NaOH溶液,乙同学取20mL36.5%的盐酸稀释到200mL。甲为了证明NaOH溶液与稀盐酸能发生化学反应,设计并完成了如图所示的实验。
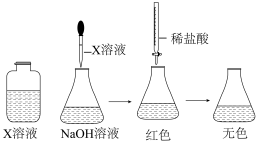
X溶液滴入的量一般为____ ,使用酸式滴定管前要检查活塞是否漏水的操作方法是____ 。
(2)乙设计完成了另一个实验,以证明NaOH溶液与盐酸能够发生反应。他在盛有20mL稀盐酸的锥形瓶里,用碱式滴定管滴入NaOH溶液,不断振荡溶液,同时用pH计测定溶液的pH,直到NaOH溶液过量。则在滴定过程中,滴定终点附近的操作是____ 。
(3)你认为甲、乙两位同学的实验中,____ (填“甲”、“乙”或“甲和乙”)的实验能充分证明NaOH与盐酸发生了反应。
(4)丙同学为了测定上述36.5%盐酸的物质的量浓度,进行了如下实验:在锥形瓶中加入已稀释的盐酸,用碱式滴定管滴入甲配制的NaOH溶液,测定的结果如表:
据此通过计算可知实验测定的盐酸浓度与标签说明的浓度相比____ (填“偏高”、“偏低”或“相等”)。
查阅资料:如表是实验室里盐酸、NaOH试剂瓶标签上的部分说明:
| 化学式 | 相对分子质量 | ||
| 盐酸 | HCl | 36.5 | 密度:1.20g·mL-1,质量分数:36.5%,无色易挥发 |
| 氢氧化钠 | NaOH | 40 | 俗名:烧碱、火碱、苛性钠,易潮解的固体 |
(1)配制溶液:甲同学配制100mL1.5mol·L-1NaOH溶液,乙同学取20mL36.5%的盐酸稀释到200mL。甲为了证明NaOH溶液与稀盐酸能发生化学反应,设计并完成了如图所示的实验。

X溶液滴入的量一般为
(2)乙设计完成了另一个实验,以证明NaOH溶液与盐酸能够发生反应。他在盛有20mL稀盐酸的锥形瓶里,用碱式滴定管滴入NaOH溶液,不断振荡溶液,同时用pH计测定溶液的pH,直到NaOH溶液过量。则在滴定过程中,滴定终点附近的操作是
(3)你认为甲、乙两位同学的实验中,
(4)丙同学为了测定上述36.5%盐酸的物质的量浓度,进行了如下实验:在锥形瓶中加入已稀释的盐酸,用碱式滴定管滴入甲配制的NaOH溶液,测定的结果如表:
| 测定次数 | 盐酸的体积/mL | 氢氧化钠溶液的体积 | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 2.00 | 21.99 |
| 3 | 25.00 | 0.20 | 20.20 |
您最近一年使用:0次
名校
2 . 某兴趣小组对NaOH溶液和稀盐酸混合后的有关问题进行了如下探究:查阅资料:下表是实验室里盐酸、NaOH试剂瓶标签上的部分说明:
实验探究:
(1)配制溶液:甲同学配制100 mL 1.5 mol·L-1NaOH溶液,乙同学取20 mL 36.5%的盐酸稀释到200 mL。甲为了证明NaOH溶液与稀盐酸能发生化学反应,设计并完成了如下图所示的实验。
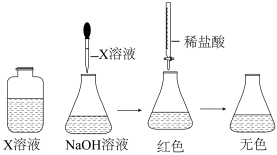
X溶液滴入的量一般为______ ,使用酸式滴定管前要检查活塞是否漏水的操作方法是________ 。
(2)乙设计完成了另一个实验,以证明NaOH溶液与盐酸能够发生反应。他在盛有20 mL稀盐酸的锥形瓶里,用碱式滴定管滴入NaOH溶液,不断振荡溶液,同时用pH计测定溶液的pH,直到NaOH溶液过量。则在滴定过程中,滴定终点附近的操作是_______ 。
(3)你认为甲、乙两位同学的实验中,______ (填“甲”、“乙”或“甲和乙”)的实验能充分证明NaOH与盐酸发生了反应。
(4)丙同学为了测定上述36.5%盐酸的物质的量浓度,进行了如下实验:在锥形瓶中加入已稀释的盐酸,用碱式滴定管滴入甲配制的NaOH溶液,测定的结果如下表:
据此通过计算可知实验测定的盐酸浓度与标签说明的浓度相比_____ (填“偏高”、“偏低”或“相等”)。
| 化学式 | 相对分子质量 | ||
| 盐酸 | HCl | 36.5 | 密度: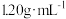 , ,质量分数:36.5%, 无色易挥发 |
| 氢氧化钠 | NaOH | 40 | 俗名:烧碱、火碱、苛 性钠,易潮解的固体 |
(1)配制溶液:甲同学配制100 mL 1.5 mol·L-1NaOH溶液,乙同学取20 mL 36.5%的盐酸稀释到200 mL。甲为了证明NaOH溶液与稀盐酸能发生化学反应,设计并完成了如下图所示的实验。

X溶液滴入的量一般为
(2)乙设计完成了另一个实验,以证明NaOH溶液与盐酸能够发生反应。他在盛有20 mL稀盐酸的锥形瓶里,用碱式滴定管滴入NaOH溶液,不断振荡溶液,同时用pH计测定溶液的pH,直到NaOH溶液过量。则在滴定过程中,滴定终点附近的操作是
(3)你认为甲、乙两位同学的实验中,
(4)丙同学为了测定上述36.5%盐酸的物质的量浓度,进行了如下实验:在锥形瓶中加入已稀释的盐酸,用碱式滴定管滴入甲配制的NaOH溶液,测定的结果如下表:
| 测定次数 | 盐酸的体积/mL | 氢氧化钠溶液的体积 | |
| 测定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 2.00 | 21.99 |
| 3 | 25.00 | 0.20 | 20.20 |
您最近一年使用:0次
2019-07-01更新
|
102次组卷
|
2卷引用:云南省玉溪市景东一中2018-2019学年高二6月份考试化学试题
名校
解题方法
3 . 用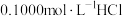 溶液滴定未知浓度的NaOH溶液。有关该实验说法中,不正确的是
溶液滴定未知浓度的NaOH溶液。有关该实验说法中,不正确的是
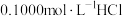 溶液滴定未知浓度的NaOH溶液。有关该实验说法中,不正确的是
溶液滴定未知浓度的NaOH溶液。有关该实验说法中,不正确的是| A.本实验可选用酚酞作指示剂 |
B.用酸式滴定管盛装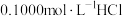 溶液 溶液 |
| C.用未知浓度的NaOH溶液润洗锥形瓶2~3次 |
| D.滴定结束时俯视酸式滴定管读数,测量结果偏低 |
您最近一年使用:0次
2024-01-09更新
|
210次组卷
|
15卷引用:云南省昭通一中教研联盟2023-2024学年高二上学期期末质量检测化学(B卷)
云南省昭通一中教研联盟2023-2024学年高二上学期期末质量检测化学(B卷)北京市西城区2021—2022学年高二上学期期末化学试题北京十四中2022-2023学年高二上学期期中检测化学试题北京市第八中学2022-2023学年高二上学期期末考试化学试题山西省太原市2022-2023学年高二下学期2月期末考试化学试题四川省雅安市2022-2023学年高二下学期期末检测化学试题广东省广州市协和中学等3校2022-2023学年高二上学期(12月)期末考试化学试题北京市清华大学附属中学朝阳学校2023-2024学年高二上学期期中考试化学试题 北京师范大学附属实验中学2023-2024学年高二上学期期中考试化学试题北京市第八中学2022-2023学年高二上学期期中考试化学试题北京市广渠门中学2023-2024学年高二上学期期中考试化学试题 北京师范大学附属实验中学顺义学校2023-2024学年高二上学期12月月考化学试题北京市第五十中学2023-2024学年高二上学期12月月考化学试题陕西省西安市周至县第四中学2023-2024学年高二上学期1月期末化学试题新疆阿克苏市实验中学2023-2024学年高二上学期期末考试化学试题
4 . 实验室用标准KMnO4溶液滴定未知浓度的FeSO4溶液,下列说法或操作正确的是
| A.选碱式滴定管量取标准KMnO4溶液,并用碘化钾淀粉溶液作指示剂 |
| B.滴定前仰视读数,滴定后俯视读数会导致滴定结果偏低 |
| C.盛FeSO4溶液的锥形瓶滴定前用FeSO4溶液润洗2~3次 |
| D.锥形瓶内溶液颜色变化由浅绿色变紫红色,立即记下滴定管液面所在刻度 |
您最近一年使用:0次
5 . 甲胺(CH3NH2)是一种应用广泛的一元弱碱。常温下,向20.00 mL0. 10 mol∙L-1的甲胺溶液中滴加V mL 0.10 mol·L-1盐酸,混合溶液的pH与 的关系曲线如图所示。
的关系曲线如图所示。

下列说法错误的是
 的关系曲线如图所示。
的关系曲线如图所示。
下列说法错误的是
| A.该滴定过程可选用甲基橙作指示剂 |
| B.常温下,甲胺的电离常数为Kb,则pKb=-lgKb=3.4 |
C.c点对应溶液可能存在关系:2c(H+)+c(CH3NH )=c(CH3NH2)+2c(OH-)+c(Cl-) )=c(CH3NH2)+2c(OH-)+c(Cl-) |
| D.b点对应溶液中加入盐酸的体积为20.00 mL |
您最近一年使用:0次
名校
6 . 下列有关实验操作的说法正确的是
| A.用苯萃取溴水中的溴,分液时应从下口放出溴的苯溶液 |
| B.中和热测定时环形玻璃搅拌棒要不断地顺时针搅拌,目的是为了混合均匀,充分反应 |
| C.用滴定管量取溶液体积,若读数时放出液体前仰视,放出液体后俯视,则测量值小于真实值 |
| D.用已知质量分数和密度的浓硫酸配制100 mL 1 mol· L-1H2SO4溶液,通常按计算值称量所需浓硫酸的质量. |
您最近一年使用:0次
名校
7 . 用 的
的 标准溶液滴定某未知浓度的
标准溶液滴定某未知浓度的 溶液,下列说法错误的是
溶液,下列说法错误的是
 的
的 标准溶液滴定某未知浓度的
标准溶液滴定某未知浓度的 溶液,下列说法错误的是
溶液,下列说法错误的是| A.该滴定实验不需要指示剂 |
| B.该实验用到的玻璃仪器有酸式滴定管、碱式滴定管、锥形瓶 |
| C.滴定管使用前需检验是否漏液 |
D.若滴定终止时,仰视读数,所测 浓度偏高 浓度偏高 |
您最近一年使用:0次
2020-09-20更新
|
629次组卷
|
9卷引用:云南省瑞丽市第一民族中学2021-2022学年高二下学期3月月考化学试题
云南省瑞丽市第一民族中学2021-2022学年高二下学期3月月考化学试题湖南省益阳市2018届高三4月调研考试理综化学试题(已下线)专题8.2 水的电离和溶液的pH(练)-《2020年高考一轮复习讲练测》鲁科版(2019)选择性必修1第3章 物质在水溶液中的行为 第4节 离子反应 课时2 离子反应的应用——酸碱中和滴定高中必刷题高二选择性必修1第三章 水溶液中的离子反应与平衡 第二节 水的电离和溶液的pH 课时2 酸碱中和滴定选择性必修1 专题3 第二单元 课时2 酸碱中和滴定黑龙江省七台河市勃利县高级中学2021-2022学年高二上学期9月月考化学试题3.2.2酸碱中和滴定 课后浙江省杭州市浙江大学附属中学2023-2024学年高二上学期期中考试化学试题
名校
8 . 下列关于酸碱中和滴定实验的说法正确的是( )
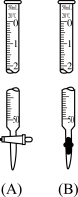

| A.用图B的滴定管可准确量取25.00mL的酸性KMnO4溶液 |
| B.滴定过程中,眼睛要时刻注视滴定管中液面的变化 |
| C.滴定管装入液体前需用待装液润洗 |
| D.滴定前平视,滴定结束后仰视读数,不影响测定结果 |
您最近一年使用:0次
2019-11-03更新
|
345次组卷
|
7卷引用:云南省楚雄天人中学2021-2022学年高二上学期12月月考化学试题(B卷)
云南省楚雄天人中学2021-2022学年高二上学期12月月考化学试题(B卷)安徽省滁州市明光中学2019-2020学年高二上学期第一次月考化学试题江苏省启东中学2019-2020学年高二上学期期中考试化学试题(已下线)3.2.2 酸碱中和滴定(练习)-2020-2021学年上学期高二化学同步精品课堂(新教材人教版选择性必修1)宁夏青铜峡市高级中学2020-2021学年高二上学期期中考试化学试题湖南省新宁县崀山培英学校2020-2021学年高二上学期期中考试化学试题(已下线)第03章 水溶液中的离子反应与平衡(A卷基础强化篇)-2020-2021学年高二化学选择性必修1同步单元AB卷(新教材人教版)
名校
解题方法
9 . 下列有关滴定操作的说法正确的是
| A.用25mL滴定管进行中和滴定时,用去标准液的体积为21.7mL |
| B.用标准的KOH溶液滴定未知浓度的盐酸,洗净碱式滴定管后直接取标准KOH溶液进行滴定,则测定结果偏低 |
| C.用标准的KOH溶液滴定未知浓度的盐酸,配制标准溶液的固体KOH中含有NaOH杂质,则测定结果偏高 |
| D.用未知浓度的盐酸滴定标准的KOH溶液时,若读取读数时,滴定前仰视,滴定到终点后俯视,会导致测定结果偏高 |
您最近一年使用:0次
2018-08-19更新
|
1921次组卷
|
15卷引用:云南省曲靖市会泽县第一中学2018-2019学年高二上学期第二次半月考化学试题
云南省曲靖市会泽县第一中学2018-2019学年高二上学期第二次半月考化学试题【全国校级联考】湖北省部分重点中学2019届高三上学期起点考试化学试题【全国百强校】黑龙江省哈尔滨市第六中学2018-2019学年高二上学期10月月考化学试题【全国百强校】湖南省衡阳市第八中学2018-2019学年高二上学期六科联赛试题(12月)化学试题【全国百强校】河北省石家庄市第二中学2018-2019学年高二上学期期中考试化学试题河北省邯郸市大名县第一中学2019-2020学年高二上学期12月月考化学试题(普通班)吉林省梅河口市第五中学2020-2021学年高二上学期第二次月考化学试题(已下线)3.2.4 酸碱中和滴定(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)吉林省抚松县第一中学2021-2022学年高二下学期开学考试化学试题第二节 水的电离和溶液的pH 第3课时 酸碱中和滴定黑龙江省绥化市庆安县第一中学2022-2023学年高二上学期期中考试化学试题黑龙江省绥化市庆安县第一中学2022-2023学年高二上学期期中考试化学试题(已下线)考点27 水的电离与溶液的pH(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)第三章 第二节 水的电离和溶液的pH 第2课时 酸碱中和滴定(已下线)第02讲 水的电离和溶液的酸碱性(练习)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)
名校
解题方法
10 . 一定物质的量浓度溶液的配制和酸碱中和滴定是中学化学中两个典型的定量实验。若要配制1 mol·L-1的稀硫酸标准溶液,用其滴定某未知浓度的NaOH溶液。下列有关说法错误的是( )
| A.实验中用到的滴定管和容量瓶使用前都需要检漏 |
| B.如果实验需用85 mL的稀硫酸标准溶液,配制时可选用100 mL容量瓶 |
| C.用甲基橙作指示剂,滴定终点时,溶液颜色从红色变为橙色 |
| D.酸式滴定管用蒸馏水洗涤后,即装入标准浓度的稀硫酸滴定,会导致测定的NaOH溶液浓度偏大 |
您最近一年使用:0次
2017-08-20更新
|
973次组卷
|
5卷引用:云南省临沧市第一中学2018届高三上学期期末考试化学试题



