名校
解题方法
1 . 用含铁废铜制备胆矾的流程如图所示,下列说法错误的是
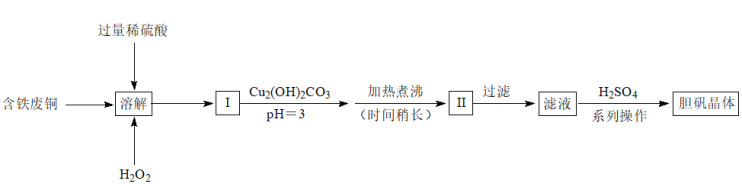

| A.“溶解”中加H2O2只是将Fe2+氧化为Fe3+ |
| B.流程中Cu2(OH)2CO3可用CuO代替 |
| C.pH=3时,c(Cu2+)·c2(OH-)<Ksp[Cu(OH)2] |
| D.“系列操作”前加入H2SO4的目的是抑制Cu2+的水解 |
您最近一年使用:0次
2021-09-18更新
|
1545次组卷
|
8卷引用:甘肃省高台县第一中学2021-2022学年高三上学期第二次检测化学试题
甘肃省高台县第一中学2021-2022学年高三上学期第二次检测化学试题河北省唐山市2021-2022学年高三上学期开学摸底考试化学试题河北省石家庄市第二十二中学2022届高三10月月考化学试题河北省石家庄市第二中学2022届高三上学期11月第三次考试化学试题(已下线)3.4.2 沉淀溶解平衡原理的应用-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)湖南省益阳市沅江市第一中学2022届高三下学期期中考试化学试题(已下线)第三章 水溶液中的离子反应与平衡(B卷·能力提升练)-【单元测试】2022-2023学年高二化学分层训练AB卷(人教版2019选择性必修1)(已下线)专题14 工艺流程选择题-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)
名校
2 . NA代表阿伏伽德罗常数的值,下列叙述错误 的是
①18 g金刚石中,碳碳共价键数为3NA
②1mol铜与足量硫蒸气反应,转移电子数为 NA
③常温常压时S2和S8的混合物共6.4g,其中所含硫原子数一定为0.2NA
④一定温度下,1 L 0.50 mol·L━1NH4Cl溶液与2 L 0.25mol·L━1NH4Cl溶液中NH4+的物质的量均小于0.5NA,且前者更少
⑤电解法精炼铜时,当阳极质量减少64g时,电路中通过的电子数一定为2NA
①18 g金刚石中,碳碳共价键数为3NA
②1mol铜与足量硫蒸气反应,转移电子数为 NA
③常温常压时S2和S8的混合物共6.4g,其中所含硫原子数一定为0.2NA
④一定温度下,1 L 0.50 mol·L━1NH4Cl溶液与2 L 0.25mol·L━1NH4Cl溶液中NH4+的物质的量均小于0.5NA,且前者更少
⑤电解法精炼铜时,当阳极质量减少64g时,电路中通过的电子数一定为2NA
| A.② | B.②④⑤ | C.④⑤ | D.②④ |
您最近一年使用:0次
2018-01-11更新
|
1322次组卷
|
2卷引用:【全国百强校】甘肃省兰州市第一中学2019届高三上学期12月月考化学试题
3 . 下列实验操作和现象对应的结论正确的是
| 选项 | 实验操作和现象 | 结 论 |
A | 向溶液X中滴加BaCl2溶液,有白色沉淀生成 | 溶液X中可能含有SO42- |
B | 2mL10%的CuSO4溶液中滴加2%的NaOH溶液4~6滴制得新制氢氧化铜,再滴加几滴葡萄糖溶液,加热 | 检验葡萄糖中含有醛基 |
C | 向1 mL浓度均为0.05 mol·L-l NaCl、NaI的混合溶液中滴加2滴0.01 mol·L-l AgNO3溶液,振荡,沉淀呈黄色 | Ksp (AgCl) |
D | 将Al2(SO4)3溶液蒸干、灼烧至恒重 | 最终剩余固体是Al2O3 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
4 . 金属及其化合物在生产中用途广泛。
Ⅰ.从含铜丰富的自然资源黄铜矿(CuFeS2)冶炼铜的工艺流程如下:
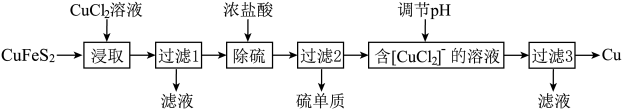
已知:CuFeS2+3CuCl2=4CuCl↓+FeCl2+2S↓
(1)浸取时,若改用FeCl3溶液,也能生成CuCl和S,该反应化学方程式为___________ 。
(2)若过滤1所得滤液中只含FeCl2,则将其在空气中加热蒸干、灼烧后,所得固体的化学式为___________ 。
(3)调节溶液的pH后,除生成Cu外,还能产生一种金属离子,此金属离子是___________ 。(填离子符号)
(4)过滤3所得滤液中可以循环使用的物质有____________ ,为保持流程持续循环,每生成1molCu,理论上需补充CuCl2的物质的量为____________ 。
Ⅱ.利用生产硼砂的废渣——硼镁泥(主要成分为MgCO3、SiO2,还含有少量Fe2O3、MnO、CaO等)为主要原料制取轻质碳酸镁[MgCO3·Mg(OH)2·2H2O]的工业流程如下:
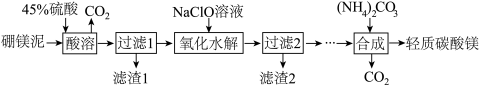
(5)写出“酸溶”一步中,MgCO3和硫酸反应的离子方程式_____________________ 。
(6)滤渣2的主要成分有MnO2和_____________ ,写出生成MnO2的离子方程式____________________ 。
(7)“合成”时需通蒸汽至80 ℃,边加热边搅拌,温度控制在80 ℃的原因是________________________ (只需写出相应的化学方程式)。
Ⅰ.从含铜丰富的自然资源黄铜矿(CuFeS2)冶炼铜的工艺流程如下:

已知:CuFeS2+3CuCl2=4CuCl↓+FeCl2+2S↓
(1)浸取时,若改用FeCl3溶液,也能生成CuCl和S,该反应化学方程式为
(2)若过滤1所得滤液中只含FeCl2,则将其在空气中加热蒸干、灼烧后,所得固体的化学式为
(3)调节溶液的pH后,除生成Cu外,还能产生一种金属离子,此金属离子是
(4)过滤3所得滤液中可以循环使用的物质有
Ⅱ.利用生产硼砂的废渣——硼镁泥(主要成分为MgCO3、SiO2,还含有少量Fe2O3、MnO、CaO等)为主要原料制取轻质碳酸镁[MgCO3·Mg(OH)2·2H2O]的工业流程如下:

(5)写出“酸溶”一步中,MgCO3和硫酸反应的离子方程式
(6)滤渣2的主要成分有MnO2和
(7)“合成”时需通蒸汽至80 ℃,边加热边搅拌,温度控制在80 ℃的原因是
您最近一年使用:0次
10-11高二下·浙江嘉兴·期中
名校
5 . 10℃时加热NaHCO3饱和溶液,测得该溶液的pH发生如下变化:
(1)甲同学认为,该溶液的pH升高的原因是HCO3-水解程度增大,故碱性增强,该反应的离子方程式为______________________ 。乙同学认为,溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度________ NaHCO3(填“大于”或“小于”)。丙同学认为甲、乙的判断都不充分,丙认为:
(2)只要在加热煮沸的溶液中加入足量的试剂X,若产生沉淀,则________ (填“甲”或“乙”)判断正确。试剂X是________ (填选项)。
(3)查阅资料发现NaHCO3的分解温度为150℃,丙断言________ (填“甲”或“乙”)判断是错误的,理由是________________________________________________ 。
| 温度/℃ | 10 | 20 | 30 | 加热煮沸后冷却到50℃ |
| pH | 8.3 | 8.4 | 8.5 | 8.8 |
(1)甲同学认为,该溶液的pH升高的原因是HCO3-水解程度增大,故碱性增强,该反应的离子方程式为
(2)只要在加热煮沸的溶液中加入足量的试剂X,若产生沉淀,则
| A.Ba(OH)2溶液 | B.BaCl2溶液 |
| C.NaOH溶液 | D.澄清的石灰水 |
(3)查阅资料发现NaHCO3的分解温度为150℃,丙断言
您最近一年使用:0次
2016-01-14更新
|
175次组卷
|
9卷引用:2011-2012学年甘肃省白银市平川中恒学校高二上学期期末考试化学(理)试卷
(已下线)2011-2012学年甘肃省白银市平川中恒学校高二上学期期末考试化学(理)试卷(已下线)2010—2011学年浙江省嘉兴一中高二下学期期中考试化学试卷(已下线)2010-2011年云南省玉溪一中高二下学期期末考试化学试卷(已下线)2011-2012学年山东省莘县实验高中高二上学期期中考试化学试卷(已下线)2011-2012学年福建省罗源一中高二上学期期末考试化学试卷陕西省西安市第一中学2015-2016学年高二上12月月考化学试卷福建省莆田第一中学2017-2018学年高二上学期期末考试化学试题【全国百强校】福建省上杭县第一中学2018-2019学年高二上学期12月月考化学试题贵州省岑巩县第二中学2019-2020学年高二上学期期末考试化学试题



