名校
解题方法
1 . 根据要求回答下列问题:
(1)生活中明矾常作净水剂,其净水的原理是___ (用离子方程式表示)。
(2)在25℃时,pH等于9和pH等于11的两种氢氧化钠溶液等体积混合后(忽略溶液体积的变化),溶液中的氢离子浓度为___ 。
(3)现将0.2mol·L-1的NH3·H2O溶液与0.1mol·L-1的HCl溶液等体积混合,写出该混合溶液质子守恒式:___ 。
(4)FeCl2溶液蒸干并灼烧得到的物质是___ (填化学式)。
(5)浓度均为0.1mol•L﹣1的①H2S、②NaHS、③Na2S、④H2S和NaHS混合液,溶液pH从大到小的顺序是___ 。(用序号表示)
(6)在常温下,现有下列四种溶液:①0.1mol·L-1 CH3COONH4溶液,②0.1mol·L-1NH4HSO4溶液,③0.1mol·L-1 NH3·H2O和0.1mol·L-1 NH4Cl混合溶液,④0.1mol·L-1 NH3·H2O溶液。比较①、②、③、④溶液中c(NH4+)由小到大的顺序为___ (用序号表示)
(1)生活中明矾常作净水剂,其净水的原理是
(2)在25℃时,pH等于9和pH等于11的两种氢氧化钠溶液等体积混合后(忽略溶液体积的变化),溶液中的氢离子浓度为
(3)现将0.2mol·L-1的NH3·H2O溶液与0.1mol·L-1的HCl溶液等体积混合,写出该混合溶液质子守恒式:
(4)FeCl2溶液蒸干并灼烧得到的物质是
(5)浓度均为0.1mol•L﹣1的①H2S、②NaHS、③Na2S、④H2S和NaHS混合液,溶液pH从大到小的顺序是
(6)在常温下,现有下列四种溶液:①0.1mol·L-1 CH3COONH4溶液,②0.1mol·L-1NH4HSO4溶液,③0.1mol·L-1 NH3·H2O和0.1mol·L-1 NH4Cl混合溶液,④0.1mol·L-1 NH3·H2O溶液。比较①、②、③、④溶液中c(NH4+)由小到大的顺序为
您最近一年使用:0次
名校
解题方法
2 . 下列实验能达到预期目的的是( )
| 选项 | 实验内容 | 实验目的 |
| A | 室温下,用pH试纸分别测定浓度均为0.1mol·L-1的NaClO溶液和CH3COONa溶液的pH | 比较HClO和CH3COOH的酸性强弱 |
| B | 将FeCl3饱和溶液滴加到沸腾的蒸馏水中,加热至溶液呈红褐色 | 制备Fe(OH)3胶体 |
| C | 常温下,测得饱和溶液的pH:NaA>NaB | 证明常温下的水解程度:A- <B- |
| D | 等体积、pH均为2的HA和HB两种酸分别与足量Zn 反应,HA放出的H2多 | 证明HA是强酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
3 . 已知某温度下水的离子积常数为Kw,下列溶液一定呈中性的是( )
| A.pH=7的溶液 | B.c(H+)=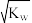 mol·L-1的溶液 mol·L-1的溶液 |
| C.由强酸、强碱等物质的量反应得到的溶液 | D.非电解质溶于水得到的溶液 |
您最近一年使用:0次
名校
解题方法
4 . 下列事实:①NaHSO4溶液呈酸性;②长期使用化肥(NH4)2SO4会使土壤酸性增大,发生板结;③配制CuCl2溶液,用稀盐酸溶解CuCl2固体;④NaHS溶液中c(H2S)>c(S2-);⑤氯化铵溶液可去除金属制品表面的锈斑。其中与盐类的水解有关的叙述有( )
| A.6项 | B.5项 | C.3项 | D.4项 |
您最近一年使用:0次
名校
5 . 把三氯化铁溶液蒸干灼烧,最后得到固体产物是
| A.无水三氯化铁 | B.氢氧化铁 | C.氧化亚铁 | D.三氧化二铁 |
您最近一年使用:0次
2016-12-09更新
|
162次组卷
|
7卷引用:新疆博尔塔拉蒙古自治州第五师高级中学2019-2020学年高二上学期期中考试化学试题



