1 . 某研究小组拟在实验室以废铁屑(含有少量炭和 杂质)为原料制备无水
杂质)为原料制备无水 ,设计如下流程(已知
,设计如下流程(已知 易水解):
易水解):不正确 的是
 杂质)为原料制备无水
杂质)为原料制备无水 ,设计如下流程(已知
,设计如下流程(已知 易水解):
易水解):
| A.试剂X可选用硫酸 |
B.“氧化”时: |
| C.操作①②均需用到漏斗、烧杯、玻璃棒 |
| D.“脱水”时可能会产生亚铁盐 |
您最近一年使用:0次
2024·内蒙古呼和浩特·二模
名校
2 . 三氯三(四氢呋喃)合铬(Ⅲ) 可催化烯烃加聚,制备的方法加下。
可催化烯烃加聚,制备的方法加下。
已知:① 易潮解,易升华,高温下易被氧气氧化。
易潮解,易升华,高温下易被氧气氧化。
② 气体有毒,遇水发生水解产生两种酸性气体。
气体有毒,遇水发生水解产生两种酸性气体。
Ⅰ.制备无水 :
:
某化学小组用 (沸点76.8℃)和
(沸点76.8℃)和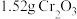 在高温下制备无水
在高温下制备无水 ,同时生成
,同时生成 气体,实验装置如图所示:
气体,实验装置如图所示: ,实验装置合理的连接顺序为A→G-→F→
,实验装置合理的连接顺序为A→G-→F→_______ →B(填装置字母标号,可重复使用)。
(2)装置乙名称为_______ ,装置D中粗导管的作用是_______ 。
(3)尾气处理时发生反应的离子方程式:_______ 。
Ⅱ.合成 :
: 原理为:
原理为:
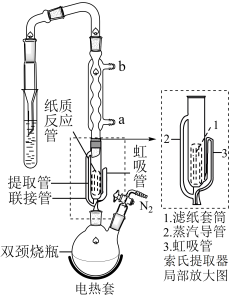
实验操作:按如图组装仪器,将步骤Ⅰ所得无水 和
和 锌粉放入滤纸套筒内,双颈烧瓶中加入
锌粉放入滤纸套筒内,双颈烧瓶中加入 无水四氢呋喃(THF),通
无水四氢呋喃(THF),通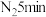 后关闭,接通冷却水,加热四氢呋喃至沸腾,在索氏提取器中发生反应,回流
后关闭,接通冷却水,加热四氢呋喃至沸腾,在索氏提取器中发生反应,回流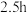 后再通入
后再通入 冷却至室温;取下双颈烧瓶,在通风橱中蒸发至有较多固体析出,冷却、抽滤、干燥后称量即得产品
冷却至室温;取下双颈烧瓶,在通风橱中蒸发至有较多固体析出,冷却、抽滤、干燥后称量即得产品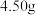 。
。_______ 。
(5)产品沿索氏提取器的管_______ (2或3)流回双颈烧瓶。
(6)已知Cr(Ⅱ)对该反应有催化作用,推断加入Zn粉发生反应的化学方程式为:_______ 。
(7)实验所用的四氢呋喃需进行无水处理,下列可以除去四氢呋喃中少量水分的试剂是_______ 。
A.金属钠 B.浓硫酸 C.具有吸水能力的分子筛
(8)产品产率为____ %(结果保留小数点后一位)[已知: 的摩尔质量为
的摩尔质量为 ;
; 的摩尔质量为
的摩尔质量为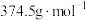 ]。
]。
 可催化烯烃加聚,制备的方法加下。
可催化烯烃加聚,制备的方法加下。已知:①
 易潮解,易升华,高温下易被氧气氧化。
易潮解,易升华,高温下易被氧气氧化。②
 气体有毒,遇水发生水解产生两种酸性气体。
气体有毒,遇水发生水解产生两种酸性气体。Ⅰ.制备无水
 :
:某化学小组用
 (沸点76.8℃)和
(沸点76.8℃)和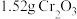 在高温下制备无水
在高温下制备无水 ,同时生成
,同时生成 气体,实验装置如图所示:
气体,实验装置如图所示: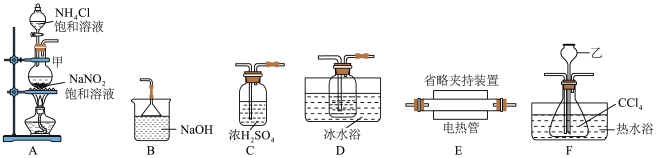
 ,实验装置合理的连接顺序为A→G-→F→
,实验装置合理的连接顺序为A→G-→F→(2)装置乙名称为
(3)尾气处理时发生反应的离子方程式:
Ⅱ.合成
 :
:①四氢呋喃(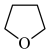 THF)为常见的有机溶剂,沸点66℃,易燃。
THF)为常见的有机溶剂,沸点66℃,易燃。
 原理为:
原理为:
实验操作:按如图组装仪器,将步骤Ⅰ所得无水
 和
和 锌粉放入滤纸套筒内,双颈烧瓶中加入
锌粉放入滤纸套筒内,双颈烧瓶中加入 无水四氢呋喃(THF),通
无水四氢呋喃(THF),通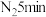 后关闭,接通冷却水,加热四氢呋喃至沸腾,在索氏提取器中发生反应,回流
后关闭,接通冷却水,加热四氢呋喃至沸腾,在索氏提取器中发生反应,回流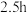 后再通入
后再通入 冷却至室温;取下双颈烧瓶,在通风橱中蒸发至有较多固体析出,冷却、抽滤、干燥后称量即得产品
冷却至室温;取下双颈烧瓶,在通风橱中蒸发至有较多固体析出,冷却、抽滤、干燥后称量即得产品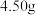 。
。
(5)产品沿索氏提取器的管
(6)已知Cr(Ⅱ)对该反应有催化作用,推断加入Zn粉发生反应的化学方程式为:
(7)实验所用的四氢呋喃需进行无水处理,下列可以除去四氢呋喃中少量水分的试剂是
A.金属钠 B.浓硫酸 C.具有吸水能力的分子筛
(8)产品产率为
 的摩尔质量为
的摩尔质量为 ;
; 的摩尔质量为
的摩尔质量为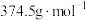 ]。
]。
您最近一年使用:0次
解题方法
3 . 下列有关离子方程式书写错误的是
A.用纯碱溶液浸泡锅炉水垢(CaSO4):CaSO4(s)+ (aq) (aq)  (aq)+CaCO3(s) (aq)+CaCO3(s) |
B.泡沫灭火器工作原理:Al3++3 =Al(OH)3↓+3CO2↑ =Al(OH)3↓+3CO2↑ |
C.纯碱溶液去除油污: +H2O +H2O  +OH- +OH- |
D.明矾净水的原理:Al3++3H2O Al(OH)3↓+3H+ Al(OH)3↓+3H+ |
您最近一年使用:0次
解题方法
4 . 久置的硝酸银溶液,试剂瓶底部有黑色固体A,瓶口和瓶壁上有黑色固体B。
已知:①硝酸银见光或受热会分解,分解产物相同。
②氧化银为棕黑色粉末,难溶于水,可溶于氨水和稀硝酸,见光或200℃左右分解生成氧气。
③AgOH不稳定,极易分解生成 和
和 。
。
某兴趣小组开展以下探究活动。
Ⅰ.探究硝酸银固体受热分解的产物
利用下列装置(夹持仪器略去)进行实验。
(1)仪器e名称为___________ ,试管b的主要作用是___________ 。
(2)试管a中反应的化学方程式为___________ 。
Ⅱ.探究A、B的成分
【提出猜想】甲、乙同学猜想固体中含有Ag、 中的一种或两种。
中的一种或两种。
(3)从化学变化角度,甲、乙同学猜想固体中可能含有 的依据是
的依据是___________ 。
【进行实验】甲、乙分别对固体A、B按以下步骤进行实验。
i.取少量固体于试管中;
ii.加入过量氨水,振荡;
iii.……
【形成结论】甲得出固体A为Ag和 的混合物,乙得出固体B为Ag。
的混合物,乙得出固体B为Ag。
(4)①甲同学步骤ⅱ观察到的现象为___________ ,相应的化学方程式为___________ 。
②乙同学步骤ⅲ加入的试剂为___________ (填名称)。
【反思与应用】
(5)固体A与固体B成分不同的可能原因是___________ 。
(6)实验室保存硝酸银溶液采取的措施为___________ (写出两条)。
已知:①硝酸银见光或受热会分解,分解产物相同。
②氧化银为棕黑色粉末,难溶于水,可溶于氨水和稀硝酸,见光或200℃左右分解生成氧气。
③AgOH不稳定,极易分解生成
 和
和 。
。某兴趣小组开展以下探究活动。
Ⅰ.探究硝酸银固体受热分解的产物
利用下列装置(夹持仪器略去)进行实验。

(1)仪器e名称为
(2)试管a中反应的化学方程式为
Ⅱ.探究A、B的成分
【提出猜想】甲、乙同学猜想固体中含有Ag、
 中的一种或两种。
中的一种或两种。(3)从化学变化角度,甲、乙同学猜想固体中可能含有
 的依据是
的依据是【进行实验】甲、乙分别对固体A、B按以下步骤进行实验。
i.取少量固体于试管中;
ii.加入过量氨水,振荡;
iii.……
【形成结论】甲得出固体A为Ag和
 的混合物,乙得出固体B为Ag。
的混合物,乙得出固体B为Ag。(4)①甲同学步骤ⅱ观察到的现象为
②乙同学步骤ⅲ加入的试剂为
【反思与应用】
(5)固体A与固体B成分不同的可能原因是
(6)实验室保存硝酸银溶液采取的措施为
您最近一年使用:0次
2024-04-01更新
|
454次组卷
|
5卷引用:福建省莆田市2024届高三下学期毕业班二模考试化学试题
福建省莆田市2024届高三下学期毕业班二模考试化学试题(已下线)题型9 实验综合题(25题)-2024年高考化学常考点必杀300题(新高考通用)2024届陕西省渭南市临渭区高三下学期三模理综试题-高中化学2024届陕西省渭南市富平县高三下学期二模理综试题-高中化学(已下线)压轴题12?化学实验综合题(5大题型+方法总结+压轴题速练)-2024年高考化学压轴题专项训练(新高考通用)
解题方法
5 . 化学与生活密切相关,下列说法错误的是
| A.热的碳酸钠溶液可用于去除餐具的油污 |
| B.燃烧木柴时,采用较细木材并将木柴架空 |
| C.明矾可用作净水剂 |
| D.一次性干电池的工作原理是电能转化为化学能 |
您最近一年使用:0次
6 . 中华文化源远流长,化学与文化传承密不可分。下列说法错误的是
| A.大米酿酒过程中碳元素易被还原 |
B.“白青 得铁化为铜”,其中的“白青”属于盐 得铁化为铜”,其中的“白青”属于盐 |
C.古陶瓷修复所用的熟石膏,其化学成分为 |
D.“盖此矾色绿,味酸,烧之则赤”,“味酸”是因绿矾水解产生 |
您最近一年使用:0次
7 . 中华文化源远流长,化学与文化传承密不可分。下列说法错误的是
| A.闻名世界的秦兵马俑是陶制品,由黏土经高温烧结而成,其属于无机非金属材料 |
B.“白青 得铁化为铜”,其中白青属于盐 得铁化为铜”,其中白青属于盐 |
C.“盖此矾色绿,味酸,烧之则赤”,“味酸”是因绿矾水解产生了 |
| D.四千余年前用谷物酿造出酒和醋,酿造过程只发生水解反应 |
您最近一年使用:0次
名校
解题方法
8 . 铂、镁在现代工业中有着极为重要的应用,某化工厂从含铂废料(主要成分为Pt,含少量MgO、Fe2O3、Al2O3、SiO2,表面沉积着有机物)中回收铂,并获得MgCl2•6H2O的工艺流程如图所示:
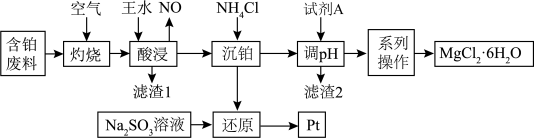
该工艺条件下,相关金属离子开始沉淀和完全沉淀时的pH如表:
(1)灼烧含铂废料最主要的目的是_______ 。
(2)滤渣1的主要成分为______ ,“沉铂”得到的沉淀(NH4)2PtCl6(氯铂酸铵)中铂元素的化合价为______ 。
(3)“还原”步骤中氯铂酸铵沉淀与Na2SO3溶液反应的主要离子方程式为_______ 。
(4)“试剂A”可选用______ ,pH的调控范围为______ 。
a.盐酸 b.NaOH溶液 c.氨水 d.MgO
(5)“系列操作”中最后的步骤为在HCl氛围中结晶,原因是_______ 。
(6)某小组为测定Na2SO3溶液浓度进行以下探究:取25.00mLNa2SO3样品溶液于锥形瓶中,滴入3~4滴稀硫酸酸化,用0.0200mol/LKMnO4标准溶液滴定,达到滴定终点的判断依据是当滴入最后半滴KMnO4标准溶液,锥形瓶中溶液由______ 。平行测定三次,平均消耗KMnO4标准溶液24.30mL,计算样品溶液中Na2SO3的浓度为______ mol/L。

该工艺条件下,相关金属离子开始沉淀和完全沉淀时的pH如表:
| Fe3+ | Al3+ | Mg2+ | |
| 开始沉淀 | 2.2 | 3.5 | 9.5 |
| 完全沉淀 | 3.2 | 4.7 | 11.1 |
(1)灼烧含铂废料最主要的目的是
(2)滤渣1的主要成分为
(3)“还原”步骤中氯铂酸铵沉淀与Na2SO3溶液反应的主要离子方程式为
(4)“试剂A”可选用
a.盐酸 b.NaOH溶液 c.氨水 d.MgO
(5)“系列操作”中最后的步骤为在HCl氛围中结晶,原因是
(6)某小组为测定Na2SO3溶液浓度进行以下探究:取25.00mLNa2SO3样品溶液于锥形瓶中,滴入3~4滴稀硫酸酸化,用0.0200mol/LKMnO4标准溶液滴定,达到滴定终点的判断依据是当滴入最后半滴KMnO4标准溶液,锥形瓶中溶液由
您最近一年使用:0次
名校
解题方法
9 . 化学与人类生活、生产息息相关。下列说法不正确 的是
| A.燃料电池的电极材料可以相同,也可以不相同 |
B.施肥时,草木灰(有效成分为 )不能与铵态氨肥混合使用 )不能与铵态氨肥混合使用 |
| C.漂白粉和明矾可用于水的处理,二者的作用原理不同 |
D.用氯气处理水中的 等重金属离子 等重金属离子 |
您最近一年使用:0次
名校
解题方法
10 . 下列实验装置或实验设计能达到相应实验目的的是
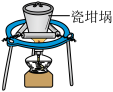
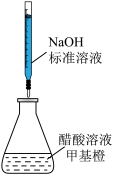
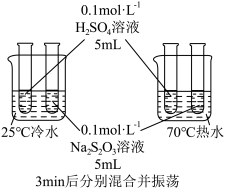
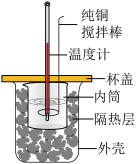
| 选项 | A | B | C | D |
| 实验装置 |
|
|
|
|
| 实验目的 | 蒸发浓缩含有少量稀盐酸的 溶液,获得 溶液,获得 晶体 晶体 | 测定醋酸溶液的浓度 | 探究温度对化学反应速率的影响 | 测定稀硫酸和 溶液发生中和反应的反应热 溶液发生中和反应的反应热 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-03-09更新
|
654次组卷
|
3卷引用:福建省福州市福建师范大学附属中学2024届高三一模化学试题