1 . 某研究小组拟在实验室以废铁屑(含有少量炭和 杂质)为原料制备无水
杂质)为原料制备无水 ,设计如下流程(已知
,设计如下流程(已知 易水解):
易水解):不正确 的是
 杂质)为原料制备无水
杂质)为原料制备无水 ,设计如下流程(已知
,设计如下流程(已知 易水解):
易水解):
| A.试剂X可选用硫酸 |
B.“氧化”时: |
| C.操作①②均需用到漏斗、烧杯、玻璃棒 |
| D.“脱水”时可能会产生亚铁盐 |
您最近一年使用:0次
2024·内蒙古呼和浩特·二模
名校
2 . 三氯三(四氢呋喃)合铬(Ⅲ) 可催化烯烃加聚,制备的方法加下。
可催化烯烃加聚,制备的方法加下。
已知:① 易潮解,易升华,高温下易被氧气氧化。
易潮解,易升华,高温下易被氧气氧化。
② 气体有毒,遇水发生水解产生两种酸性气体。
气体有毒,遇水发生水解产生两种酸性气体。
Ⅰ.制备无水 :
:
某化学小组用 (沸点76.8℃)和
(沸点76.8℃)和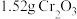 在高温下制备无水
在高温下制备无水 ,同时生成
,同时生成 气体,实验装置如图所示:
气体,实验装置如图所示: ,实验装置合理的连接顺序为A→C→F→
,实验装置合理的连接顺序为A→C→F→_______ →B(填装置字母标号,可重复使用)。
(2)装置乙名称为_______ ,装置D中粗导管的作用是_______ 。
(3)尾气处理时发生反应的离子方程式:_______ 。
Ⅱ.合成 :
: 原理为:
原理为:
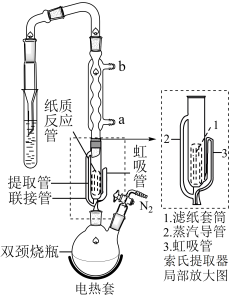
实验操作:按如图组装仪器,将步骤Ⅰ所得无水 和
和 锌粉放入滤纸套筒内,双颈烧瓶中加入
锌粉放入滤纸套筒内,双颈烧瓶中加入 无水四氢呋喃(THF),通
无水四氢呋喃(THF),通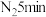 后关闭,接通冷却水,加热四氢呋喃至沸腾,在索氏提取器中发生反应,回流
后关闭,接通冷却水,加热四氢呋喃至沸腾,在索氏提取器中发生反应,回流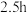 后再通入
后再通入 冷却至室温;取下双颈烧瓶,在通风橱中蒸发至有较多固体析出,冷却、抽滤、干燥后称量即得产品
冷却至室温;取下双颈烧瓶,在通风橱中蒸发至有较多固体析出,冷却、抽滤、干燥后称量即得产品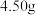 。
。_______ 。
(5)产品沿索氏提取器的管_______ (2或3)流回双颈烧瓶。
(6)已知Cr(Ⅱ)对该反应有催化作用,推断加入Zn粉发生反应的化学方程式为:_______ 。
(7)实验所用的四氢呋喃需进行无水处理,下列可以除去四氢呋喃中少量水分的试剂是_______ 。
A.金属钠 B.浓硫酸 C.具有吸水能力的分子筛
(8)产品产率为____ %(结果保留小数点后一位)[已知: 的摩尔质量为
的摩尔质量为 ;
; 的摩尔质量为
的摩尔质量为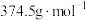 ]。
]。
 可催化烯烃加聚,制备的方法加下。
可催化烯烃加聚,制备的方法加下。已知:①
 易潮解,易升华,高温下易被氧气氧化。
易潮解,易升华,高温下易被氧气氧化。②
 气体有毒,遇水发生水解产生两种酸性气体。
气体有毒,遇水发生水解产生两种酸性气体。Ⅰ.制备无水
 :
:某化学小组用
 (沸点76.8℃)和
(沸点76.8℃)和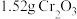 在高温下制备无水
在高温下制备无水 ,同时生成
,同时生成 气体,实验装置如图所示:
气体,实验装置如图所示: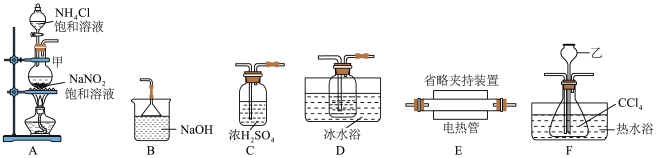
 ,实验装置合理的连接顺序为A→C→F→
,实验装置合理的连接顺序为A→C→F→(2)装置乙名称为
(3)尾气处理时发生反应的离子方程式:
Ⅱ.合成
 :
:①四氢呋喃(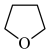 THF)为常见的有机溶剂,沸点66℃,易燃。
THF)为常见的有机溶剂,沸点66℃,易燃。
 原理为:
原理为:
实验操作:按如图组装仪器,将步骤Ⅰ所得无水
 和
和 锌粉放入滤纸套筒内,双颈烧瓶中加入
锌粉放入滤纸套筒内,双颈烧瓶中加入 无水四氢呋喃(THF),通
无水四氢呋喃(THF),通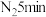 后关闭,接通冷却水,加热四氢呋喃至沸腾,在索氏提取器中发生反应,回流
后关闭,接通冷却水,加热四氢呋喃至沸腾,在索氏提取器中发生反应,回流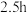 后再通入
后再通入 冷却至室温;取下双颈烧瓶,在通风橱中蒸发至有较多固体析出,冷却、抽滤、干燥后称量即得产品
冷却至室温;取下双颈烧瓶,在通风橱中蒸发至有较多固体析出,冷却、抽滤、干燥后称量即得产品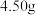 。
。
(5)产品沿索氏提取器的管
(6)已知Cr(Ⅱ)对该反应有催化作用,推断加入Zn粉发生反应的化学方程式为:
(7)实验所用的四氢呋喃需进行无水处理,下列可以除去四氢呋喃中少量水分的试剂是
A.金属钠 B.浓硫酸 C.具有吸水能力的分子筛
(8)产品产率为
 的摩尔质量为
的摩尔质量为 ;
; 的摩尔质量为
的摩尔质量为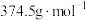 ]。
]。
您最近一年使用:0次
解题方法
3 . 久置的硝酸银溶液,试剂瓶底部有黑色固体A,瓶口和瓶壁上有黑色固体B。
已知:①硝酸银见光或受热会分解,分解产物相同。
②氧化银为棕黑色粉末,难溶于水,可溶于氨水和稀硝酸,见光或200℃左右分解生成氧气。
③AgOH不稳定,极易分解生成 和
和 。
。
某兴趣小组开展以下探究活动。
Ⅰ.探究硝酸银固体受热分解的产物
利用下列装置(夹持仪器略去)进行实验。
(1)仪器e名称为___________ ,试管b的主要作用是___________ 。
(2)试管a中反应的化学方程式为___________ 。
Ⅱ.探究A、B的成分
【提出猜想】甲、乙同学猜想固体中含有Ag、 中的一种或两种。
中的一种或两种。
(3)从化学变化角度,甲、乙同学猜想固体中可能含有 的依据是
的依据是___________ 。
【进行实验】甲、乙分别对固体A、B按以下步骤进行实验。
i.取少量固体于试管中;
ii.加入过量氨水,振荡;
iii.……
【形成结论】甲得出固体A为Ag和 的混合物,乙得出固体B为Ag。
的混合物,乙得出固体B为Ag。
(4)①甲同学步骤ⅱ观察到的现象为___________ ,相应的化学方程式为___________ 。
②乙同学步骤ⅲ加入的试剂为___________ (填名称)。
【反思与应用】
(5)固体A与固体B成分不同的可能原因是___________ 。
(6)实验室保存硝酸银溶液采取的措施为___________ (写出两条)。
已知:①硝酸银见光或受热会分解,分解产物相同。
②氧化银为棕黑色粉末,难溶于水,可溶于氨水和稀硝酸,见光或200℃左右分解生成氧气。
③AgOH不稳定,极易分解生成
 和
和 。
。某兴趣小组开展以下探究活动。
Ⅰ.探究硝酸银固体受热分解的产物
利用下列装置(夹持仪器略去)进行实验。

(1)仪器e名称为
(2)试管a中反应的化学方程式为
Ⅱ.探究A、B的成分
【提出猜想】甲、乙同学猜想固体中含有Ag、
 中的一种或两种。
中的一种或两种。(3)从化学变化角度,甲、乙同学猜想固体中可能含有
 的依据是
的依据是【进行实验】甲、乙分别对固体A、B按以下步骤进行实验。
i.取少量固体于试管中;
ii.加入过量氨水,振荡;
iii.……
【形成结论】甲得出固体A为Ag和
 的混合物,乙得出固体B为Ag。
的混合物,乙得出固体B为Ag。(4)①甲同学步骤ⅱ观察到的现象为
②乙同学步骤ⅲ加入的试剂为
【反思与应用】
(5)固体A与固体B成分不同的可能原因是
(6)实验室保存硝酸银溶液采取的措施为
您最近一年使用:0次
2024-04-01更新
|
607次组卷
|
5卷引用:福建省莆田市2024届高三下学期毕业班二模考试化学试题
福建省莆田市2024届高三下学期毕业班二模考试化学试题2024届陕西省渭南市临渭区高三下学期三模理综试题-高中化学2024届陕西省渭南市富平县高三下学期二模理综试题-高中化学(已下线)题型9 实验综合题(25题)-2024年高考化学常考点必杀300题(新高考通用)(已下线)压轴题12?化学实验综合题(5大题型+方法总结+压轴题速练)-2024年高考化学压轴题专项训练(新高考通用)
4 . 中华文化源远流长,化学与文化传承密不可分。下列说法错误的是
| A.大米酿酒过程中碳元素易被还原 |
B.“白青 得铁化为铜”,其中的“白青”属于盐 得铁化为铜”,其中的“白青”属于盐 |
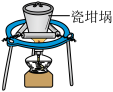
C.古陶瓷修复所用的熟石膏,其化学成分为 |
D.“盖此矾色绿,味酸,烧之则赤”,“味酸”是因绿矾水解产生 |
您最近一年使用:0次
名校
解题方法
5 . 下列实验装置或实验设计能达到相应实验目的的是
| 选项 | A | B | C | D |
| 实验装置 |
|
|
|
|
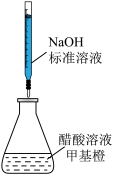
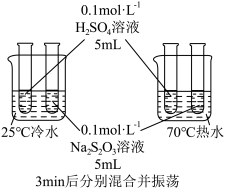
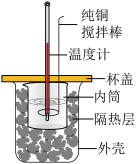
| 实验目的 | 蒸发浓缩含有少量稀盐酸的 溶液,获得 溶液,获得 晶体 晶体 | 测定醋酸溶液的浓度 | 探究温度对化学反应速率的影响 | 测定稀硫酸和 溶液发生中和反应的反应热 溶液发生中和反应的反应热 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-03-09更新
|
671次组卷
|
4卷引用:福建省福州市福建师范大学附属中学2024届高三一模化学试题
名校
6 . “实践出真知”。下列所述化学知识正确且与劳动项目有关联的是
选项 | 劳动项目 | 化学知识 |
A | 社区劳动:用含纯碱的去污粉擦拭餐具 |
|
B | 环保志愿者:公园捡拾塑料袋、废纸等集中处理 | 塑料、废纸均为难降解的高分子化合物 |
C | 帮厨劳动:用含 |
|
D | 田间宣传:田间不能焚烧农作物秸秆 | 秸秆焚烧产生 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-03-08更新
|
372次组卷
|
3卷引用:福建省福州市福建师范大学附属中学2024届高三一模化学试题
7 . 碳酸亚铁作为饲料中铁的补充剂,其干燥品在空气中稳定,湿品在空气中被氧化为氢氧化铁成茶色。用含少量 的废铁屑制取
的废铁屑制取 的流程如图所示:
的流程如图所示: 存在自偶电离:
存在自偶电离: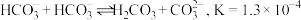 ;②
;② 的
的 ;③
;③ 开始沉淀的
开始沉淀的 。
。
下列说法正确的是
 的废铁屑制取
的废铁屑制取 的流程如图所示:
的流程如图所示: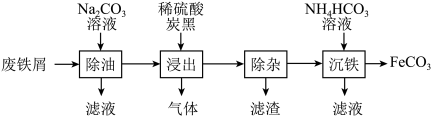
 存在自偶电离:
存在自偶电离: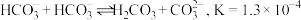 ;②
;② 的
的 ;③
;③ 开始沉淀的
开始沉淀的 。
。下列说法正确的是
| A.“浸出”时为了提高反应速率,可以把稀硫酸换成浓硫酸 |
B.“沉铁”过程中发生反应的离子方程式是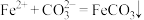 |
| C.“沉铁”过程中也可使用饱和碳酸钠溶液 |
| D.“沉铁”得到的碳酸亚铁过滤后要用无水乙醇洗涤、隔绝空气干燥 |
您最近一年使用:0次
2024-03-01更新
|
128次组卷
|
2卷引用:福建省厦门市国祺中学2023-2024学年高三下学期第二次模拟化学试题
8 . 下列有关离子方程式书写正确的是
A.明矾净水的原理: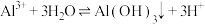 |
B.用小苏打治疗胃酸过多: |
C.用醋酸和碘化钾淀粉溶液检验加碘盐中的 : : |
D.用纯碱溶液浸泡锅炉水垢( ): ):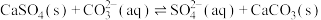 |
您最近一年使用:0次
9 . 化学可以提高人们的生活质量。下列相关方程式错误的是
A.氢氟酸雕刻玻璃: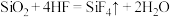 |
B.泡沫灭火器: |
C.制镜: |
D.管道疏通剂(苛性钠、铝粉): |
您最近一年使用:0次
2023-08-30更新
|
635次组卷
|
2卷引用:福建省泉州市普通高中毕业班2024届高三质量检测(一)(8月)化学试题
名校
解题方法
10 . 钴盐在生活和生产中有着重要应用。
(1)在活性炭的催化作用下,通过氧化CoCl2·6H2O制得到[Co(NH3)6]Cl3流程如下:
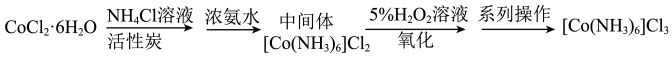
①在“氧化”过程,需水浴控温在50~60℃,温度不能过高,原因是:___________ 。“系列操作”是指在高浓度的盐酸中使[Co(NH3)6]Cl3结晶析出,过滤,醇洗,干燥。使用乙醇洗涤产品的具体操作是:___________ 。
②结束后废水中的Co2+,人们常用FeS沉淀剂来处理,原理是___________ (用离子方程式表示)。
(2)草酸钴是制备钴氧化物的重要原料,常用(NH4)2C2O4溶液和CoCl2溶液制取难溶于水的CoC2O4·2H2O晶体。
①常温下,(NH4)2C2O4溶液的pH___________ 7(填“>”、“=”或“<”)。(已知:常温下Kb(NH3·H2O)=1.8×10-5,H2C2O4:Ka1=5.6×10-2,Ka2=5.4×10-5)
②制取CoC2O4·2H2O晶体时,还需加入适量氨水,其作用是___________ 。
③在空气中加热10.98g二水合草酸钴(CoC2O4·2H2O),受热过程中在不同温度范围内分别得到一种固体物质。已知Co的两种常见化合价为+2价和+3价,M(CoC2O4·2H2O)=183g/mol。
i.温度在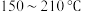 范围内,固体物质为
范围内,固体物质为___________ (填化学式);
ii.从 加热到
加热到 时生成一种钴的氧化物和CO2,此过程发生反应的化学方程式是
时生成一种钴的氧化物和CO2,此过程发生反应的化学方程式是______ 。
(1)在活性炭的催化作用下,通过氧化CoCl2·6H2O制得到[Co(NH3)6]Cl3流程如下:
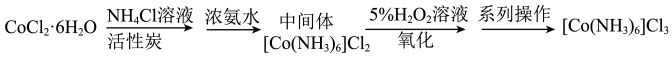
①在“氧化”过程,需水浴控温在50~60℃,温度不能过高,原因是:
②结束后废水中的Co2+,人们常用FeS沉淀剂来处理,原理是
(2)草酸钴是制备钴氧化物的重要原料,常用(NH4)2C2O4溶液和CoCl2溶液制取难溶于水的CoC2O4·2H2O晶体。
①常温下,(NH4)2C2O4溶液的pH
②制取CoC2O4·2H2O晶体时,还需加入适量氨水,其作用是
③在空气中加热10.98g二水合草酸钴(CoC2O4·2H2O),受热过程中在不同温度范围内分别得到一种固体物质。已知Co的两种常见化合价为+2价和+3价,M(CoC2O4·2H2O)=183g/mol。
| 温度范围/℃ | 150~210 | 290~320 |
| 固体质量/g | 8.82 | 4.82 |
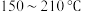 范围内,固体物质为
范围内,固体物质为ii.从
 加热到
加热到 时生成一种钴的氧化物和CO2,此过程发生反应的化学方程式是
时生成一种钴的氧化物和CO2,此过程发生反应的化学方程式是
您最近一年使用:0次
2023-07-28更新
|
297次组卷
|
4卷引用:福建省宁德市五校教学联合体2023届高三一模考试化学试题

 电离显碱性
电离显碱性 的发酵粉拌面,蒸制馒头
的发酵粉拌面,蒸制馒头
 等有毒气体
等有毒气体

