解题方法
1 . 利用如图装置和试剂进行实验(部分夹持装置略),能达到相应实验目的的是
| A | B |
|
|
| 制备并收集少量NO2 | 制备无水MgCl2 |
| C | D |
|
|
| 模拟“侯氏制碱法”制备NaHCO3 | 排出盛有酸性KMnO4溶液的滴定管尖嘴内的气泡 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2 . 化学和生活、科技、社会发展息息相关,下列说法正确的是
A.华为 手机芯片的关键材料是 手机芯片的关键材料是 |
B.用饱和苏打溶液去油污,加热可增强去污效果,是因为升温能促进 电离 电离 |
| C.工人将模具干燥后再注入熔融钢水,是因为高温下铁与水蒸气反应产生氢气 |
| D.碳纳米管是一种比表面积大的合成纤维,属于高分子化合物 |
您最近一年使用:0次
3 . 短周期元素X、Y、Z、W的原子序数依次增大,其中X、Y、Z三种元素形成的一种化合物的结构如图所示,Z元素的简单阴离子与W的简单阳离子具有相同的电子层结构。下列说法正确的是
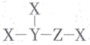
| A.原子半径:Y>Z>W |
| B.简单氢化物稳定性:Y>Z |
| C.W只能是Na、Mg两种元素 |
| D.W3Y2与X2Z反应可能产生有刺激性气味的气体 |
您最近一年使用:0次
名校
4 . 化学反应常伴随热效应。某些反应(如中和反应)的热量变化,其数值Q可通过量热装置测量反应前后体系温度的变化,用公式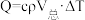 计算获得。(注:实验所用酸、碱、盐溶液的密度和比热容与水相同,忽略水以外各物质吸收的热量,忽略实验装置的比热容,c和
计算获得。(注:实验所用酸、碱、盐溶液的密度和比热容与水相同,忽略水以外各物质吸收的热量,忽略实验装置的比热容,c和 分别取4.18
分别取4.18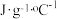 和1.0
和1.0 ,下同)请回答下列问题:
,下同)请回答下列问题:
(1)NaOH溶液浓度的测定:移取20.00mL待测液,加入指示剂,用0.5000 的盐酸溶液滴定至终点,消耗盐酸溶液22.00mL。在测定过程中,滴定操作的顺序为检查是否漏水→蒸馏水洗涤→
的盐酸溶液滴定至终点,消耗盐酸溶液22.00mL。在测定过程中,滴定操作的顺序为检查是否漏水→蒸馏水洗涤→___ (用序号表示)→滴定→达到滴定终点,停止滴定,记录读数。
a.轻轻转动滴定管的活塞,使滴定管尖嘴部分充满溶液,无气泡
b.调整管中液面至“0”或“0”刻度以下,记录读数
c.将洗涤液从滴定管下部放入预置的烧杯中
d.装入标准溶液至“0”刻度以上2~3mL,固定好滴定管
e.从滴定管上口加入3mL所要盛装的溶液,倾斜着转动滴定管
(2)热量的测定:取上述NaOH溶液和盐酸各50mL进行反应。
①实验室现有纸条、硬纸板(中心有两个小孔)、量筒、100mL烧杯,为了完成该实验,还需要图中的实验仪器是_______ (填序号)。 、
、 ,则该过程放出的热量为
,则该过程放出的热量为______ J(用含 、
、 的式子表示)。
的式子表示)。
(3)借鉴(2)的方法,甲同学测量放热反应: 的焓变
的焓变 (忽略温度对焓变的影响,下同)。实验结果见下表:
(忽略温度对焓变的影响,下同)。实验结果见下表:
温度:b、c、d的大小关系为_______ 。结果表明,该方法可行。
(4)乙同学也借鉴(2)的方法,测量反应A: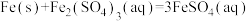 的焓变△H。
的焓变△H。
查阅资料:配制 溶液时需加入酸。
溶液时需加入酸。
提出猜想:Fe粉与 溶液混合,在反应A进行的过程中,可能存在反应B:
溶液混合,在反应A进行的过程中,可能存在反应B:_______ (填化学方程式)。
验证猜想:用pH试纸测得 溶液的pH不大于1;向少量
溶液的pH不大于1;向少量 溶液中加入Fe粉,观察到的现象为
溶液中加入Fe粉,观察到的现象为____ ,说明同时存在反应A和B。
实验小结:猜想成立,不能直接测得反应A的焓变 。
。
教师指导:结合甲同学的测定结果及盖斯定律可以计算无法直接测定的反应热。
优化设计:根据相关原理,丙同学还需要测定反应_______ (填化学方程式)的焓变 ,通过计算可得反应A的焓变
,通过计算可得反应A的焓变
______ (用含 和
和 的式子表示)。
的式子表示)。
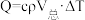 计算获得。(注:实验所用酸、碱、盐溶液的密度和比热容与水相同,忽略水以外各物质吸收的热量,忽略实验装置的比热容,c和
计算获得。(注:实验所用酸、碱、盐溶液的密度和比热容与水相同,忽略水以外各物质吸收的热量,忽略实验装置的比热容,c和 分别取4.18
分别取4.18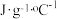 和1.0
和1.0 ,下同)请回答下列问题:
,下同)请回答下列问题:(1)NaOH溶液浓度的测定:移取20.00mL待测液,加入指示剂,用0.5000
 的盐酸溶液滴定至终点,消耗盐酸溶液22.00mL。在测定过程中,滴定操作的顺序为检查是否漏水→蒸馏水洗涤→
的盐酸溶液滴定至终点,消耗盐酸溶液22.00mL。在测定过程中,滴定操作的顺序为检查是否漏水→蒸馏水洗涤→a.轻轻转动滴定管的活塞,使滴定管尖嘴部分充满溶液,无气泡
b.调整管中液面至“0”或“0”刻度以下,记录读数
c.将洗涤液从滴定管下部放入预置的烧杯中
d.装入标准溶液至“0”刻度以上2~3mL,固定好滴定管
e.从滴定管上口加入3mL所要盛装的溶液,倾斜着转动滴定管
(2)热量的测定:取上述NaOH溶液和盐酸各50mL进行反应。
①实验室现有纸条、硬纸板(中心有两个小孔)、量筒、100mL烧杯,为了完成该实验,还需要图中的实验仪器是
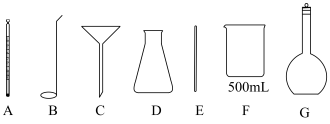
 、
、 ,则该过程放出的热量为
,则该过程放出的热量为 、
、 的式子表示)。
的式子表示)。(3)借鉴(2)的方法,甲同学测量放热反应:
 的焓变
的焓变 (忽略温度对焓变的影响,下同)。实验结果见下表:
(忽略温度对焓变的影响,下同)。实验结果见下表:| 序号 | 反应试剂 | 体系温度/℃ | ||
| 反应前 | 反应后 | |||
| ⅰ | 0.2  溶液100mL 溶液100mL | 0.56g铁粉 | a | b |
| ⅱ | 1.12g铁粉 | a | c | |
| ⅲ | 1.68g铁粉 | a | d | |
(4)乙同学也借鉴(2)的方法,测量反应A:
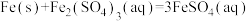 的焓变△H。
的焓变△H。查阅资料:配制
 溶液时需加入酸。
溶液时需加入酸。提出猜想:Fe粉与
 溶液混合,在反应A进行的过程中,可能存在反应B:
溶液混合,在反应A进行的过程中,可能存在反应B:验证猜想:用pH试纸测得
 溶液的pH不大于1;向少量
溶液的pH不大于1;向少量 溶液中加入Fe粉,观察到的现象为
溶液中加入Fe粉,观察到的现象为实验小结:猜想成立,不能直接测得反应A的焓变
 。
。教师指导:结合甲同学的测定结果及盖斯定律可以计算无法直接测定的反应热。
优化设计:根据相关原理,丙同学还需要测定反应
 ,通过计算可得反应A的焓变
,通过计算可得反应A的焓变
 和
和 的式子表示)。
的式子表示)。
您最近一年使用:0次
5 . 亚硫酰氯(SOCl2)常用作脱水剂,沸点79℃,140℃以上易分解,遇水剧烈反应生成 和HCl。实验室合成
和HCl。实验室合成 的原理之一是
的原理之一是 ,部分模拟装置如图所示。下列叙述正确的是
,部分模拟装置如图所示。下列叙述正确的是
 和HCl。实验室合成
和HCl。实验室合成 的原理之一是
的原理之一是 ,部分模拟装置如图所示。下列叙述正确的是
,部分模拟装置如图所示。下列叙述正确的是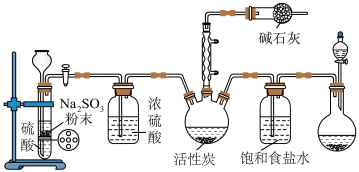
A.图中制 能实现“随开随用、随关随停” 能实现“随开随用、随关随停” |
B.碱石灰具有吸收多余 或 或 的作用 的作用 |
| C.整套装置设计并无不妥,能达成目的 |
D.可将 与 与 混合加热制取无水 混合加热制取无水 |
您最近一年使用:0次
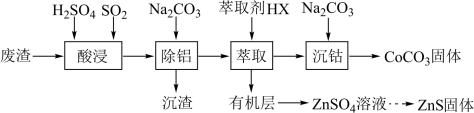
6 . CoCO3可用作选矿剂、催化剂及涂料的颜料。以含钴废渣(主要成分为CoO、Co2O3,还含有Al2O3、ZnO等杂质)为原料制备CoCO3的一种工艺流程如下:
(1)“酸浸”时需控制温度在40℃左右,原因是___________ 。
(2)“除铝”时发生反应的离子方程式为___________ 。
(3)上述“萃取”过程可表示为 。
。
①下列说法不正确的是___________ 。
A.可将废渣粉碎以提高酸浸效率
B.“除铝”时,应加入过量的Na2CO3溶液
C.可选择CCl4作为萃取剂
D.往萃取后的有机层中加水可获得ZnSO4溶液
②若萃取操作是在实验室完成,请选择合适的编号,按正确的操作顺序(有的操作可重复使用),完成萃取实验(假设只放气一次)。___________
倒入溶液和萃取剂→___________→___________→___________→___________→f→___________→___________→使下层液体慢慢流出→c→上层液体从上口倒出
a.打开分液漏斗上口玻璃塞;b.塞上分液漏斗上口玻璃塞;c.关闭分液漏斗旋塞;
d打开分液漏斗旋塞;e.倒转分液漏斗振摇;
f.将分液漏斗放在铁圈上静置;g.手持分液漏斗静置。
(4)“沉钴”时,溶液滴加过快会导致产品不纯,请解释可能原因___________ 。
(5)该工艺的副产物ZnS可参与H2S与CO2生成COS的反应,反应前后ZnS的质量不变,该过程中涉及到的化学反应有___________ 。
(6)在空气中煅烧CoCO3生成钴氧化物和CO2,测得充分煅烧后固体质量为2.41g,CO2的体积为0.672L(标准状况),则该钴氧化物的化学式为___________ 。
(1)“酸浸”时需控制温度在40℃左右,原因是
(2)“除铝”时发生反应的离子方程式为
(3)上述“萃取”过程可表示为
 。
。①下列说法不正确的是
A.可将废渣粉碎以提高酸浸效率
B.“除铝”时,应加入过量的Na2CO3溶液
C.可选择CCl4作为萃取剂
D.往萃取后的有机层中加水可获得ZnSO4溶液
②若萃取操作是在实验室完成,请选择合适的编号,按正确的操作顺序(有的操作可重复使用),完成萃取实验(假设只放气一次)。
倒入溶液和萃取剂→___________→___________→___________→___________→f→___________→___________→使下层液体慢慢流出→c→上层液体从上口倒出
a.打开分液漏斗上口玻璃塞;b.塞上分液漏斗上口玻璃塞;c.关闭分液漏斗旋塞;
d打开分液漏斗旋塞;e.倒转分液漏斗振摇;
f.将分液漏斗放在铁圈上静置;g.手持分液漏斗静置。
(4)“沉钴”时,溶液滴加过快会导致产品不纯,请解释可能原因
(5)该工艺的副产物ZnS可参与H2S与CO2生成COS的反应,反应前后ZnS的质量不变,该过程中涉及到的化学反应有
(6)在空气中煅烧CoCO3生成钴氧化物和CO2,测得充分煅烧后固体质量为2.41g,CO2的体积为0.672L(标准状况),则该钴氧化物的化学式为
您最近一年使用:0次
解题方法
7 . 掌握化学知识,助力乡村振兴。下列相关说法错误的是
| A.施加熟石灰可改良酸性土壤,提高土壤pH值 |
| B.为防止肥效降低,不可将草木灰和铵态氮肥混合施用 |
| C.向果蔬中通入乙烯可达到延长保鲜时间的目的 |
| D.向污水中加入可溶性铁盐或铝盐可实现污水净化 |
您最近一年使用:0次
解题方法
8 . 贵金属银有广泛用途。工业上用银锰精矿(主要含 、MnS、
、MnS、 等)制备银,同时获得二氧化锰的流程如下。
等)制备银,同时获得二氧化锰的流程如下。
(1)“浸锰”步骤中产生的浸锰液主要含有 ,生成气体的主要成分为
,生成气体的主要成分为_______ ;用惰性电极电解浸锰液制 ,写出电解总反应的化学方程式
,写出电解总反应的化学方程式_______ 。
(2)已知“浸铁”步骤中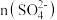 保持不变,反应中n(氧化剂):n(还原剂)=
保持不变,反应中n(氧化剂):n(还原剂)=_______ ;浸铁滤饼的主要成分为S和_______ 。
(3)“浸银”时发生反应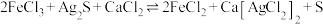 ,其中
,其中 在溶液中是一种稳定配合物。加入
在溶液中是一种稳定配合物。加入 的作用是
的作用是_______ ;结合离子方程式,从平衡角度分析选用氯化物浓溶液的原因是_______ 。
(4)“沉银”步骤中,生成单质银的离子反应方程式为_______ ,沉银液经处理可再利用,方法是向沉银液中通入_______ (写化学式),通过一步转化后循环再用。
 、MnS、
、MnS、 等)制备银,同时获得二氧化锰的流程如下。
等)制备银,同时获得二氧化锰的流程如下。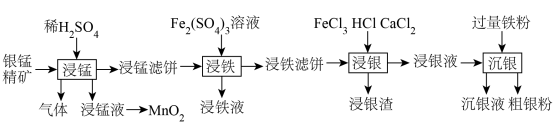
(1)“浸锰”步骤中产生的浸锰液主要含有
 ,生成气体的主要成分为
,生成气体的主要成分为 ,写出电解总反应的化学方程式
,写出电解总反应的化学方程式(2)已知“浸铁”步骤中
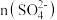 保持不变,反应中n(氧化剂):n(还原剂)=
保持不变,反应中n(氧化剂):n(还原剂)=(3)“浸银”时发生反应
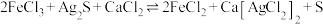 ,其中
,其中 在溶液中是一种稳定配合物。加入
在溶液中是一种稳定配合物。加入 的作用是
的作用是(4)“沉银”步骤中,生成单质银的离子反应方程式为
您最近一年使用:0次
名校
解题方法
9 .  为无色结晶,有毒;水中的溶解度为35.7g(20℃)、58.7g(100℃)。实验室用毒重石(主要含
为无色结晶,有毒;水中的溶解度为35.7g(20℃)、58.7g(100℃)。实验室用毒重石(主要含 ,及少量
,及少量 、
、 、
、 等杂质)经过加工处理,可制得
等杂质)经过加工处理,可制得 晶体。其实验步骤如下:
晶体。其实验步骤如下:
I.样品分解:称取a g毒重石矿粉于烧杯中,加入稍过量的 溶液,90℃下加热搅拌2h,待充分反应后,冷却,过滤。
溶液,90℃下加热搅拌2h,待充分反应后,冷却,过滤。
II.除 :向滤液中加入一定量的BaS溶液,有黑色沉淀生成,过滤。
:向滤液中加入一定量的BaS溶液,有黑色沉淀生成,过滤。
III.结晶:将步骤II的 滤液经过___________,___________,抽滤,用冷水和乙醇各洗涤晶体2~3次,自然晾干。
滤液经过___________,___________,抽滤,用冷水和乙醇各洗涤晶体2~3次,自然晾干。
回答下列问题:
(1)步骤I中,观察到的实验现象有___________ 。
(2)步骤II检验 是否完全沉淀的方法是
是否完全沉淀的方法是___________ ;在过滤中,下列仪器必需用到的是___________ (填仪器名称),与普通过滤相比,步骤III抽滤的优点是___________ 。___________ ,___________ ,抽滤”。
(4)样品分解时,不选用酸性更强且等量的盐酸溶液替代 溶液,可能的原因是
溶液,可能的原因是___________ 。
(5) 纯度的测定
纯度的测定
某学生查阅资料: ,X代表
,X代表 ,
, 、
、 等,
等, 代表
代表 的阴离子,设计如下纯度测量方案:
的阴离子,设计如下纯度测量方案:
步骤I.准确称取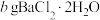 粗品并用20.0mL水溶解。
粗品并用20.0mL水溶解。
步骤II.用 的
的 标准溶液滴定其中的
标准溶液滴定其中的
步骤III.重复滴定2~3次,记录每次消耗 标准溶液的体积
标准溶液的体积
①滴定时采用下图所示的侧边自动定零位滴定管,结合该装置的使用说明书分析其优点___________ 。 含量的测定值偏高的是
含量的测定值偏高的是___________ (填序号)。
a.未干燥锥形瓶 b. 标准溶液久置部分失效
标准溶液久置部分失效
c.滴定终点时滴定管尖嘴中产生气泡 d.杂质可与 反应
反应
 为无色结晶,有毒;水中的溶解度为35.7g(20℃)、58.7g(100℃)。实验室用毒重石(主要含
为无色结晶,有毒;水中的溶解度为35.7g(20℃)、58.7g(100℃)。实验室用毒重石(主要含 ,及少量
,及少量 、
、 、
、 等杂质)经过加工处理,可制得
等杂质)经过加工处理,可制得 晶体。其实验步骤如下:
晶体。其实验步骤如下:I.样品分解:称取a g毒重石矿粉于烧杯中,加入稍过量的
 溶液,90℃下加热搅拌2h,待充分反应后,冷却,过滤。
溶液,90℃下加热搅拌2h,待充分反应后,冷却,过滤。II.除
 :向滤液中加入一定量的BaS溶液,有黑色沉淀生成,过滤。
:向滤液中加入一定量的BaS溶液,有黑色沉淀生成,过滤。III.结晶:将步骤II的
 滤液经过___________,___________,抽滤,用冷水和乙醇各洗涤晶体2~3次,自然晾干。
滤液经过___________,___________,抽滤,用冷水和乙醇各洗涤晶体2~3次,自然晾干。回答下列问题:
(1)步骤I中,观察到的实验现象有
(2)步骤II检验
 是否完全沉淀的方法是
是否完全沉淀的方法是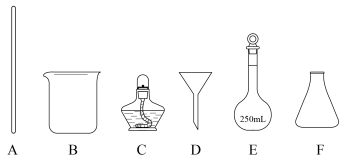
(4)样品分解时,不选用酸性更强且等量的盐酸溶液替代
 溶液,可能的原因是
溶液,可能的原因是(5)
 纯度的测定
纯度的测定某学生查阅资料:
 ,X代表
,X代表 ,
, 、
、 等,
等, 代表
代表 的阴离子,设计如下纯度测量方案:
的阴离子,设计如下纯度测量方案:步骤I.准确称取
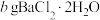 粗品并用20.0mL水溶解。
粗品并用20.0mL水溶解。步骤II.用
 的
的 标准溶液滴定其中的
标准溶液滴定其中的
步骤III.重复滴定2~3次,记录每次消耗
 标准溶液的体积
标准溶液的体积①滴定时采用下图所示的侧边自动定零位滴定管,结合该装置的使用说明书分析其优点
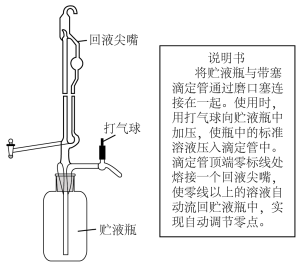
 含量的测定值偏高的是
含量的测定值偏高的是a.未干燥锥形瓶 b.
 标准溶液久置部分失效
标准溶液久置部分失效c.滴定终点时滴定管尖嘴中产生气泡 d.杂质可与
 反应
反应
您最近一年使用:0次
2024-03-29更新
|
239次组卷
|
3卷引用:2024届四川省雅安市、遂宁市、眉山市高三第二次诊断性考试理科综合试题-高中化学
2024届四川省雅安市、遂宁市、眉山市高三第二次诊断性考试理科综合试题-高中化学四川省乐山市2024届高三第二次调查研究考试理科综合-化学试题(已下线)湖南省长沙市第一中学2023-2024学年高三下学期三模化学试题
10 . 化学为满足人民日益增长的美好生活需要做出突出贡献。下列说法不合理的是
| A.FAST用到的碳化硅是一种无机非金属材料 |
| B.硫酸铁用于净水是利用其强氧化性进行杀菌消毒 |
| C.乙烯可以用作水果的催熟剂,以使水果尽快成熟 |
| D.“深海一号”从深海中开采的石油和天然气都属于混合物 |
您最近一年使用:0次
2024-03-29更新
|
283次组卷
|
3卷引用:2024届四川省雅安市、遂宁市、眉山市高三第二次诊断性考试理科综合试题-高中化学







