1 . 某学习小组对“ 溶液的灼烧”进行实验探究。回答下列问题:
溶液的灼烧”进行实验探究。回答下列问题:
(1)如图所示将浸泡过 溶液的粉笔夹持于酒精灯上灼烧,加热过程中观察到粉笔表面颜色变化:黄色→红褐色→铁锈色→黑色。
溶液的粉笔夹持于酒精灯上灼烧,加热过程中观察到粉笔表面颜色变化:黄色→红褐色→铁锈色→黑色。 溶液的操作为先加
溶液的操作为先加____________ 溶解 ,再稀释至所需浓度。
,再稀释至所需浓度。
②用化学方程式解释粉笔表面出现红褐色的原因:________________ 。
③溶液变铁锈色是因为生成了______________ (填化学式)。
(2)针对粉笔表面颜色最终变为黑色的现象,设计实验探究黑色物质成分。
查阅资料: 是一种黑色粉末,不稳定,在空气中加热可被氧化为
是一种黑色粉末,不稳定,在空气中加热可被氧化为 ;隔绝空气加热歧化为
;隔绝空气加热歧化为 和
和 。
。
提出猜想:
猜想1:酒精与粉笔灼烧的产物;
猜想2:酒精还原铁锈色物质而得到的产物。
实验设计:
①实验1:利用一个简单的操作证明猜想1不成立,实验操作为________________ ,未呈现黑色。
②实验2:如图所示密闭装置中,先在浸泡过酒精的粉笔处加热,再在铁锈色物质处加热,观察到铁锈色物质变为黑色后持续加热 ,取下试管加热,观察到有砖红色沉淀产生,先在粉笔处加热的目的是
,取下试管加热,观察到有砖红色沉淀产生,先在粉笔处加热的目的是_______________ 。
限选试剂:黑色粉末样品、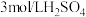 溶液、
溶液、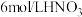 溶液、
溶液、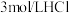 溶液、
溶液、 酸性
酸性 溶液、
溶液、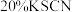 溶液、蒸馏水。
溶液、蒸馏水。
(4)由以上实验测得黑色粉末中铁元素的质量分数为_______________ (已知实验条件下所得 固体中
固体中 与
与 个数比为
个数比为 )。
)。
 溶液的灼烧”进行实验探究。回答下列问题:
溶液的灼烧”进行实验探究。回答下列问题:(1)如图所示将浸泡过
 溶液的粉笔夹持于酒精灯上灼烧,加热过程中观察到粉笔表面颜色变化:黄色→红褐色→铁锈色→黑色。
溶液的粉笔夹持于酒精灯上灼烧,加热过程中观察到粉笔表面颜色变化:黄色→红褐色→铁锈色→黑色。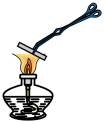
 溶液的操作为先加
溶液的操作为先加 ,再稀释至所需浓度。
,再稀释至所需浓度。②用化学方程式解释粉笔表面出现红褐色的原因:
③溶液变铁锈色是因为生成了
(2)针对粉笔表面颜色最终变为黑色的现象,设计实验探究黑色物质成分。
查阅资料:
 是一种黑色粉末,不稳定,在空气中加热可被氧化为
是一种黑色粉末,不稳定,在空气中加热可被氧化为 ;隔绝空气加热歧化为
;隔绝空气加热歧化为 和
和 。
。提出猜想:
猜想1:酒精与粉笔灼烧的产物;
猜想2:酒精还原铁锈色物质而得到的产物。
实验设计:
①实验1:利用一个简单的操作证明猜想1不成立,实验操作为
②实验2:如图所示密闭装置中,先在浸泡过酒精的粉笔处加热,再在铁锈色物质处加热,观察到铁锈色物质变为黑色后持续加热
 ,取下试管加热,观察到有砖红色沉淀产生,先在粉笔处加热的目的是
,取下试管加热,观察到有砖红色沉淀产生,先在粉笔处加热的目的是
限选试剂:黑色粉末样品、
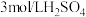 溶液、
溶液、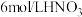 溶液、
溶液、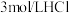 溶液、
溶液、 酸性
酸性 溶液、
溶液、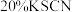 溶液、蒸馏水。
溶液、蒸馏水。实验序号 | 实验操作 | 实验现象 | 实验结论 |
| 3 | 取黑色粉末靠近磁铁 | 黑色粉末几乎全被磁铁吸引,未被吸收的黑色粉末经检验不含铁元素 | 黑色粉末不是 |
| 4 | 向盛有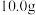 黑色粉末的试管中加入① 黑色粉末的试管中加入① | 固体全部溶解且无气泡产生 | ② |
| 5 | 将实验4的溶液分为四等份,用 酸性 酸性 溶液滴定至终点,重复三次平均消耗 溶液滴定至终点,重复三次平均消耗 溶液 溶液 | 滴定终点现象是 ③ | 黑色粉末是 |
| 6 | 取实验5中剩余一等份溶液于洁净试管中,加入④ | ⑤ |
(4)由以上实验测得黑色粉末中铁元素的质量分数为
 固体中
固体中 与
与 个数比为
个数比为 )。
)。
您最近一年使用:0次
名校
解题方法
2 . 下列实验操作或实验仪器的使用错误的是
| A.用酸式滴定管量取10.00mL高锰酸钾溶液 | B.容量瓶和分液漏斗使用前均需检查是否漏水 |
| C.保存氯化亚铁溶液时,加入少量稀盐酸和铁粉 | D.皮肤溅上液溴,立即用苯洗涤,然后用水冲洗 |
您最近一年使用:0次
3 . 硫酰氯( )是一种重要的化工试剂,被广泛应用于制造医药品、染料、表面活性剂等。某兴趣小组在实验室利用
)是一种重要的化工试剂,被广泛应用于制造医药品、染料、表面活性剂等。某兴趣小组在实验室利用 和
和 反应合成
反应合成 。
。
已知:① 。
。
② 的熔点为
的熔点为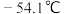 ,沸点为
,沸点为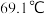 ;
; 以上会分解;遇水能发生剧烈反应,并产生白雾。
以上会分解;遇水能发生剧烈反应,并产生白雾。
回答下列问题:
(1)从甲~戊中选择合适的装置(可以重复选用)制备 ,正确的连接顺序是
,正确的连接顺序是
_______ 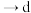 (用小写字母表示)。
(用小写字母表示)。_______ ;仪器Y中盛放的试剂为_______ (填名称),其作用为_______ 。
(3)装置丙中发生反应的离子方程式为_______ 。
(4)装置丁的作用有除去少量 气体、平衡气压和
气体、平衡气压和_______ 。
(5)硫酰氯纯度的测定:取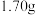 硫酰氯产品在密闭条件下溶于烧碱溶液,最后定容为
硫酰氯产品在密闭条件下溶于烧碱溶液,最后定容为 溶液,取
溶液,取 该溶液于锥形瓶中,调
该溶液于锥形瓶中,调 为
为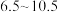 ,加入少量
,加入少量 作指示剂,用
作指示剂,用 的
的 标准溶液滴定(滴定过程中
标准溶液滴定(滴定过程中 不参与反应),平行滴定三次,平均消耗
不参与反应),平行滴定三次,平均消耗 标准溶液
标准溶液 。
。
①下列操作使测定结果偏低的是_______ (填字母)。
A.调节 过低
过低
B.滴定终点时,俯视标准液液面读数
C.锥形瓶未用待测液润洗
②该硫酰氯产品的纯度为_______ 。
(6)亚硫酰氯( )易水解,被广泛应用于结晶水合物的脱水。将
)易水解,被广泛应用于结晶水合物的脱水。将 与
与 混合并加热,可得到无水
混合并加热,可得到无水 ,写出该反应的化学方程式:
,写出该反应的化学方程式:_______ 。
 )是一种重要的化工试剂,被广泛应用于制造医药品、染料、表面活性剂等。某兴趣小组在实验室利用
)是一种重要的化工试剂,被广泛应用于制造医药品、染料、表面活性剂等。某兴趣小组在实验室利用 和
和 反应合成
反应合成 。
。已知:①
 。
。②
 的熔点为
的熔点为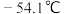 ,沸点为
,沸点为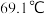 ;
; 以上会分解;遇水能发生剧烈反应,并产生白雾。
以上会分解;遇水能发生剧烈反应,并产生白雾。回答下列问题:
(1)从甲~戊中选择合适的装置(可以重复选用)制备
 ,正确的连接顺序是
,正确的连接顺序是
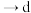 (用小写字母表示)。
(用小写字母表示)。
(3)装置丙中发生反应的离子方程式为
(4)装置丁的作用有除去少量
 气体、平衡气压和
气体、平衡气压和(5)硫酰氯纯度的测定:取
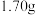 硫酰氯产品在密闭条件下溶于烧碱溶液,最后定容为
硫酰氯产品在密闭条件下溶于烧碱溶液,最后定容为 溶液,取
溶液,取 该溶液于锥形瓶中,调
该溶液于锥形瓶中,调 为
为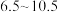 ,加入少量
,加入少量 作指示剂,用
作指示剂,用 的
的 标准溶液滴定(滴定过程中
标准溶液滴定(滴定过程中 不参与反应),平行滴定三次,平均消耗
不参与反应),平行滴定三次,平均消耗 标准溶液
标准溶液 。
。①下列操作使测定结果偏低的是
A.调节
 过低
过低B.滴定终点时,俯视标准液液面读数
C.锥形瓶未用待测液润洗
②该硫酰氯产品的纯度为
(6)亚硫酰氯(
 )易水解,被广泛应用于结晶水合物的脱水。将
)易水解,被广泛应用于结晶水合物的脱水。将 与
与 混合并加热,可得到无水
混合并加热,可得到无水 ,写出该反应的化学方程式:
,写出该反应的化学方程式:
您最近一年使用:0次
4 . 水解原理在化学生产生活中应用广泛,下列反应未使用水解原理的是
A.盐卤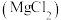 点豆腐 点豆腐 | B.皂化反应 | C. 溶液用于金属除锈 溶液用于金属除锈 | D.淀粉酿酒 |
您最近一年使用:0次
名校
5 . 这周末,高中生小明帮家里做家务。下列劳动项目与所涉及的化学原理不相符的是
| 选项 | 劳动项目 | 化学原理 |
| A | 用盐卤和豆浆制作豆腐 | 胶体的聚沉 |
| B | 用加水稀释的“84”消毒液拖地面 | 氧化还原反应 |
| C | 用白醋清洗水壶中的水垢 | 分解反应 |
| D | 用热的纯碱溶液洗涤餐具 | 水解反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
6 . “劳动最光荣、劳动最崇高”。下列劳动项目与所述的化学知识没有关联的是
选项 | 劳动项目 | 化学知识 |
A | 实验员用TiCl4加大量的水制备TiO2 | 稀释促进盐的水解 |
B | 科学家用乳酸合成聚乳酸 | 合成聚乳酸是缩聚反应 |
C | 工人使用糯米酿造米酒 | 葡萄糖在酶作用下转化为乙醇 |
D | 农艺师施肥时用土壤掩埋铵态氨肥 | 铵盐易溶于水 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7 . 某研究小组拟在实验室以废铁屑(含有少量炭和 杂质)为原料制备无水
杂质)为原料制备无水 ,设计如下流程(已知
,设计如下流程(已知 易水解):
易水解):不正确 的是
 杂质)为原料制备无水
杂质)为原料制备无水 ,设计如下流程(已知
,设计如下流程(已知 易水解):
易水解):
| A.试剂X可选用硫酸 |
B.“氧化”时: |
| C.操作①②均需用到漏斗、烧杯、玻璃棒 |
| D.“脱水”时可能会产生亚铁盐 |
您最近一年使用:0次
名校
8 . 氯化亚铁在冶金、医药制造、媒染剂等方面有着较为广泛的用途,氯化亚铁可以对许多分子进行激活反应,成为一种新型“明星分子”。回答下列问题:
(1)由 固体粗略配制
固体粗略配制 溶液,称取
溶液,称取___________ g 固体在
固体在___________ (填试剂)中溶解后,加水稀释为 ,最后加入少量铁粉。
,最后加入少量铁粉。
(2)“无汞定铁法”标定 溶液浓度:
溶液浓度:
①将___________ (填酸式或碱式)滴定管先水洗,再润洗,最后盛装 标准
标准 溶液,其下一步操作是
溶液,其下一步操作是___________ ,……正确安装滴定管。
②用移液管准确量取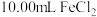 溶液注入锥形瓶中,并加入
溶液注入锥形瓶中,并加入 硫酸和几滴二苯胺磺酸钠。二苯胺磺酸钠的作用是
硫酸和几滴二苯胺磺酸钠。二苯胺磺酸钠的作用是___________ 。
③用 标准溶液滴定,当锥形瓶中溶液颜色从绿色变为紫红色即为滴定终点,平行滴定三次,平均消耗
标准溶液滴定,当锥形瓶中溶液颜色从绿色变为紫红色即为滴定终点,平行滴定三次,平均消耗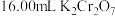 标准溶液,写出滴定反应的离子方程式
标准溶液,写出滴定反应的离子方程式___________ 。 溶液的标定浓度为
溶液的标定浓度为___________ 。
(3)取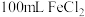 溶液加热、蒸干、灼烧至质量不变。固体质量为
溶液加热、蒸干、灼烧至质量不变。固体质量为___________ 。
(4)已知:亚硫酰氯( )沸点为
)沸点为 ,遇水极易水解。实验室利用
,遇水极易水解。实验室利用 固体和亚硫酰氯(
固体和亚硫酰氯( )制备新型“明星分子”
)制备新型“明星分子” 固体的装置如下图所示:
固体的装置如下图所示: 后,先加热装置
后,先加热装置___________ (填“a”或“b”)。
②装置c、d连接在一起共同起到的作用___________ 。
③硬质玻璃试管b中发生反应的化学方程式___________ 。
④装置e中试剂为 的酸性
的酸性 溶液,发生反应的离子方程式为
溶液,发生反应的离子方程式为___________ 。
(1)由
 固体粗略配制
固体粗略配制 溶液,称取
溶液,称取 固体在
固体在 ,最后加入少量铁粉。
,最后加入少量铁粉。(2)“无汞定铁法”标定
 溶液浓度:
溶液浓度:①将
 标准
标准 溶液,其下一步操作是
溶液,其下一步操作是②用移液管准确量取
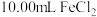 溶液注入锥形瓶中,并加入
溶液注入锥形瓶中,并加入 硫酸和几滴二苯胺磺酸钠。二苯胺磺酸钠的作用是
硫酸和几滴二苯胺磺酸钠。二苯胺磺酸钠的作用是③用
 标准溶液滴定,当锥形瓶中溶液颜色从绿色变为紫红色即为滴定终点,平行滴定三次,平均消耗
标准溶液滴定,当锥形瓶中溶液颜色从绿色变为紫红色即为滴定终点,平行滴定三次,平均消耗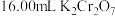 标准溶液,写出滴定反应的离子方程式
标准溶液,写出滴定反应的离子方程式 溶液的标定浓度为
溶液的标定浓度为(3)取
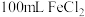 溶液加热、蒸干、灼烧至质量不变。固体质量为
溶液加热、蒸干、灼烧至质量不变。固体质量为(4)已知:亚硫酰氯(
 )沸点为
)沸点为 ,遇水极易水解。实验室利用
,遇水极易水解。实验室利用 固体和亚硫酰氯(
固体和亚硫酰氯( )制备新型“明星分子”
)制备新型“明星分子” 固体的装置如下图所示:
固体的装置如下图所示: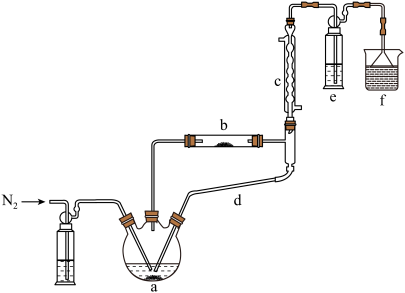
 后,先加热装置
后,先加热装置②装置c、d连接在一起共同起到的作用
③硬质玻璃试管b中发生反应的化学方程式
④装置e中试剂为
 的酸性
的酸性 溶液,发生反应的离子方程式为
溶液,发生反应的离子方程式为
您最近一年使用:0次
7日内更新
|
201次组卷
|
2卷引用:陕西省西安市第一中学2024届高三下学期模拟押题(二)理综试-化学题
名校
解题方法
9 . 七水硫酸锌在农业中可用作微量元素肥料,也被广泛用于工业领域。锌渣制备 的工艺流程如下。
的工艺流程如下。 ,含有少量
,含有少量 下列说法正确的是
下列说法正确的是
 的工艺流程如下。
的工艺流程如下。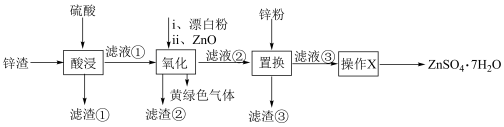
 ,含有少量
,含有少量 下列说法正确的是
下列说法正确的是A.滤渣①为 ,滤渣③为 ,滤渣③为 和 和 |
B.氧化操作发生的反应为: |
C.加入 的主要作用是调节溶液的 的主要作用是调节溶液的 |
| D.操作X用到的玻璃仪器有蒸发皿、玻璃棒、漏斗 |
您最近一年使用:0次
解题方法
10 . 肉桂酸钠(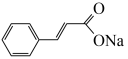 )是一种食品防腐剂,也是一种化妆品成分。某小组探究肉桂酸钠的性质。
)是一种食品防腐剂,也是一种化妆品成分。某小组探究肉桂酸钠的性质。
| 序号 | 操作 | 现象 |
 | 取适量肉桂酸钠溶于水中,滴加酚酞溶液 | 溶液变红色 |
 | 向酸性 溶液中滴加肉桂酸钠溶液,振荡 溶液中滴加肉桂酸钠溶液,振荡 | 溶液褪色 |
 | 向溴水中滴加肉桂酸钠溶液,振荡 | 溶液褪色 |
(1)实验
 可证明肉桂酸是
可证明肉桂酸是(2)由实验
 可知,肉桂酸钠具有
可知,肉桂酸钠具有 中发生反应的类型是
中发生反应的类型是实验(二):探究肉桂酸钠的水解(肉桂酸钠用NaR表示)。
(3)用肉桂酸钠固体配制
 溶液。
溶液。①下列仪器中,配制上述溶液不需要的是

(4)为了探究外界条件对NaR水解的影响,该小组设计如表所示实验:
| 序号 |  溶液/mL 溶液/mL | 蒸馏水/mL | 温度/℃ | 测定pH |
 | 10.0 | 0 | 25 | 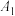 |
 | 5.0 | 5.0 | 25 | 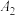 |
 | 10.0 | 0 | 45 |  |
 、
、 的目的是
的目的是②已知NaR水解为吸热反应,甲同学预测:
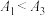 ,实验结果:
,实验结果: ,二者矛盾的主要原因是
,二者矛盾的主要原因是(5)该小组通过测定不同温度下NaR的水解常数
 ,确定温度对NaR水解程度的影响。
,确定温度对NaR水解程度的影响。【查阅资料】
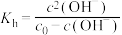 ,
, 为NaR溶液起始浓度。
为NaR溶液起始浓度。试剂和仪器:0.10 mol·L-1NaR溶液、0.100 0 mol·L-1盐酸、甲基橙溶液、pH计。
【设计实验】测定45℃下NaR的水解常数
 ,补充下表中实验。
,补充下表中实验。| 序号 | 实验 | 记录的数据 |
 | 取20.00mLNaR溶液,滴几滴甲基橙溶液,用 盐酸滴定至终点 盐酸滴定至终点 | 盐酸体积为 |
 | 测定45℃纯水的pH |  |
 |  |
【实验处理】
45℃下,

【实验结论】Kh(65℃)>Kh(55℃)>Kh(45℃),升高温度,NaR水解程度增大。
您最近一年使用:0次



