名校
1 . 将等物质的量浓度等体积的甘氨酸溶液与盐酸混合,发生反应: ,取上述溶液(含0.04mol
,取上述溶液(含0.04mol  ),滴加NaOH溶液,pH的变化如下图所示(注:b点溶液中甘氨酸以
),滴加NaOH溶液,pH的变化如下图所示(注:b点溶液中甘氨酸以 的形式存在)。
的形式存在)。
 ,取上述溶液(含0.04mol
,取上述溶液(含0.04mol  ),滴加NaOH溶液,pH的变化如下图所示(注:b点溶液中甘氨酸以
),滴加NaOH溶液,pH的变化如下图所示(注:b点溶液中甘氨酸以 的形式存在)。
的形式存在)。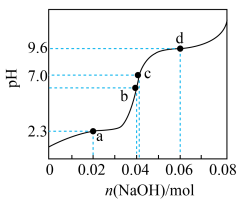
A. 中解离出 中解离出 的能力: 的能力: |
B.b点溶液pH<7,推测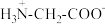 中 中 解离出 解离出 的程度大于-COO-水解的程度 的程度大于-COO-水解的程度 |
C.c点溶液中存在: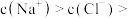 c( c(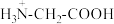 ) )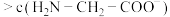 |
D.由d点可知: 的 的 |
您最近一年使用:0次
2024-04-10更新
|
631次组卷
|
5卷引用:2024届宁夏石嘴山市第三中学高三下学期四模理综试题-高中化学
名校
2 . 为探究温度对盐类水解的影响,利用手持技术测定0.1mol•L-1Na2CO3溶液温度由20℃升高到60℃过程的pH,130s后的曲线如图所示(已知pKw=pH+pOH)。下列说法正确的是


| A.加热升温时,溶液中的c(OH-)降低 |
B.加热过程中,n(H2CO3)+n(HCO )+n(CO )+n(CO )逐渐增大 )逐渐增大 |
C.常温下,Kh1(CO )为10-4.6 )为10-4.6 |
D.Kw受温度的影响程度大于Kh1(CO ) ) |
您最近一年使用:0次
2022-01-15更新
|
443次组卷
|
4卷引用:宁夏回族自治区银川一中2022-2023学年高二上学期期中考试化学试题
宁夏回族自治区银川一中2022-2023学年高二上学期期中考试化学试题福建省泉州市2021-2022学年高三上学期1月普通高中毕业班质量监测(二)化学试题(已下线)考点28 盐类的水解-备战2023年高考化学一轮复习考点帮(全国通用)云南省腾冲市第八中学2022-2023学年高二下学期第三次月考化学试题
名校
3 . 25℃时,NaCN溶液中CN-、HCN浓度所占分数( )随pH变化的关系如图甲所示,其中a点的坐标为(9.5,0.5)。向10mL0.01mol·L-1NaCN溶液中逐滴加入0.01mol·L-1的盐酸,其pH变化曲线如图乙所示。下列溶液中的关系中一定正确的
)随pH变化的关系如图甲所示,其中a点的坐标为(9.5,0.5)。向10mL0.01mol·L-1NaCN溶液中逐滴加入0.01mol·L-1的盐酸,其pH变化曲线如图乙所示。下列溶液中的关系中一定正确的
 )随pH变化的关系如图甲所示,其中a点的坐标为(9.5,0.5)。向10mL0.01mol·L-1NaCN溶液中逐滴加入0.01mol·L-1的盐酸,其pH变化曲线如图乙所示。下列溶液中的关系中一定正确的
)随pH变化的关系如图甲所示,其中a点的坐标为(9.5,0.5)。向10mL0.01mol·L-1NaCN溶液中逐滴加入0.01mol·L-1的盐酸,其pH变化曲线如图乙所示。下列溶液中的关系中一定正确的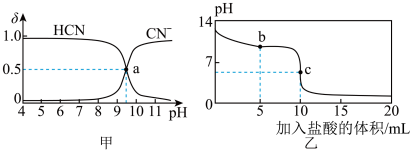
| A.图甲中pH=7的溶液:c(Cl-)=c(HCN) |
| B.常温下,NaCN的水解平衡常数:Kh(NaCN)=10-4.5mol/L |
| C.图乙中b点的溶液:c(CN-)>c(Cl-)>c(HCN)>c(OH-)>c(H+) |
| D.图乙中c点的溶液:c(Na+)+ c(H+)= c(HCN)+ c(OH-)+ c(CN-) |
您最近一年使用:0次
2020-04-26更新
|
284次组卷
|
6卷引用:2024届宁夏回族自治区银川一中高三下学期第二次模拟考试理科综合试卷-高中化学
单选题
|
较难(0.4)
|
名校
4 . 下列说法正确的是
| A.升高NH4Cl溶液的温度,其水的离子积常数和pH均增大 |
| B.在有AgI沉淀的上层清液中滴加一定浓度的NaCl溶液,不可能产生白色沉淀 |
| C.pH=3的盐酸与pH=11的氨水等体积混合后,溶液中:c(NH4+>c(Cl-)>c(OH-)>c(H+) |
D.室温下,稀释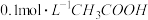 溶液,溶液的导电能力增强 溶液,溶液的导电能力增强 |
您最近一年使用:0次
名校
5 . 常温下,如果取0.1mol/LHA溶液与0.1mol/LNaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=8。试回答下列问题:
(1)混合溶液pH=8的原因是______________ (用离子方程式表示)
(2)混合溶液中由水电离出的c(OH-)___________ (填“大于”、“等于”或“小于”)0.1mol/LNaOH溶液中由水电离出的c(OH-)
(3)求出混合溶液中下列算式的精确计算结果(填具体数字):
c(Na+)- c(A-)=____________ mol/L, c(OH-)- c(HA)=____________ mol/L
常温下,将PH=2的酸HA溶液与PH=12的NaOH溶液等体积混合后,所得溶液PH_________ 7 (填“大于”、“等于”或“小于”)
(5)已知NH4A溶液为中性,又知HA溶液加到Na2CO3溶液中有气体放出,试推断(NH4)2CO3溶液的PH___________ 7(填“大于”、“等于”或“小于”)。
(1)混合溶液pH=8的原因是
(2)混合溶液中由水电离出的c(OH-)
(3)求出混合溶液中下列算式的精确计算结果(填具体数字):
c(Na+)- c(A-)=
常温下,将PH=2的酸HA溶液与PH=12的NaOH溶液等体积混合后,所得溶液PH
(5)已知NH4A溶液为中性,又知HA溶液加到Na2CO3溶液中有气体放出,试推断(NH4)2CO3溶液的PH
您最近一年使用:0次
2017-03-06更新
|
967次组卷
|
2卷引用:宁夏青铜峡市高级中学2019-2020学年高二上学期期中考试化学试题



