解题方法
1 . 下列离子方程式的书写正确的是
A.硫酸铜溶液中通入 : : |
B.用石墨电极电解氯化铝溶液: |
C. 溶液与 溶液与 溶液混合反应: 溶液混合反应: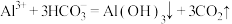 |
D.少量 通入足量 通入足量 溶液中: 溶液中: |
您最近一年使用:0次
名校
2 . 常温下,下列各组离子在指定溶液中因发生双水解而不能大量共存的是
A.无色透明的溶液中: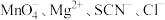 |
B.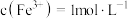 的溶液中: 的溶液中: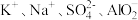 |
C.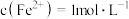 的溶液中: 的溶液中: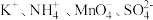 |
D.使甲基橙呈红色的溶液中: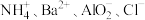 |
您最近一年使用:0次
2024-01-16更新
|
108次组卷
|
2卷引用:湖北省武汉市武钢三中2023-2024学年高二上学期12月月考化学试题
解题方法
3 . 下列各组离子在给定溶液中能 大量共存的是
A.1.0mol/L 盐酸中: |
B.1.0molL 氨水中: |
C.0.1 mol/L  溶液中: 溶液中: |
D.0.1 mol/L 溶液中: 溶液中: |
您最近一年使用:0次
名校
解题方法
4 . CoCl2可用于电镀,是一种性能优越的电池前驱材料,由含钴矿(Co 元素主要以Co2O3、 CoO 的形式存在,还含有Fe、Si、Cu、Zn、Mn、Ni、Mg、Ca 元素,碳及有机物等)制取氯化钴晶体的一种工艺流程如图:

已知:①焦亚硫酸钠(Na2S2O5)常作食品抗氧化剂。CaF2、MgF2 难溶于水。
②CoCl2∙6H2O 的熔点为 86℃,易溶于水、乙醚等;常温下稳定无毒,加热至 110~120℃时, 失去结晶水变成有毒的无水氯化钴。
③部分金属阳离子形成氢氧化物的 pH 见表:
回答下列问题:
(1)“550℃焙烧”的目的是_______ 。
(2)“浸取”的过程中,用离子方程式表示 Na2S2O5的主要作用是_______ 。
(3)滤液 1 中加入 NaClO3溶液的作用是_______ 。
(4)加入Na2CO3 溶液生成滤渣 2 的主要离子方程式为_______ 。
滤液 3 经过多次萃取与反萃取制备CoCl2 晶体:
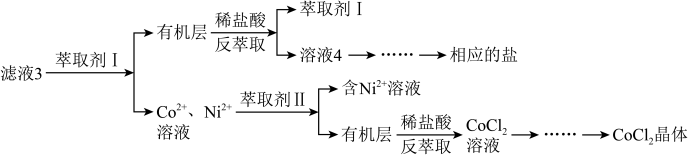
(5)滤液 3 中加入萃取剂 I,然后用稀盐酸反萃取的目的是_______ 。
(6)制备晶体CoCl2∙6H2O,需在减压环境下烘干的原因是_______ 。
(7)测定产品的纯度:称取 CoCl2∙6H2O 样品,将其用适当试剂转化为 CoC2O4,再转化为(NH4)2C2O4溶液,稀硫酸酸化后用高锰酸钾标准溶液滴定,滴定终点的判定_______ 。

已知:①焦亚硫酸钠(Na2S2O5)常作食品抗氧化剂。CaF2、MgF2 难溶于水。
②CoCl2∙6H2O 的熔点为 86℃,易溶于水、乙醚等;常温下稳定无毒,加热至 110~120℃时, 失去结晶水变成有毒的无水氯化钴。
③部分金属阳离子形成氢氧化物的 pH 见表:
| Co3+ | Fe3+ | Cu2+ | Co2+ | Fe2+ | Zn2+ | Mn2+ | Mg2+ | |
| 开始沉淀 pH | 0.3 | 2.7 | 5.5 | 7.2 | 7.6 | 7.6 | 8.3 | 9.6 |
| 完全沉淀 pH | 1.1 | 3.2 | 6.6 | 9.2 | 9.6 | 9.2 | 9.3 | 11.1 |
(1)“550℃焙烧”的目的是
(2)“浸取”的过程中,用离子方程式表示 Na2S2O5的主要作用是
(3)滤液 1 中加入 NaClO3溶液的作用是
(4)加入Na2CO3 溶液生成滤渣 2 的主要离子方程式为
滤液 3 经过多次萃取与反萃取制备CoCl2 晶体:

(5)滤液 3 中加入萃取剂 I,然后用稀盐酸反萃取的目的是
(6)制备晶体CoCl2∙6H2O,需在减压环境下烘干的原因是
(7)测定产品的纯度:称取 CoCl2∙6H2O 样品,将其用适当试剂转化为 CoC2O4,再转化为(NH4)2C2O4溶液,稀硫酸酸化后用高锰酸钾标准溶液滴定,滴定终点的判定
您最近一年使用:0次
5 . 常温下,下列各组离子一定能大量共存的是
A.0.1mol/L的 溶液中: 溶液中: 、 、 、 、 、 、 |
B.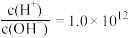 的溶液中:: 的溶液中:: 、 、 、 、 、 、 |
C.滴加KSCN溶液显红色的溶液中: 、 、 、 、 、 、 |
D.水电离产生的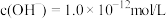 的溶液中: 的溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
名校
解题方法
6 . 常温下,下列各组离子在给定溶液中一定能大量共存的是
A.pH=1的溶液:I-、Mg2+、 、 、 |
B.能使酚酞试液变红的溶液:K+、Na+、S2-、 |
C.中性溶液:Al3+、K+、Cl-、 |
D.由水电离出的c(H+)·c(OH-)=10-20的溶液:Na+、Cl-、S2-、 |
您最近一年使用:0次
2023高三·全国·专题练习
名校
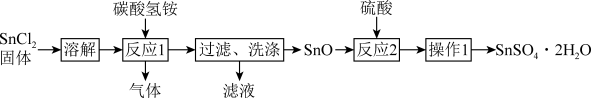
7 .  易水解,是常见的抗氧化剂。实验室以
易水解,是常见的抗氧化剂。实验室以 为原料制备
为原料制备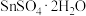 的流程如下:
的流程如下:
下列说法错误的是
 易水解,是常见的抗氧化剂。实验室以
易水解,是常见的抗氧化剂。实验室以 为原料制备
为原料制备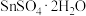 的流程如下:
的流程如下:
下列说法错误的是
A.溶解时,将 固体溶解在较浓的盐酸中,然后加水稀释 固体溶解在较浓的盐酸中,然后加水稀释 |
B.反应1的离子方程式为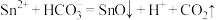 |
C.可用 酸化的 酸化的 溶液检验 溶液检验 沉淀是否已被洗涤干净 沉淀是否已被洗涤干净 |
| D.操作1为蒸发浓缩、冷却结晶、过滤、洗涤、干燥 |
您最近一年使用:0次
8 . 室温下,通过下列实验探究NaHCO3溶液的性质。
实验1 用pH试纸测得0.1 NaHCO3溶液的pH约为8;
NaHCO3溶液的pH约为8;
实验2 向0.1 NaHCO3溶液滴入等浓度Ba(OH)2溶液至恰好完全反应;
NaHCO3溶液滴入等浓度Ba(OH)2溶液至恰好完全反应;
实验3 向0.1 NaHCO3溶液中加入等体积0.1
NaHCO3溶液中加入等体积0.1 NaOH溶液;
NaOH溶液;
实验4 向浓NaHCO3溶液中加入浓Al2(SO4)3溶液,有气体和沉淀生成;
下列说法错误的是
实验1 用pH试纸测得0.1
 NaHCO3溶液的pH约为8;
NaHCO3溶液的pH约为8;实验2 向0.1
 NaHCO3溶液滴入等浓度Ba(OH)2溶液至恰好完全反应;
NaHCO3溶液滴入等浓度Ba(OH)2溶液至恰好完全反应;实验3 向0.1
 NaHCO3溶液中加入等体积0.1
NaHCO3溶液中加入等体积0.1 NaOH溶液;
NaOH溶液;实验4 向浓NaHCO3溶液中加入浓Al2(SO4)3溶液,有气体和沉淀生成;
下列说法错误的是
A.实验1的溶液中存在c(H2CO3)>c(CO ) ) |
| B.实验2过程中,水的电离程度先逐渐增大,然后逐渐减小 |
C.实验3反应后的溶液中存在c(OH-)=c(H+)+c(HCO )+c(H2CO3) )+c(H2CO3) |
| D.实验4所生成的气体一定是CO2 |
您最近一年使用:0次
2023-01-12更新
|
186次组卷
|
4卷引用:湖北省部分重点中学(武汉市,十堰市,襄阳市,恩施土家族苗族自治州)2022-2023学年高二下学期三月智学联合检测化学试题
湖北省部分重点中学(武汉市,十堰市,襄阳市,恩施土家族苗族自治州)2022-2023学年高二下学期三月智学联合检测化学试题上海市冠龙高级中学2022-2023学年高三上学期期末考试化学试题(已下线)江苏省南京市、盐城市2021-2022学年高三第一次模拟考试(选择题11-14)(已下线)专题06 酸碱中和与盐类水解及难溶电解质的沉淀溶解平衡-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(上海专用)
9 . 下列各组离子,在指定条件下,一定能大量共存的是
A. 的 的 溶液中: 溶液中: 、 、 、 、 |
B.在 的溶液中: 的溶液中: 、 、 、 、 |
C.使甲基橙试液变红的溶液中: 、 、 、 、 |
D.水电离产生的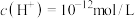 的溶液中: 的溶液中: 、 、 、 、 |
您最近一年使用:0次
名校
解题方法
10 . 下列过程中的化学反应,相应的离子方程式正确的是
A.用泡沫灭火器灭火原理: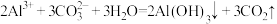 |
B.将氯化银溶于氨水: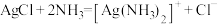 |
C.用漂白液吸收少量二氧化硫气体: |
D.除去苯中混有的少量苯酚: + +   + +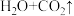 |
您最近一年使用:0次
2023-01-10更新
|
1225次组卷
|
5卷引用:湖北省部分市州2022-2023学年高三元月联合调研考试化学试题



