1 . 往锅炉注入Na2CO3溶液浸泡,将水垢中的CaSO4转化为CaCO3,再用盐酸去除,下列叙述正确的是
| A.温度升高,Na2CO3溶液的KW和c平(OH-)均会减小 |
| B.CaSO4能转化为CaCO3,说明Ksp(CaCO3)>Ksp(CaSO4) |
| C.CaCO3溶解于盐酸而CaSO4不溶,是因为硫酸酸性强于盐酸 |
D.沉淀转化的离子方程式为 (aq)+CaSO4(s) (aq)+CaSO4(s)  CaCO3(s)+ CaCO3(s)+ (aq) (aq) |
您最近一年使用:0次
2023-08-27更新
|
306次组卷
|
3卷引用:作业(二十二) 沉淀的溶解与生成、转化及应用
名校
2 . 将浓盐酸加到NaCl饱和溶液中,会析出NaCl晶体,对这种现象正确的解释是
| A.由于c平(Cl-)增加,使溶液中c平(Na+)·c平(Cl-)>Ksp(NaCl),故产生NaCl晶体 |
| B.HCl是强酸,所以它能使NaCl沉淀出来 |
| C.由于c平(Cl-)增加,使NaCl的溶解平衡向析出NaCl的方向移动,故有NaCl沉淀析出 |
| D.酸的存在,降低了盐的溶解度 |
您最近一年使用:0次
2023-08-26更新
|
472次组卷
|
4卷引用:第1课时 沉淀溶解平衡与溶度积
3 . 当氢氧化镁固体在水中达到沉淀溶解平衡Mg(OH)2(s) Mg2+(aq)+2OH-(aq)时,为使Mg(OH)2固体的量减少,需加入少量的
Mg2+(aq)+2OH-(aq)时,为使Mg(OH)2固体的量减少,需加入少量的
 Mg2+(aq)+2OH-(aq)时,为使Mg(OH)2固体的量减少,需加入少量的
Mg2+(aq)+2OH-(aq)时,为使Mg(OH)2固体的量减少,需加入少量的| A.NH4NO3 | B.NaOH |
| C.MgSO4 | D.Na2SO4 |
您最近一年使用:0次
名校
解题方法
4 . 氯酸镁[Mg(ClO3)2]常用作催熟剂、除草剂等,以卤块(主要成分为MgCl2·6H2O,含有MgSO4、FeCl2等杂质)为原料制备少量Mg(ClO3)2·6H2O的流程如下:
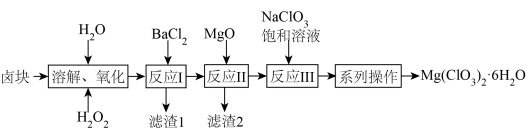
下列说法错误的是

下列说法错误的是
| A.“溶解、氧化”时,温度不能太高 |
B.“反应Ⅰ”离子方程式为 |
| C.“反应Ⅱ”发生的依据是Mg(OH)2和Fe(OH)3的Ksp |
| D.“系列操作”需用到的玻璃仪器有烧杯、玻璃棒、分液漏斗等 |
您最近一年使用:0次
2023-08-14更新
|
416次组卷
|
4卷引用:河北省部分学校2023届高三4月大联考二模化学试题
名校
解题方法
5 . 为了除去硫酸镁酸性溶液中的 ,下列操作
,下列操作不正确 的是
 ,下列操作
,下列操作| A.加入过量的NaOH溶液充分反应后过滤 |
| B.加入过量的MgO并通入空气充分反应后过滤 |
C.加入适量的 并通入空气充分反应后过滤 并通入空气充分反应后过滤 |
D.加入适量的 和 和 固体充分反应后过滤 固体充分反应后过滤 |
您最近一年使用:0次
2023-07-29更新
|
244次组卷
|
4卷引用:河南省郑州市2022-2023学年高二上学期期末化学试题
2023高二上·全国·专题练习
6 . 沉淀转化的应用
(1)锅炉除水垢(含有CaSO4):CaSO4(s) CaCO3(s)
CaCO3(s) Ca2+(aq),反应为:
Ca2+(aq),反应为:_______ 。
(2)自然界中矿物的转化:原生铜的硫化物 CuSO4溶液
CuSO4溶液 铜蓝(CuS),反应为:
铜蓝(CuS),反应为:_______ 。
(3)工业废水处理:工业废水处理过程中,重金属离子可利用沉淀转化原理用FeS等难溶物转化为HgS、Ag2S、PbS等沉淀。用FeS除去Hg2+的离子方程式:_______ 。
(1)锅炉除水垢(含有CaSO4):CaSO4(s)
 CaCO3(s)
CaCO3(s) Ca2+(aq),反应为:
Ca2+(aq),反应为:(2)自然界中矿物的转化:原生铜的硫化物
 CuSO4溶液
CuSO4溶液 铜蓝(CuS),反应为:
铜蓝(CuS),反应为:(3)工业废水处理:工业废水处理过程中,重金属离子可利用沉淀转化原理用FeS等难溶物转化为HgS、Ag2S、PbS等沉淀。用FeS除去Hg2+的离子方程式:
您最近一年使用:0次
7 . 固体的溶解过程
固体物质的溶解是可逆过程:固体溶质 溶液中的溶质
溶液中的溶质
(1)v(溶解)_____ v(结晶):固体溶解
(2)v(溶解)_____ v(结晶):溶解平衡
(3)v(溶解)_____ v(结晶):析出晶体
固体物质的溶解是可逆过程:固体溶质
 溶液中的溶质
溶液中的溶质(1)v(溶解)
(2)v(溶解)
(3)v(溶解)
您最近一年使用:0次
8 . 溶度积规则
通过比较溶度积Ksp与溶液中有关离子浓度幂的乘积Qc的相对大小,可以判断难溶电解质在给定条件下沉淀能否生成或溶解:
(1)Qc>Ksp,_____ 。
(2)Qc=Ksp,_____ 。
(3)Qc<Ksp,_____ 。
通过比较溶度积Ksp与溶液中有关离子浓度幂的乘积Qc的相对大小,可以判断难溶电解质在给定条件下沉淀能否生成或溶解:
(1)Qc>Ksp,
(2)Qc=Ksp,
(3)Qc<Ksp,
您最近一年使用:0次
9 . 用沉淀溶解平衡原理解决下列问题:
(1)除去硫酸铜溶液中的少量Fe3+_______ 。
(2)除去NH4Cl溶液中的少量FeCl3_______ 。
(3)除去MgCl2溶液中的少量CuCl2_______ 。
(1)除去硫酸铜溶液中的少量Fe3+
(2)除去NH4Cl溶液中的少量FeCl3
(3)除去MgCl2溶液中的少量CuCl2
您最近一年使用:0次
10 . 根据沉淀溶解平衡原理,如果加入与溶液中相同的离子,使平衡向沉淀方向移动,就可以生成沉淀。实例:可溶性钡盐(如BaCl2等)当作食盐食用,会造成钡中毒。中毒患者常用5.0%的Na2SO4溶液洗胃的原因是_______ 。
您最近一年使用:0次



