1 . 向50mlL0.018mol/LAgNO3溶液中加入50mL0.02mol/L盐酸。已知AgCl(s)的溶度积常数Ksp=1×10-10,混合后溶液的体积变化忽略不计。请计算:
(1)沉淀生成后,溶液中c(Ag+)=_____ 。
(2)沉淀生成后,溶液的pH=_____ 。
(3)如果向沉淀生成后的溶液中继续加入50ml0.001mol/L的盐酸,是否产生沉淀_____ ?(填“是”或“否”)
(1)沉淀生成后,溶液中c(Ag+)=
(2)沉淀生成后,溶液的pH=
(3)如果向沉淀生成后的溶液中继续加入50ml0.001mol/L的盐酸,是否产生沉淀
您最近一年使用:0次
名校
2 . (1)常温下,0.1 mol/L的醋酸溶液加水稀释后,下列说法正确的是_____ 。
A. 溶液中导电粒子的数目减少
B. 醋酸的电离程度增大,c(H+)亦增大
C. 溶液中 不变
不变
(2)常温下若溶液由pH=3的HCl溶液V1 mL与pH=11的NaOH溶液V2 mL混合使pH等于7,则V1_____ V2(填>、<或 =)。溶液中离子浓度大小顺序为_____ 。
(3)常温下,浓度均为0.1 mol/L的下列五种溶液的pH如表所示:
①根据表中数据,浓度均为0.01 mol/L的下列四种酸的溶液pH最小的是_____
A HCN B HClO C H2CO3 D CH3COOH
②根据以上数据,判断下列反应可以成立的是________
A.CH3COOH+Na2CO3=NaHCO3+CH3COONa
B.CH3COOH+NaCN=CH3COONa+HCN
C.CO2+H2O+2NaClO=Na2CO3+2HClO
D.NaHCO3+HCN=NaCN+H2O+CO2↑
(4)几种离子开始沉淀时的pH如下表:
当向含相同浓度Cu2+、Mg2+和Fe2+的溶液中滴加NaOH溶液时,(填离子符号)_____ 先沉淀。
A. 溶液中导电粒子的数目减少
B. 醋酸的电离程度增大,c(H+)亦增大
C. 溶液中
 不变
不变 (2)常温下若溶液由pH=3的HCl溶液V1 mL与pH=11的NaOH溶液V2 mL混合使pH等于7,则V1
(3)常温下,浓度均为0.1 mol/L的下列五种溶液的pH如表所示:
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
①根据表中数据,浓度均为0.01 mol/L的下列四种酸的溶液pH最小的是
A HCN B HClO C H2CO3 D CH3COOH
②根据以上数据,判断下列反应可以成立的是
A.CH3COOH+Na2CO3=NaHCO3+CH3COONa
B.CH3COOH+NaCN=CH3COONa+HCN
C.CO2+H2O+2NaClO=Na2CO3+2HClO
D.NaHCO3+HCN=NaCN+H2O+CO2↑
(4)几种离子开始沉淀时的pH如下表:
| 离子 | Fe2+ | Cu2+ | Mg2+ |
| pH | 7.6 | 5.2 | 10.4 |
当向含相同浓度Cu2+、Mg2+和Fe2+的溶液中滴加NaOH溶液时,(填离子符号)
您最近一年使用:0次
2020-12-08更新
|
219次组卷
|
2卷引用:吉林省长春市第二十九中学2020-2021学年高二上学期第二学程考试化学(理)试题
名校
解题方法
3 . 已知氢硫酸与碳酸的电离平衡常数分别为
H2S: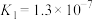

H2CO3:

请回答下列问题:
(1)室温下,0.1mol·L-1的硫化钠溶液和0.1mol·L-1的碳酸钠溶液,碱性更强的是_________________ ,其原因是______________________________________________ ;
(2)向ZnSO4溶液中滴加饱和H2S溶液,没有沉淀生成,继续滴加—定量的氨水后,生成ZnS沉淀。用电离平衡原理解释上述现象:___________________________________________ 。
H2S:
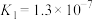

H2CO3:


请回答下列问题:
(1)室温下,0.1mol·L-1的硫化钠溶液和0.1mol·L-1的碳酸钠溶液,碱性更强的是
(2)向ZnSO4溶液中滴加饱和H2S溶液,没有沉淀生成,继续滴加—定量的氨水后,生成ZnS沉淀。用电离平衡原理解释上述现象:
您最近一年使用:0次



