1 . 下列实验操作及现象所得结论正确的是
| 选项 | 实验操作及现象 | 结论 |
| A | 向碳酸钙的悬浊液中通入NO2,悬浊液逐渐变澄清 |  酸性强于 酸性强于 |
| B | 向新制的Cu(OH)2中滴入用碱中和后的蔗糖水解液,加热,产生砖红色沉淀 | 蔗糖已完全水解 |
| C | 取某补铁剂溶于硝酸,向所得溶液中滴加KSCN溶液,溶液变红色 | 该补铁剂中铁元素的化合价为+3价 |
| D | 向CuCl2、MgCl2的混合溶液中滴加NaOH溶液,溶液中先生成蓝色沉淀 |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
2 . 根据下列实验操作和现象所得的结论错误的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向1 mL  AgNO3溶液中,滴加1 mL AgNO3溶液中,滴加1 mL 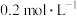 NaCl溶液,然后再滴加0.1 mL NaCl溶液,然后再滴加0.1 mL  KI溶液 KI溶液 | 先出现白色沉淀,然后白色沉淀变黄 |  |
| B | 将败脂醛(CH2=CHCHO)加入酸性高锰酸钾溶液中 | 酸性KMnO4溶液褪色 | 败脂醛中含有碳碳双键 |
| C | 取两支试管分别加入2 mL 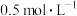 CuCl2溶液,将第一支试管加热,第二支试管置于冷水中 CuCl2溶液,将第一支试管加热,第二支试管置于冷水中 | 第一支试管中溶液颜色呈绿色,第二支试管中溶液颜色呈蓝色 | CuCl2溶液中的平衡: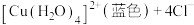 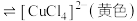  是吸热反应 是吸热反应 |
| D | 将SO2通入Na2CO3溶液中,产生的气体先通入足量的酸性KMnO4溶液,再通入澄清石灰水 | 酸性KMnO4溶液颜色变浅,澄清石灰水变浑浊 | 亚硫酸的酸性强于碳酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
3 . 下列说法正确的是
| A.灼热的木炭伸入浓硝酸中产生红棕色气体,则浓硝酸在加热条件下能氧化碳单质 |
| B.将花生油和NaOH溶液混合加热,分层现象逐渐消失,则花生油在水中的溶解度随温度的升高而增大 |
C.向盛有少量0.1mol/LNaCl溶液的试管里滴几滴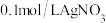 溶液,产生白色沉淀,再滴入1mol/L氨水,振荡,沉淀消失 溶液,产生白色沉淀,再滴入1mol/L氨水,振荡,沉淀消失 |
D.取两份新制氯水,分别滴加 溶液和淀粉KI溶液,前者有白色沉淀,后者溶液变蓝色,则氯气与水的反应存在限度 溶液和淀粉KI溶液,前者有白色沉淀,后者溶液变蓝色,则氯气与水的反应存在限度 |
您最近一年使用:0次
7日内更新
|
106次组卷
|
2卷引用:辽宁省大连市2023-2024学年高三下学期第二次模拟考试化学试卷
解题方法
4 . 实验是探究物质性质的重要方法,下列实验中,根据操作和现象得出的结论正确的是
选项 | 操作 | 现象 | 结论 |
A | 向装有FeS固体的装置中加稀盐酸 | 有气体产生 | 非金属性: |
B | 在烧瓶中加入木炭颗粒与浓硝酸,然后加热 | 烧瓶中出现红棕色气体 | 木炭具有还原性,能还原 |
C | 向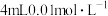 酸性 酸性 溶液中加入 溶液中加入 溶液 溶液 | 产生气泡的速率先增大后减小 | 该反应一定为放热反应 |
D | 向 溶液中加入KI溶液,再加入苯,振荡后静置 溶液中加入KI溶液,再加入苯,振荡后静置 | 上层呈紫红色,下层有白色沉淀生成 |  可以氧化 可以氧化 ,白色沉淀可能为CuI ,白色沉淀可能为CuI |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
5 . 工业上使用 溶液可将
溶液可将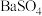 转化为
转化为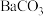 ,一定温度下
,一定温度下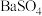 和
和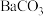 的沉淀溶解平衡曲线如图所示。已知
的沉淀溶解平衡曲线如图所示。已知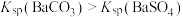 ,处理过程中忽略溶液体积的变化,
,处理过程中忽略溶液体积的变化,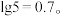
 溶液可将
溶液可将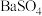 转化为
转化为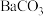 ,一定温度下
,一定温度下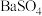 和
和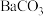 的沉淀溶解平衡曲线如图所示。已知
的沉淀溶解平衡曲线如图所示。已知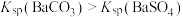 ,处理过程中忽略溶液体积的变化,
,处理过程中忽略溶液体积的变化,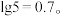
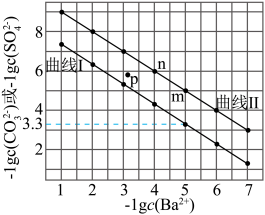
A.曲线I为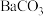 的沉淀溶解平衡曲线, 的沉淀溶解平衡曲线, 的数量级是 的数量级是 |
B.向 点饱和溶液中加适量 点饱和溶液中加适量 固体,可使溶液由 固体,可使溶液由 点变到 点变到 点 点 |
C.p点条件下,能生成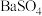 沉淀,不能生成 沉淀,不能生成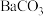 沉淀 沉淀 |
D.用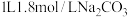 处理 处理 ,处理5次可使 ,处理5次可使 全进入溶液 全进入溶液 |
您最近一年使用:0次
名校
6 . 下列含硫化合物的反应中,离子方程式正确的是
A.将SO2通入NaClO溶液中: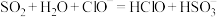 |
B.向硫酸铜溶液中加入NaHS溶液生成黑色沉淀: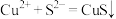 |
C.向硫代硫酸钠溶液中加入硫酸: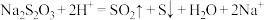 |
D.水垢中的CaSO4用Na2CO3溶液处理: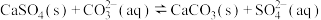 |
您最近一年使用:0次
7日内更新
|
227次组卷
|
3卷引用:安徽省合肥市2024届高三第三次教学质量检测化学试题
7 . 已知:常温下, 、
、 、
、 的溶度积依次为
的溶度积依次为 、
、 、
、 ,化学反应中,平衡常数
,化学反应中,平衡常数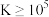 即认为反应能完全进行,不可逆,下列叙述正确的是
即认为反应能完全进行,不可逆,下列叙述正确的是
 、
、 、
、 的溶度积依次为
的溶度积依次为 、
、 、
、 ,化学反应中,平衡常数
,化学反应中,平衡常数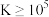 即认为反应能完全进行,不可逆,下列叙述正确的是
即认为反应能完全进行,不可逆,下列叙述正确的是A.溶解度: |
B.向含 废水中加入 废水中加入 ,可完全除去 ,可完全除去 |
C.在含 、 、 、 、 的溶液中通入 的溶液中通入 ,一定最先析出 ,一定最先析出 |
D.在饱和 溶液中, 溶液中, |
您最近一年使用:0次
名校
8 . 砷的化合物可用于半导体领域。一种从酸性高浓度含砷废水[砷主要以亚砷酸 形式存在,废水中还含有一定量的硫酸]中回收砷的工艺流程如下:
形式存在,废水中还含有一定量的硫酸]中回收砷的工艺流程如下: ;
;
П.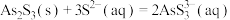 ;
;
III.砷酸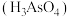 在酸性条件下有强氧化性,能被
在酸性条件下有强氧化性,能被 等还原;
等还原;
IV.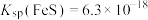 ,
,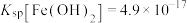 。
。
回答下列问题:
(1)“沉砷”时,亚砷酸转化为 的化学方程式为
的化学方程式为___________ 。
(2)“沉砷”时产生的废气可用___________ 溶液吸收处理(填化学式)。
(3)“NaOH溶液浸取”后,所得“滤渣”的主要成分是___________ (填化学式),“滤渣”中___________  (填“含有”或“不含有”)。
(填“含有”或“不含有”)。
(4)向滤液II中通入氧气进行“氧化脱硫”,反应的离子方程式为___________ 。
(5)“沉砷”过程中FeS不可用过量的 替换,原因是
替换,原因是___________ (从平衡移动的角度解释)。
(6)该流程最后一步用 “还原”砷酸,发生反应的化学方程式为
“还原”砷酸,发生反应的化学方程式为___________ 。
 形式存在,废水中还含有一定量的硫酸]中回收砷的工艺流程如下:
形式存在,废水中还含有一定量的硫酸]中回收砷的工艺流程如下: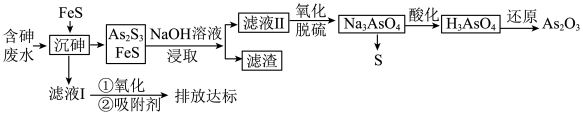
 ;
;П.
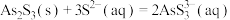 ;
;III.砷酸
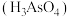 在酸性条件下有强氧化性,能被
在酸性条件下有强氧化性,能被 等还原;
等还原;IV.
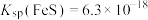 ,
,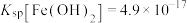 。
。回答下列问题:
(1)“沉砷”时,亚砷酸转化为
 的化学方程式为
的化学方程式为(2)“沉砷”时产生的废气可用
(3)“NaOH溶液浸取”后,所得“滤渣”的主要成分是
 (填“含有”或“不含有”)。
(填“含有”或“不含有”)。(4)向滤液II中通入氧气进行“氧化脱硫”,反应的离子方程式为
(5)“沉砷”过程中FeS不可用过量的
 替换,原因是
替换,原因是(6)该流程最后一步用
 “还原”砷酸,发生反应的化学方程式为
“还原”砷酸,发生反应的化学方程式为
您最近一年使用:0次
名校
解题方法
9 . 下列事实不能用平衡移动原理解释的是
A.将 溶液加热蒸干不能得到 溶液加热蒸干不能得到 固体 固体 |
B.用稀硫酸洗涤 沉淀比用等体积蒸馏水洗涤损失的 沉淀比用等体积蒸馏水洗涤损失的 少 少 |
| C.铁质器件附有铜质配件,久置,在接触处铁易生锈 |
| D.在漂白液中加入适量盐酸能增强其漂白效果 |
您最近一年使用:0次
名校
解题方法
10 . 秦俑彩绘中含有铅白 和黄色的
和黄色的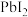 。常温下,
。常温下, 和
和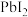 在不同的溶液中分别达到沉淀溶解平衡时pM(阳离子浓度的负对数)与pR(阴离子浓度的负对数)的关系如下图所示。下列说法正确的是
在不同的溶液中分别达到沉淀溶解平衡时pM(阳离子浓度的负对数)与pR(阴离子浓度的负对数)的关系如下图所示。下列说法正确的是
 和黄色的
和黄色的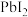 。常温下,
。常温下, 和
和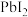 在不同的溶液中分别达到沉淀溶解平衡时pM(阳离子浓度的负对数)与pR(阴离子浓度的负对数)的关系如下图所示。下列说法正确的是
在不同的溶液中分别达到沉淀溶解平衡时pM(阳离子浓度的负对数)与pR(阴离子浓度的负对数)的关系如下图所示。下列说法正确的是
A. 为 为 达到沉淀溶解平衡时pM与pR的关系曲线 达到沉淀溶解平衡时pM与pR的关系曲线 |
B.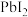 的 的 数量级为 数量级为 |
C. ,正反应比逆反应更难 ,正反应比逆反应更难 |
D.X点时溶液中不能产生 沉淀 沉淀 |
您最近一年使用:0次



