名校
1 .  和
和 在生产、生活中具有广泛的用途,回答下列问题:
在生产、生活中具有广泛的用途,回答下列问题:
已知:①常温下, ,
, ;
;
②不考虑溶液混合时体积和温度的变化。
(1)在 的
的 溶液中,
溶液中,
___________ 。
(2)常温下,向 溶液中滴加
溶液中滴加 的盐酸,溶液的pH随加入的盐酸体积V的变化如图所示:
的盐酸,溶液的pH随加入的盐酸体积V的变化如图所示:

①a点溶液中,水电离出的
___________  (忽略
(忽略 电离的影响)。
电离的影响)。
②b点溶液中,
___________  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
③d点溶液中,
___________  。
。
(3)常温下,将等体积等浓度的 和
和 溶液完全混合,在该混合后的溶液中,各离子浓度由大到小的顺序为
溶液完全混合,在该混合后的溶液中,各离子浓度由大到小的顺序为___________ 。
(4)锅炉中最难清洗的锅垢是硫酸钡固体,298K时工业上常使用碳酸钠溶液进行处理: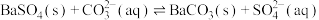 ,已知
,已知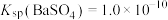 ,
,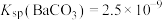 ,若平衡溶液中
,若平衡溶液中 为
为 ,则
,则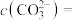
___________  。
。
 和
和 在生产、生活中具有广泛的用途,回答下列问题:
在生产、生活中具有广泛的用途,回答下列问题:已知:①常温下,
 ,
, ;
;②不考虑溶液混合时体积和温度的变化。
(1)在
 的
的 溶液中,
溶液中,
(2)常温下,向
 溶液中滴加
溶液中滴加 的盐酸,溶液的pH随加入的盐酸体积V的变化如图所示:
的盐酸,溶液的pH随加入的盐酸体积V的变化如图所示:
①a点溶液中,水电离出的

 (忽略
(忽略 电离的影响)。
电离的影响)。②b点溶液中,

 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。③d点溶液中,

 。
。(3)常温下,将等体积等浓度的
 和
和 溶液完全混合,在该混合后的溶液中,各离子浓度由大到小的顺序为
溶液完全混合,在该混合后的溶液中,各离子浓度由大到小的顺序为(4)锅炉中最难清洗的锅垢是硫酸钡固体,298K时工业上常使用碳酸钠溶液进行处理:
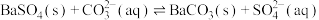 ,已知
,已知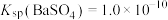 ,
,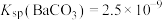 ,若平衡溶液中
,若平衡溶液中 为
为 ,则
,则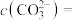
 。
。
您最近一年使用:0次
名校
解题方法
2 . 回答下列问题
(1)若在空气中加热MgCl2·6H2O,生成的是Mg(OH)Cl或MgO,写出生成Mg(OH)Cl关反应的化学方程式_______ 。
(2)用电解法制取金属镁时,需要无水氯化镁。需要在干燥的HCl气流中加热MgCl2·6H2O,才能得到无水MgCl2,其原因是_______ 。
(3)在25℃下,向浓度均为0.1 mol·L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成_______ 沉淀(填化学式)。已知25℃时Ksp[Mg(OH)2]=1.8×10-11,KsP[Cu(OH)2]=2.2×10-20。
Ⅱ.现有常温下的0.1mol·L-1纯碱溶液。
(4)你认为该溶液呈碱性的原因是(用离子方程式表示):_______ 。
(5)已知25℃时,Kh=2×10-4,则当溶液中c(HCO ):c(CO
):c(CO )=2:1时,溶液的pH=
)=2:1时,溶液的pH=_______
(6)0.1mol·L-1 Na2CO3溶液中c(OH-)-c(H+)=_______ [用含c(HCO )、c(H2CO3)的关系式表示]
)、c(H2CO3)的关系式表示]
(7)向Na2CO3溶液中加入明矾会产生沉淀和气体,请写出相关的离子方程式:_______
(1)若在空气中加热MgCl2·6H2O,生成的是Mg(OH)Cl或MgO,写出生成Mg(OH)Cl关反应的化学方程式
(2)用电解法制取金属镁时,需要无水氯化镁。需要在干燥的HCl气流中加热MgCl2·6H2O,才能得到无水MgCl2,其原因是
(3)在25℃下,向浓度均为0.1 mol·L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成
Ⅱ.现有常温下的0.1mol·L-1纯碱溶液。
(4)你认为该溶液呈碱性的原因是(用离子方程式表示):
(5)已知25℃时,Kh=2×10-4,则当溶液中c(HCO
 ):c(CO
):c(CO )=2:1时,溶液的pH=
)=2:1时,溶液的pH=(6)0.1mol·L-1 Na2CO3溶液中c(OH-)-c(H+)=
 )、c(H2CO3)的关系式表示]
)、c(H2CO3)的关系式表示](7)向Na2CO3溶液中加入明矾会产生沉淀和气体,请写出相关的离子方程式:
您最近一年使用:0次
3 . T1、T2两种温度下 在水中的沉淀溶解平衡曲线如图所示,请回答下列问题。
在水中的沉淀溶解平衡曲线如图所示,请回答下列问题。
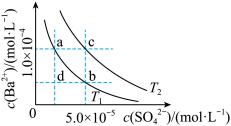
(1)T1___________ T2 (填“>”“<”或“=”),T2温度时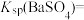
___________ 。
(2)根据T1温度时 的沉淀溶解平衡曲线,判断下列说法正确的是
的沉淀溶解平衡曲线,判断下列说法正确的是___________ (填序号)。
A.加入 固体可由a点变为b点
固体可由a点变为b点
B.T1温度下,在T1曲线上方区域(不含曲线)的任意一点时,均有 沉淀生成
沉淀生成
C.蒸发溶剂可能由d点变为T1,曲线上a、b之间(不含a、b)的某一点
D.升温可由b点变为d点
(3) T2温度时,现有0.2mol的 沉淀,每次用1 L饱和
沉淀,每次用1 L饱和 溶液(浓度为1.7mol/L)处理。若使
溶液(浓度为1.7mol/L)处理。若使 中的
中的 全部转化到溶液中,需要反复处理
全部转化到溶液中,需要反复处理___________ 次[提示: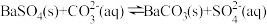
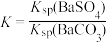 ,
,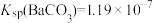 ]。
]。
 在水中的沉淀溶解平衡曲线如图所示,请回答下列问题。
在水中的沉淀溶解平衡曲线如图所示,请回答下列问题。
(1)T1
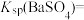
(2)根据T1温度时
 的沉淀溶解平衡曲线,判断下列说法正确的是
的沉淀溶解平衡曲线,判断下列说法正确的是A.加入
 固体可由a点变为b点
固体可由a点变为b点B.T1温度下,在T1曲线上方区域(不含曲线)的任意一点时,均有
 沉淀生成
沉淀生成C.蒸发溶剂可能由d点变为T1,曲线上a、b之间(不含a、b)的某一点
D.升温可由b点变为d点
(3) T2温度时,现有0.2mol的
 沉淀,每次用1 L饱和
沉淀,每次用1 L饱和 溶液(浓度为1.7mol/L)处理。若使
溶液(浓度为1.7mol/L)处理。若使 中的
中的 全部转化到溶液中,需要反复处理
全部转化到溶液中,需要反复处理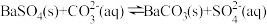
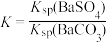 ,
,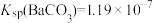 ]。
]。
您最近一年使用:0次
2021-08-07更新
|
1020次组卷
|
12卷引用:山东省东营市第一中学2021-2022学年高二上学期期中考试化学试题
山东省东营市第一中学2021-2022学年高二上学期期中考试化学试题鲁科版(2019)选择性必修1第3章 物质在水溶液中的行为 第3节 沉淀溶解平衡 课时2 Ksp图象及其相关计算高中必刷题高二选择性必修1第三章 水溶液中的离子反应与平衡 第四节 沉淀溶解平衡 课时2 Ksp图像及其相关计算(已下线)第3章 章末检测-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)课选择性必修1 专题3 第四单元 课时2 Ksp相关计算及其图像分析(已下线)3.4.1 沉淀溶解平衡-2021-2022学年高二化学课后培优练(人教版选修4)(已下线)3.4.2 沉淀溶解平衡的应用-2021-2022学年高二化学课后培优练(人教版选修4)(已下线)3.4.1 难溶电解质的沉淀溶解平衡(素养提优B练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)(已下线)3.4.1 沉淀溶解平衡-2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)3.4.2沉淀溶解平衡原理的应用 课中微专题(11) 沉淀溶解平衡图像分析上海市向明中学 2023-2024学年高三上学期9月质量监控化学试题
解题方法
4 . Ⅰ.请用相关术语回答下列问题:
(1)已知NaHA水溶液呈碱性。
①用离子方程式及文字表示NaHA水溶液呈碱性的原因__________________ 。
②在NaHA水溶液中各离子浓度的大小关系是______________ 。
(2)25℃时,向浓度均为0.1mol·L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成__________ 沉淀(填化学式),生成该沉淀的离子方程式为__________________ 。已知25℃时Ksp[Mg(OH)2]=1.8×10-11,Ksp[Cu(OH)2]=2.2×10-20。
Ⅱ.已知二元酸H2A在水中存在以下电离:H2A=H++HA-,HA- H++A2-。试回答下列问题:
H++A2-。试回答下列问题:
(3)NaHA溶液呈________ (填“酸”、“碱”或“中”)性,理由是___________________ 。
(4)某温度下,向10mL、0.1mol/L NaHA溶液中加入0.1mol/L KOH溶液VmL至中性,此时溶液中以下关系一定正确的是_________ (填写字母)。
(1)已知NaHA水溶液呈碱性。
①用离子方程式及文字表示NaHA水溶液呈碱性的原因
②在NaHA水溶液中各离子浓度的大小关系是
(2)25℃时,向浓度均为0.1mol·L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成
Ⅱ.已知二元酸H2A在水中存在以下电离:H2A=H++HA-,HA-
 H++A2-。试回答下列问题:
H++A2-。试回答下列问题:(3)NaHA溶液呈
(4)某温度下,向10mL、0.1mol/L NaHA溶液中加入0.1mol/L KOH溶液VmL至中性,此时溶液中以下关系一定正确的是
| A.溶液pH=7 | B.水的离子积Kw=[c2(OH-)] |
| C.V=10 | D.c(K+)<c(Na+) |
您最近一年使用:0次



