1 . 某废水中含有 和
和 ,若始终保持
,若始终保持 饱和,且
饱和,且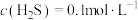 ,调节pH使
,调节pH使 和
和 形成硫化物而分离,体系中pH与
形成硫化物而分离,体系中pH与 关系如图所示(c为
关系如图所示(c为 、
、 、
、 、
、 的浓度)。下列说法正确的是
的浓度)。下列说法正确的是
 和
和 ,若始终保持
,若始终保持 饱和,且
饱和,且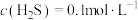 ,调节pH使
,调节pH使 和
和 形成硫化物而分离,体系中pH与
形成硫化物而分离,体系中pH与 关系如图所示(c为
关系如图所示(c为 、
、 、
、 、
、 的浓度)。下列说法正确的是
的浓度)。下列说法正确的是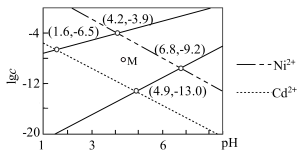
A. |
B.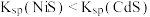 |
C.调节pH同时沉淀 和 和 时, 时,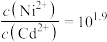 |
D.M点条件下能生成 沉淀,不能生成 沉淀,不能生成 沉淀 沉淀 |
您最近半年使用:0次
2 . 某科研人员以废镍催化剂(主要成分为NiO,另含Fe2O3、CaO、CuO、BaO)为原料回收镍,工艺流程如图。
回答下列问题:
(1)为提高“酸浸”时镍的浸取率,可采取的措施有___________ (写一条);
(2)浸出渣主要成分为___________ (填化学式);
(3)“除铜”时,写出生成S的离子方程式___________ ;
(4)“氧化”的目的是将溶液中Fe2+氧化为Fe3+,该步骤温度不能太高的原因是___________ ;
(5)“调pH”时,pH的控制范围为___________ ;
(6)用可溶性碳酸盐,可以浸取CaSO4固体,在溶液浸取过程发生反应:CaSO4(s) (ag)
(ag) CaCO3(s)
CaCO3(s) (aq)。已知:298K时,KspCaCO32.8010-9,KspCaSO44.9010-5,则此温度下该反应的平衡常数K为
(aq)。已知:298K时,KspCaCO32.8010-9,KspCaSO44.9010-5,则此温度下该反应的平衡常数K为___________ 。

| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
| 开始沉淀的pH | 1.5 | 6.5 | 7.7 |
| 沉淀完全的pH | 3.7 | 9.7 | 9.2 |
(1)为提高“酸浸”时镍的浸取率,可采取的措施有
(2)浸出渣主要成分为
(3)“除铜”时,写出生成S的离子方程式
(4)“氧化”的目的是将溶液中Fe2+氧化为Fe3+,该步骤温度不能太高的原因是
(5)“调pH”时,pH的控制范围为
(6)用可溶性碳酸盐,可以浸取CaSO4固体,在溶液浸取过程发生反应:CaSO4(s)
 (ag)
(ag) CaCO3(s)
CaCO3(s) (aq)。已知:298K时,KspCaCO32.8010-9,KspCaSO44.9010-5,则此温度下该反应的平衡常数K为
(aq)。已知:298K时,KspCaCO32.8010-9,KspCaSO44.9010-5,则此温度下该反应的平衡常数K为
您最近半年使用:0次
3 . 已知Ksp(AgCl)=1.8×10-10,Ksp(AgBr)=5.4×10-13,Ksp(Ag2CrO4)=2.0×10-12.某溶液中含有Cl-、Br-和 的浓度均为0.010mol•L-1,向该溶液中逐滴加入0.010mol•L-1AgNO3溶液时,三种阴离子产生沉淀的先后顺序为
的浓度均为0.010mol•L-1,向该溶液中逐滴加入0.010mol•L-1AgNO3溶液时,三种阴离子产生沉淀的先后顺序为
 的浓度均为0.010mol•L-1,向该溶液中逐滴加入0.010mol•L-1AgNO3溶液时,三种阴离子产生沉淀的先后顺序为
的浓度均为0.010mol•L-1,向该溶液中逐滴加入0.010mol•L-1AgNO3溶液时,三种阴离子产生沉淀的先后顺序为A.Br-、Cl-、 | B. 、Br-、Cl- 、Br-、Cl- | C.Cl-、Br-、 | D.Br-、 、Cl- 、Cl- |
您最近半年使用:0次
4 . 常温下进行下列实验,根据实验操作或目的所得的结论正确的是
| 选项 | 实验操作或目的 | 结论 |
| A | 向浓度均为0.1mol·L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成蓝色沉淀 | Ksp[Mg(OH)2]<Ksp[Cu(OH)2] |
| B | 通过加碱使废水中的c(Cr3+)降至1×10-5mol·L-1(已知常温下Ksp[Cr(OH)3]=1×10-32) | 加碱后废水的pH=5 |
| C | 向饱和Na2CO3溶液中加入少量BaSO4粉末,过滤,向洗净的沉淀中滴加稀盐酸,有气泡产生 | Ksp(BaCO3)<Ksp(BaSO4) |
| D | 测定水体中氯化物含量时,采用标准硝酸银溶液进行滴定。(已知常温下Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.3×10-17) | 滴定时可采用KI作为指示剂 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
5 . 下列实验的设计方案、现象和结论有错误的是
| 选项 | 实验目的 | 设计方案和实验现象 | 结论 |
| A | 检验菠菜中是否含有铁元素 | 取少量菠菜叶剪碎研磨后加水搅拌,取上层清液于试管中,加入稀硝酸后,再加入 溶液,溶液变红 溶液,溶液变红 | 菠菜中含有铁元素 |
| B | 检验尿液中是否含有葡萄糖 | 取尿液适量,向其中加入 至溶液呈碱性,加入新制的 至溶液呈碱性,加入新制的 悬浊液,加热煮沸,产生砖红色沉淀 悬浊液,加热煮沸,产生砖红色沉淀 | 尿液中含有葡萄糖 |
| C | 比较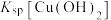 和 和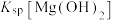 大小 大小 | 向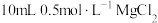 溶液中滴加 溶液中滴加 溶液,充分反应产生白色沉淀,再滴加 溶液,充分反应产生白色沉淀,再滴加 溶液,沉淀变蓝 溶液,沉淀变蓝 | 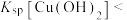 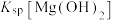 |
| D | 比较配离子 、 、 的稳定性 的稳定性 | 将 \固体溶于水,加入适量浓盐酸后,再加入少量 \固体溶于水,加入适量浓盐酸后,再加入少量 固体。溶液先由粉红色变为蓝色,再由蓝色变成粉红色(已知: 固体。溶液先由粉红色变为蓝色,再由蓝色变成粉红色(已知: 呈粉红色, 呈粉红色, 呈蓝色, 呈蓝色, 呈无色) 呈无色) | 稳定性: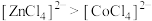 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2024-02-27更新
|
217次组卷
|
3卷引用:山东省威海市2023-2024学年高三上学期期末考试化学试题
6 . 如图为 、
、 和
和 在水中达沉淀溶解平衡时的pM-pH关系图(
在水中达沉淀溶解平衡时的pM-pH关系图( ;
; 可认为M离子沉淀完全)。下列叙述正确的是
可认为M离子沉淀完全)。下列叙述正确的是

 、
、 和
和 在水中达沉淀溶解平衡时的pM-pH关系图(
在水中达沉淀溶解平衡时的pM-pH关系图( ;
; 可认为M离子沉淀完全)。下列叙述正确的是
可认为M离子沉淀完全)。下列叙述正确的是
A.由a点可求得 |
B. 时 时 的溶解度为 的溶解度为 |
C.浓度均为 的 的 和 和 不能通过分步沉淀进行分离 不能通过分步沉淀进行分离 |
D. 、 、 混合溶液中 混合溶液中 时二者不会同时沉淀 时二者不会同时沉淀 |
您最近半年使用:0次
7 . 常温下, 和
和 沉淀溶解平衡曲线如图所示。下列说法正确的是
沉淀溶解平衡曲线如图所示。下列说法正确的是

 和
和 沉淀溶解平衡曲线如图所示。下列说法正确的是
沉淀溶解平衡曲线如图所示。下列说法正确的是
A.线Ⅰ表示 的变化情况 的变化情况 |
B.a点, |
C.b点条件下既可生成 沉淀,也可生成 沉淀,也可生成 沉淀 沉淀 |
D. 的平衡常数 的平衡常数 |
您最近半年使用:0次
8 . 工业上以富钒炉渣(主要含FeO·V2O3、V2O5和少量的SiO2、Al2O3等)为原料制备V2O5的工艺流程如下:
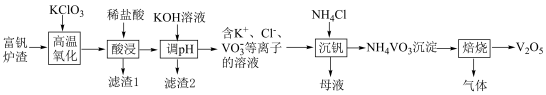
已知:①+ 5价钒元素在溶液中的存在形式与溶液pH的关系:
②Ksp[Fe(OH)3]=2.6×10–39;Ksp[Al(OH)3]=1.0×10–33;Ksp(NH4VO3)=1.6×10–3
回答下列问题:
(1)“高温氧化”前将富钒炉渣研磨粉碎的目的是___________ ;“高温氧化”过程中发生主要反应的化学方程式为___________ 。
(2)滤渣1的主要成分为___________ ;“调pH”时需将Fe3+、Al3+除尽(浓度≤1×10–5 mol∙L–1时,可认为已除尽),需调节pH的范围为___________ 。
(3)若“沉钒”前溶液中c(VO )=0.2 mol∙L–1,忽略溶液体积变化,为使钒元素的沉降率达到99%,至少应调节c(NH
)=0.2 mol∙L–1,忽略溶液体积变化,为使钒元素的沉降率达到99%,至少应调节c(NH )为
)为___________ mol·L–1。过滤、洗涤、干燥得到NH4VO3沉淀,检验NH4VO3沉淀是否洗净的操作是___________ 。
(4)“焙烧”时生成两种参与大气循环的无毒物质,则该反应的化学方程式为___________ 。

已知:①+ 5价钒元素在溶液中的存在形式与溶液pH的关系:
| 溶液pH | <1.0 | 1.0~4.0 | 4.0~6.0 | 6.0~8.5 | 8.5~13.0 | >13.0 |
| 钒元素存在形式 | VO | V2O5 | 多矾酸根 | VO | 多矾酸根 | VO |
| 备注 | 多矾酸盐在水中溶解度较小 | |||||
回答下列问题:
(1)“高温氧化”前将富钒炉渣研磨粉碎的目的是
(2)滤渣1的主要成分为
(3)若“沉钒”前溶液中c(VO
 )=0.2 mol∙L–1,忽略溶液体积变化,为使钒元素的沉降率达到99%,至少应调节c(NH
)=0.2 mol∙L–1,忽略溶液体积变化,为使钒元素的沉降率达到99%,至少应调节c(NH )为
)为(4)“焙烧”时生成两种参与大气循环的无毒物质,则该反应的化学方程式为
您最近半年使用:0次
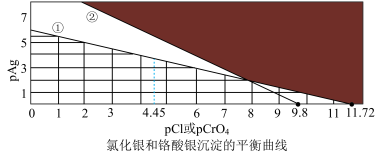
9 . AgCl和Ag2CrO4(砖红色都是难溶电解质,常温下以 对pCl和pCrO4作图的沉淀平衡曲线如图所示。下列说法正确的是
对pCl和pCrO4作图的沉淀平衡曲线如图所示。下列说法正确的是
 对pCl和pCrO4作图的沉淀平衡曲线如图所示。下列说法正确的是
对pCl和pCrO4作图的沉淀平衡曲线如图所示。下列说法正确的是
A.阴影区域 和 和 都沉淀 都沉淀 |
B. |
C.向含有 的 的 溶液中加入 溶液中加入 ,白色固体逐渐变为砖红色 ,白色固体逐渐变为砖红色 |
D.用硝酸银标准液滴定溶液中的 ,作指示剂的 ,作指示剂的 浓度在0.01mol/L左右时滴定误差很大 浓度在0.01mol/L左右时滴定误差很大 |
您最近半年使用:0次
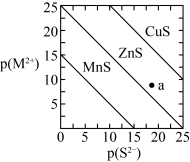
10 . 已知:一定温度下, 。三种金属硫化物在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是
。三种金属硫化物在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是
 。三种金属硫化物在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是
。三种金属硫化物在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是
A.a点有 沉淀生成 沉淀生成 |
B.可用 除去 除去 溶液中混有的少量 溶液中混有的少量 |
C.向 悬浊液中加入少量水,平衡向溶解的方向移动, 悬浊液中加入少量水,平衡向溶解的方向移动, 减小 减小 |
D. 和 和 共存的悬浊液中, 共存的悬浊液中, |
您最近半年使用:0次



