1 . 常温下进行下列实验,根据实验操作或目的所得的结论正确的是
| 选项 | 实验操作或目的 | 结论 |
| A | 向浓度均为0.1mol·L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成蓝色沉淀 | Ksp[Mg(OH)2]<Ksp[Cu(OH)2] |
| B | 通过加碱使废水中的c(Cr3+)降至1×10-5mol·L-1(已知常温下Ksp[Cr(OH)3]=1×10-32) | 加碱后废水的pH=5 |
| C | 向饱和Na2CO3溶液中加入少量BaSO4粉末,过滤,向洗净的沉淀中滴加稀盐酸,有气泡产生 | Ksp(BaCO3)<Ksp(BaSO4) |
| D | 测定水体中氯化物含量时,采用标准硝酸银溶液进行滴定。(已知常温下Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.3×10-17) | 滴定时可采用KI作为指示剂 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2 . 已知:一定温度下, 。三种金属硫化物在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是
。三种金属硫化物在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是
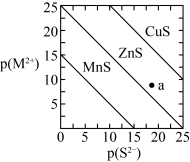
 。三种金属硫化物在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是
。三种金属硫化物在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是
A.a点有 沉淀生成 沉淀生成 |
B.可用 除去 除去 溶液中混有的少量 溶液中混有的少量 |
C.向 悬浊液中加入少量水,平衡向溶解的方向移动, 悬浊液中加入少量水,平衡向溶解的方向移动, 减小 减小 |
D. 和 和 共存的悬浊液中, 共存的悬浊液中, |
您最近一年使用:0次
3 . 下列实验操作、现象或数据和结论均准确无误的是
| 选项 | 实验操作 | 实验现象或数据 | 结论 |
| A | 在0.1mol/LZnSO4溶液中滴加少量等浓度的K2S溶液,再加入少量等浓度的CuSO4溶液 | 先产生白色沉淀,后产生黑色沉淀 | Ksp(ZnS)>Ksp(CuS) |
| B | 向BaCl2溶液中通入SO2,然后再通入A气体 | 开始无明显现象,通入A后产生白色沉淀 | 白色沉淀为BaSO4 |
| C | 用pH试纸测定等浓度的CH3COONa溶液和NaClO溶液的pH | NaClO溶液pH大于CH3COONa溶液 | 酸性:CH3COOH>HClO |
| D | 以酚酞为指示剂,用0.1mol/LNaOH溶液滴定0.1mol/L草酸溶液 | 溶液由无色变浅红色,且30s内不恢复原色;V(NaOH)=2V(草酸) | 草酸为二元弱酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
4 . 在T℃时,AgBr在水中的沉淀溶解平衡曲线如图所示。又知T℃时AgCl的Ksp=4×10-10,下列说法不正确的是

| A.在T℃时,AgBr的Ksp为4.9×10-13 |
| B.在AgBr饱和溶液中加入NaBr固体,可使溶液由c点到b点 |
| C.图中a点对应的是AgBr的不饱和溶液 |
| D.在T℃时,AgCl(s)+Br-(aq)⇌AgBr(s)+Cl-(aq)的平衡常数K≈816 |
您最近一年使用:0次
2023-12-16更新
|
172次组卷
|
77卷引用:山东省兖州市2019-2020学年高二上学期期中考试化学试题
山东省兖州市2019-2020学年高二上学期期中考试化学试题(已下线)2014年化学高考总复习课时演练 8-4难溶电解质的溶解平衡练习卷(已下线)2014高考名师推荐化学溶度积、沉淀的生成、溶解、转化(已下线)2014高考名师推荐化学--预测152014-2015山西省太原市五中高二上学期期末化学理试卷2016届宁夏银川市第二中学高三上学期统练(三)化学试卷2015-2016学年广西柳州铁路第一中学高二上段考理化学卷2015-2016学年黑龙江大庆一中高二下假期验收化学试卷2015-2016学年山东省菏泽市高二上学期期末考试化学试卷2015-2016学年湖北省宜昌市示范高中高二下期中化学试卷2017届江西省赣中南五校高三上学期第一次模拟考试化学试卷2016-2017学年湖南省长沙一中高二上期中化学卷2016-2017学年辽宁省盘锦高中高二上期中化学卷2016-2017学年江西省南昌市八一中学等五校高二上联考二化学试卷2016-2017学年福建省泉州市南安第一中学高二下学期第一次阶段考试(3月)化学试卷湖南省岳阳市第一中学2016-2017学年高二下学期期中考试化学试题四川省资阳市2016-2017学年高二下学期期末考试化学试题宁夏育才中学孔德校区2017-2018学年高二12月月考化学试题河南省南阳市第一中学2017-2018学年高二上学期第三次月考化学试题河南省滑县第二高级中学2017-2018学年高二12月月考化学试题四川省宜宾市南溪一中2017-2018学年高二下学期第一次月考化学试题(已下线)2018年11月16日 《每日一题》人教选修4-沉淀溶解平衡曲线及应用人教版高二化学选修4 第三章 第四节 难溶电解质的溶解平衡练习题【全国百强校】黑龙江省大庆第一中学2018-2019学年高二上学期期末考试化学试题(已下线)专题8.4 难溶电解质的溶解平衡(讲)-《2020年高考一轮复习讲练测》陕西省咸阳市武功县2020届高三上学期第一次模拟考试化学试题山东省章丘四中2019—2020学年高二上学期12月第二次阶段测试化学试题河北省邯郸市大名县第一中学2019-2020学年高二上学期12月月考化学试题(清北组)2019年秋高三化学复习强化练习—— 难溶电解质的沉淀溶解平衡陕西省西安中学2019-2020学年高二12月月考化学试题吉林省长春市实验中学2019-2020学年高二上学期期末考试化学试题夯基提能2020届高三化学选择题对题专练——选修4化学反应原理——沉淀溶解平衡的曲线分析2020届人教版高三专题基础复习专题8《水溶液中的离子平衡》测试卷2020届高三化学化学二轮复习——常考题型:浓度积及浓度积常数【精编24题】广西钦州市2019-2020学年高二下学期期末教学质量监测化学试题鲁科版(2019)高二选择性必修第一册第3章 物质在水溶液中的行为 第3节 沉淀溶解平衡 高效手册河北省石家庄市藁城区第一中学2019-2020学年高二上学期第三次月考化学试题河北省任丘市第一中学2020-2021学年高二上学期第二次阶段考试化学试题山西省运城市临猗县临晋中学2020-2021学年高二上学期12月月考化学试题甘肃省白银市会宁县2020-2021学年高二上学期期末考试化学试题黑龙江省哈尔滨市呼兰区第一中学校等三校2020-2021学年高二上学期期末联考化学试题宁夏吴忠中学2020-2021学年高二上学期期末考试化学试题重庆实验中学2020-2021学年高二上学期第二阶段考试化学试题黑龙江省龙东南六校2020-2021学年高二上学期期末联考化学试题安徽省安庆市第十中学2020-2021学年高二5月月考化学试题陕西省咸阳市实验中学2020-2021学年高二下学期第三次月考化学试题(已下线)第26讲 难溶电解质的溶解平衡(精讲)-2022年一轮复习讲练测(已下线)考点26 难溶电解质的溶解平衡-备战2022年高考化学一轮复习考点帮(全国通用)河北省石家庄市辛集市第一中学2020-2021学年高二月考第四次考试(一)化学试题河北省石家庄市第一中学2020-2021学年高二上学期学情反馈(一) 化学试题四川省绵阳市南山中学实验学校2022届高三上学学期开学考试化学试题甘肃省白银市第八中学2021-2022学年高二上学期第二次月考(11月)化学试题(已下线)3.4.1 沉淀溶解平衡原理(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)广东省揭阳市揭西县2021-2022学年高二上学期期末考试化学试题天津市五校联考2021-2022学年高二上学期期末考试化学试题河北省保定市博野中学2021-2022学年高二上学期12月月考化学试题甘肃省张掖市第二中学2021-2022学年高二上学期期末考试化学试题河南省九师联盟2021-2022学年高二下学期4月质量检测化学试题(已下线)押全国卷理综第12题 水溶液中的离子平衡-备战2022年高考化学临考题号押题(全国卷)广东省普宁市华侨中学2021-2022学年高二下学期期中考试化学试题山东省德州市2020-2021学年高二上学期反应原理月考(A)化学试题(已下线)第15练 以Ksp的计算突破溶解平衡-2022年【暑假分层作业】高二化学(2023届一轮复习通用)云南省玉龙县第一中学2021-2022学年高二下学期3月份考试化学试题辽宁省沈阳市铁西区重点协作校2021-2022学年高二上学期期中考试化学试题河南省中原名校2021-2022学年高二下学期第一次联考化学试题江西省重点校2022-2023学年高三上学期第二次联考化学试题.云南省玉溪市易门县一中2021-2022学年高二下学期3月月考化学试题江西省丰城市第九中学2021-2022学年高二上学期第一次月考化学试题作业(二十二) 沉淀的溶解与生成、转化及应用第三章 水溶液中的离子反应与平衡 第四节 沉淀溶解平衡 第2课时 沉淀溶解平衡的应用西省西安市铁一中学2023-2024学年高二上学期期中质量检测化学试题(已下线)电离 水解 溶解平衡图像天津市第四十二中学2023-2024学年高二上学期第二次月考化学试题 天津市静海区第一中学2023-2024学年高二上学期12月月考化学试题广东省清远市阳山县南阳中学2023-2024学年高二上学期第二次月考(期中)化学试题陕西省西安市阎良区关山中学2023-2024学年高二上学期第三次质量检测化学试题河北省石家庄市西山学校2023-2024学年高二上学期期末考试化学试题
5 . 已知:Ksp(AgCl)=1.8×10-10 ,Ksp(AgI)=1.5×10-16,Ksp(Ag2CrO4)=2.0×10-12,则下列难溶盐的饱和溶液中,Ag+浓度大小顺序正确的是
| A.AgCl>AgI>Ag2CrO4 | B.AgCl>Ag2CrO4>AgI |
| C.Ag2CrO4>AgCl>AgI | D.Ag2CrO4>AgI>AgCl |
您最近一年使用:0次
2023-08-14更新
|
1014次组卷
|
55卷引用:2012-2013学年山东省济宁市泗水一中高二12月质量检测化学试卷
(已下线)2012-2013学年山东省济宁市泗水一中高二12月质量检测化学试卷(已下线)山东省邹城市2018-2019学年高二上学期12月月考化学试卷2010年普通高等学校招生全国统一考试化学试题(海南卷)2010年高考化学试题分项专题十 电解质溶液(已下线)2010年北京五中高二下学期期末考试化学试题(已下线)2010—2011学年山西省大同一中高二上学期期末考试化学试卷(已下线)2011-2012学年湖北省襄阳市四校高二上学期期中考试化学试卷(已下线)2011-2012学年江西省九江一中高二上学期第二次月考化学试卷(已下线)2011-2012学年江苏省南京三中高二下学期期末考试化学选修试卷(已下线)2011-2012学年河北省元氏一中高二上学期期中考试化学试卷(已下线)2012-2013学年福建省南安一中高二上学期期末考试化学试卷(已下线)2013-2014学年湖北省恩施高中高二12月月考化学试卷2014-2015湖南省怀化市中小学课改高二上学期期末化学试卷2014-2015河北省隆化县存瑞中学高二下学期期中考试化学试卷2015-2016学年湖南省衡阳县高二上学期期末统考化学试卷2015-2016学年湖北省武汉三十九中高二上学期期末化学试卷2015-2016学年青海师大附属二中高二下4月月考化学试卷2015-2016学年福建师大附中高二下期中化学试卷2017届湖北省枣阳市高级中学高三上学期8月月考化学试卷2017届内蒙古赤峰二中高三上第二次月考化学试卷广西陆川县中学2017-2018学年高二上学期期中考试化学试题河北省衡水市安平中学2017-2018学年高二上学期期中考试化学试题高中化学人教版 选修四 第三章 水溶液中的离子反应 第四节 难溶电解质的溶解平衡 难溶电解质的溶解平衡内蒙古包头市第四中学2017-2018学年高二上学期期末考试化学试题(已下线)2018年11月15日 《每日一题》人教选修4-溶度积的应用【全国百强校】贵州省铜仁市第一中学2018-2019学年高二下学期开学考试化学试题步步为赢 高二化学暑假作业:作业十 水溶液中的离子平衡陕西省吴起高级中学2019-2020学年高二上学期期中考试化学(基础卷)试题(已下线)2019年11月13日 《每日一题》人教版(选修4)——溶度积的有关计算黑龙江省哈尔滨市第三中学2019-2020学年高二上学期期中考试化学(理)试题陕西省咸阳市西藏民族大学附属中学2019-2020学年高二上学期第二次月考化学试题2019年秋高三化学复习强化练习—— 与浓度积的相关计算(强化练)湖南省雅礼中学2019-2020学年高二上学期第一次月考化学试题吉林省通化市梅河口市博文学校2019-2020学年高二上学期第二次月考化学试题湖北省恩施州清江外国语学校2020-2021学年高二上学期10月月考化学试题河北省石家庄市辛集市第一中学2019-2020学年高二第二次考试(二)化学试题鲁科版(2019)高二选择性必修第一册第3章 物质在水溶液中的行为 第3节 沉淀溶解平衡人教版(2019)高二化学选择性必修1第三章 水溶液中的离子反应与平衡 第四节 沉淀溶解平衡湖南省长郡中学2020-2021学年高二上学期期中考试化学试题(已下线)练习14 难溶电解质的沉淀溶解平衡-2020-2021学年【补习教材·寒假作业】高二化学(苏教版)贵州省蟠龙高级中学2020-2021学年高二上学期第二次月考化学试题黑龙江省大庆中学2021-2022学年高二上学期期末考试化学试题(已下线)第33练 沉淀溶解平衡-2023年高考化学一轮复习小题多维练(全国通用)云南省楚雄天人中学2021-2022学年高二上学期12月月考化学试题(B卷)河南省新乡市第一中学2022-2023学年高二上学期第一次月考化学试题湖南省长沙市宁乡市四校联考2022-2023学年高二上学期11月月考化学试题湖北省罗田县第一中学2021-2022学年高二上学期12月月考化学试题山西省太原市英才学校2021-2022学年高二上学期第二次月考化学试题山东省潍坊第一中学2022-2023学年高二上学期期末考试化学试题(已下线)考点巩固卷09 水溶液中的离子反应与平衡(4大考点62题)-2024年高考化学一轮复习考点通关卷(新高考通用)第1课时 沉淀溶解平衡与溶度积作业(二十一) 沉淀溶解平衡与溶度积天津市第一中学2023-2024学年高二上学期期末考试化学试卷山东师大附中幸福柳分校2023-2024学年高二上学期12月份化学学科阶段性测试(已下线)湖南省郴州市临武县第一中学2023-2024学年高三下学期5月期中化学试题
6 . 工业上以黄铁矿(主要成分为FeS2,含有少量NiS、CuS、SiO2等杂质)为原料制备K4[Fe(CN)6]·3H2O,工艺流程如图:

下列说法错误的是

下列说法错误的是
| A.“焙烧”时氧化产物有Fe2O3和SO2 |
B.“溶液Ⅰ”中主要反应的离子方程式为 |
C.“调pH”分离  与 与 、 、 是利用了它们氢氧化物 是利用了它们氢氧化物 的不同 的不同 |
| D.“一系列操作”为过滤、洗涤、干燥 |
您最近一年使用:0次
7 . 某温度下,分别向 浓度均为
浓度均为 的
的 和
和 溶液中滴加
溶液中滴加 的
的 溶液,滴加过程中溶液中
溶液,滴加过程中溶液中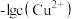 和
和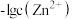 与
与 溶液体积
溶液体积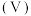 的关系如图所示[已知:
的关系如图所示[已知: ,
,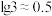 ]。下列说法正确的是
]。下列说法正确的是

 浓度均为
浓度均为 的
的 和
和 溶液中滴加
溶液中滴加 的
的 溶液,滴加过程中溶液中
溶液,滴加过程中溶液中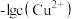 和
和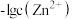 与
与 溶液体积
溶液体积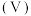 的关系如图所示[已知:
的关系如图所示[已知: ,
,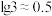 ]。下列说法正确的是
]。下列说法正确的是
A.溶液 : :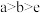 |
B.a点的 溶液中: 溶液中: |
C. 为滴定 为滴定 溶液的曲线 溶液的曲线 |
D. 点纵坐标约为33.9 点纵坐标约为33.9 |
您最近一年使用:0次
2022-12-09更新
|
530次组卷
|
4卷引用:山东省济宁市第一中学2022-2023学年高二上学期期末检测化学试题
8 . 下面是某科研小组利用废铁屑还原浸出软锰矿(主要成分为 )制备硫酸锰及电解其溶液制锰的工艺流程图:
)制备硫酸锰及电解其溶液制锰的工艺流程图: 、
、 、
、 、
、 等杂质金属离子;
等杂质金属离子;
②生成氢氧化物的 见下表:
见下表:
③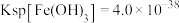 ,
,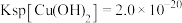 ,
, ,
, ,
,
请回答下列问题:
(1)“酸浸”前将原料粉碎的目的是___________ 。
(2)流程图中“①加入 ”的作用
”的作用___________ ,还可以用其他试剂___________ (填化学式)代替。
(3)流程图中“②调节 ”可以除去某种金属离子,应将溶液
”可以除去某种金属离子,应将溶液 调节控制的范围是
调节控制的范围是___________ ~7.6。
(4)向滤液I中加入 的作用是除去
的作用是除去 、
、 等离子,其中可以发生反应为
等离子,其中可以发生反应为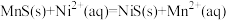 等。当该反应完全后,滤液2中的
等。当该反应完全后,滤液2中的 与
与 的物质的量浓度之比是
的物质的量浓度之比是___________ 。
(5) 具有净水作用,其净水的原理是
具有净水作用,其净水的原理是___________ 。(用离子方程式表示)
(6) 时
时 的溶液中,
的溶液中, 浓度的最大值为
浓度的最大值为
___________  。当溶液中加入
。当溶液中加入 溶液使
溶液使 时
时 开始溶解,则
开始溶解,则
___________ 。(溶液中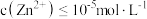 时
时 沉淀完全)
沉淀完全)
 )制备硫酸锰及电解其溶液制锰的工艺流程图:
)制备硫酸锰及电解其溶液制锰的工艺流程图:
 、
、 、
、 、
、 等杂质金属离子;
等杂质金属离子;②生成氢氧化物的
 见下表:
见下表:| 物质 |  |  |  |  |  |
开始沉淀的 | 7.5 | 2.7 | 7.7 | 7.6 | 8.3 |
完全沉淀的 | 9.7 | 3.7 | 8.4 | 8.2 | 9.8 |
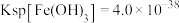 ,
,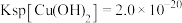 ,
, ,
, ,
,
请回答下列问题:
(1)“酸浸”前将原料粉碎的目的是
(2)流程图中“①加入
 ”的作用
”的作用(3)流程图中“②调节
 ”可以除去某种金属离子,应将溶液
”可以除去某种金属离子,应将溶液 调节控制的范围是
调节控制的范围是(4)向滤液I中加入
 的作用是除去
的作用是除去 、
、 等离子,其中可以发生反应为
等离子,其中可以发生反应为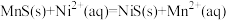 等。当该反应完全后,滤液2中的
等。当该反应完全后,滤液2中的 与
与 的物质的量浓度之比是
的物质的量浓度之比是(5)
 具有净水作用,其净水的原理是
具有净水作用,其净水的原理是(6)
 时
时 的溶液中,
的溶液中, 浓度的最大值为
浓度的最大值为
 。当溶液中加入
。当溶液中加入 溶液使
溶液使 时
时 开始溶解,则
开始溶解,则
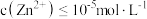 时
时 沉淀完全)
沉淀完全)
您最近一年使用:0次
名校
9 .  是一种二元弱酸,
是一种二元弱酸, 由于与空气中的某种成分作用而保持不变,已知
由于与空气中的某种成分作用而保持不变,已知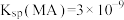 ,某水体中
,某水体中 (X为
(X为 、
、 、
、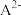 、
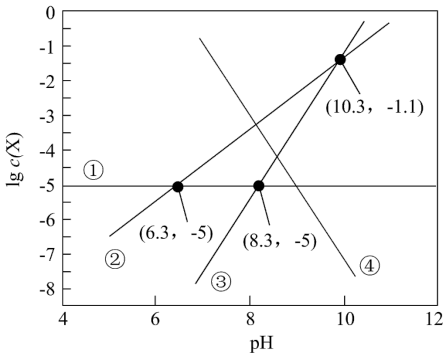
、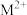 )与pH的关系如图所示。下列说法正确的是
)与pH的关系如图所示。下列说法正确的是
 是一种二元弱酸,
是一种二元弱酸, 由于与空气中的某种成分作用而保持不变,已知
由于与空气中的某种成分作用而保持不变,已知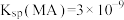 ,某水体中
,某水体中 (X为
(X为 、
、 、
、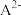 、
、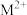 )与pH的关系如图所示。下列说法正确的是
)与pH的关系如图所示。下列说法正确的是
A.曲线②代表 |
B. 的一级电离常数为 的一级电离常数为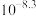 |
C.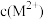 随pH升高而增大 随pH升高而增大 |
D.pH=10.3时,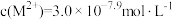 |
您最近一年使用:0次
2022-03-24更新
|
605次组卷
|
7卷引用:山东省济宁市实验中学2021-2022学年高三上学期期中考试化学试题
山东省济宁市实验中学2021-2022学年高三上学期期中考试化学试题山东省德州市2021-2022学年高三上学期期中化学考试试题(已下线)河北省普通高中学业水平选择性考试 化学预测卷(七)(已下线)【奋进985】04-备战2022年高考化学名校进阶模拟卷(通用版)(已下线)回归教材重难点07 图像数据和结果的分析-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)陕西省西安市长安区第一中学2022届高三第三次模拟考试理综化学试题(已下线)T15-溶液中的离子平衡
名校
10 . 由下列实验现象得出的结论正确的是
| 操作及现象 | 结论 | |
| A | 向盛有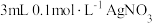 溶液的试管中加入 溶液的试管中加入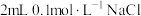 溶液产生白色沉淀,再加入几滴 溶液产生白色沉淀,再加入几滴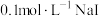 溶液,有黄色沉淀生成 溶液,有黄色沉淀生成 | 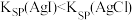 |
| B | 通过电解发生反应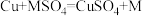 | 金属性: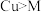 |
| C |  溶液中滴加 溶液中滴加 溶液,产生白色沉淀 溶液,产生白色沉淀 | 白色沉淀成分是 |
| D | 测定等物质的量浓度的 和 和 溶液的 溶液的 值,前者大 值,前者大 | 非金属性: |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-01-27更新
|
409次组卷
|
5卷引用:山东省济宁市2021-2022学年高二上学期期末考试化学试题



