下面是某科研小组利用废铁屑还原浸出软锰矿(主要成分为 )制备硫酸锰及电解其溶液制锰的工艺流程图:
)制备硫酸锰及电解其溶液制锰的工艺流程图: 、
、 、
、 、
、 等杂质金属离子;
等杂质金属离子;
②生成氢氧化物的 见下表:
见下表:
③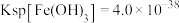 ,
,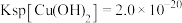 ,
, ,
, ,
,
请回答下列问题:
(1)“酸浸”前将原料粉碎的目的是___________ 。
(2)流程图中“①加入 ”的作用
”的作用___________ ,还可以用其他试剂___________ (填化学式)代替。
(3)流程图中“②调节 ”可以除去某种金属离子,应将溶液
”可以除去某种金属离子,应将溶液 调节控制的范围是
调节控制的范围是___________ ~7.6。
(4)向滤液I中加入 的作用是除去
的作用是除去 、
、 等离子,其中可以发生反应为
等离子,其中可以发生反应为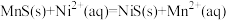 等。当该反应完全后,滤液2中的
等。当该反应完全后,滤液2中的 与
与 的物质的量浓度之比是
的物质的量浓度之比是___________ 。
(5) 具有净水作用,其净水的原理是
具有净水作用,其净水的原理是___________ 。(用离子方程式表示)
(6) 时
时 的溶液中,
的溶液中, 浓度的最大值为
浓度的最大值为
___________  。当溶液中加入
。当溶液中加入 溶液使
溶液使 时
时 开始溶解,则
开始溶解,则
___________ 。(溶液中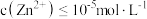 时
时 沉淀完全)
沉淀完全)
 )制备硫酸锰及电解其溶液制锰的工艺流程图:
)制备硫酸锰及电解其溶液制锰的工艺流程图:
 、
、 、
、 、
、 等杂质金属离子;
等杂质金属离子;②生成氢氧化物的
 见下表:
见下表:| 物质 |  |  |  |  |  |
开始沉淀的 | 7.5 | 2.7 | 7.7 | 7.6 | 8.3 |
完全沉淀的 | 9.7 | 3.7 | 8.4 | 8.2 | 9.8 |
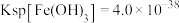 ,
,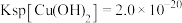 ,
, ,
, ,
,
请回答下列问题:
(1)“酸浸”前将原料粉碎的目的是
(2)流程图中“①加入
 ”的作用
”的作用(3)流程图中“②调节
 ”可以除去某种金属离子,应将溶液
”可以除去某种金属离子,应将溶液 调节控制的范围是
调节控制的范围是(4)向滤液I中加入
 的作用是除去
的作用是除去 、
、 等离子,其中可以发生反应为
等离子,其中可以发生反应为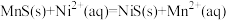 等。当该反应完全后,滤液2中的
等。当该反应完全后,滤液2中的 与
与 的物质的量浓度之比是
的物质的量浓度之比是(5)
 具有净水作用,其净水的原理是
具有净水作用,其净水的原理是(6)
 时
时 的溶液中,
的溶液中, 浓度的最大值为
浓度的最大值为
 。当溶液中加入
。当溶液中加入 溶液使
溶液使 时
时 开始溶解,则
开始溶解,则
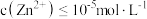 时
时 沉淀完全)
沉淀完全)
更新时间:2022-09-11 17:17:21
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】氯化亚砜(SOCl2)是一种有强烈刺激性气味的液体,遇水易反应生成二氧化硫和氯化氢,主要用于酰基氯化物及农药、医药、染料等的生产。实验室制备氯化亚砜的装置如图所示(部分夹持装置省略)。

已知:①甲装置中制备Cl2的化学方程式为MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O。
MnCl2+Cl2↑+2H2O。
②丙装置中发生的反应为2ClSO3H+S2Cl2+Cl2=2SOCl2+2SO2+2HCl。
请回答下列问题:
(1)仪器X的名称是____ 。甲装置中反应的离子方程式为____ 。
(2)试剂Y是____ 。
(3)戊装置中NaOH溶液的作用是____ 。
(4)若没有丁装置,丙装置中生成的氯化亚砜会与水反应,写出该反应的化学方程式:____ 。

已知:①甲装置中制备Cl2的化学方程式为MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O。
MnCl2+Cl2↑+2H2O。②丙装置中发生的反应为2ClSO3H+S2Cl2+Cl2=2SOCl2+2SO2+2HCl。
请回答下列问题:
(1)仪器X的名称是
(2)试剂Y是
(3)戊装置中NaOH溶液的作用是
(4)若没有丁装置,丙装置中生成的氯化亚砜会与水反应,写出该反应的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】某化学兴趣小组探究Na2SO3固体的热分解产物。
通过查阅资料可知:①4Na2SO3 Na2S+3Na2SO4。
Na2S+3Na2SO4。
②Na2S能与S反应生成Na2Sx,Na2Sx与酸反应生成S和H2S。
③BaS易溶于水。回答下面问题:
(1)硫元素在周期表的位置是___________ ,写出Na2S的电子式___________ 。
(2)Na2SO3溶液易被空气中的O2氧化,其氧化产物的化学式是___________ 。
(3)隔绝空气条件下,加热无水Na2SO3固体得到黄色固体A,过程中未检测到气体生成。黄色固体A加水得到浊液,放置得无色溶液B。
①检验分解产物Na2S:取少量溶液B,向其中滴加CuSO4溶液,产生黑色沉淀,证实有S2-。该反应的离子方程式为___________ 。
②黄色固体A中因为生成少量S单质而成黄色,加水得到浊液,放置得无色溶液B,用化学方程式表示浊液变澄清的原因是___________ 。
③检验分解产物Na2SO4:
步骤一:另取少量溶液B,加入足量盐酸,生成有臭鸡蛋气味的气体(H2S)和少量浅黄色沉淀,写出该步骤中涉及到的化学反应的离子方程式___________ 。
步骤二:利用离心机离心沉降(固液分离)后,___________ (填操作和现象),可证实分解产物中含有 。
。
通过查阅资料可知:①4Na2SO3
 Na2S+3Na2SO4。
Na2S+3Na2SO4。②Na2S能与S反应生成Na2Sx,Na2Sx与酸反应生成S和H2S。
③BaS易溶于水。回答下面问题:
(1)硫元素在周期表的位置是
(2)Na2SO3溶液易被空气中的O2氧化,其氧化产物的化学式是
(3)隔绝空气条件下,加热无水Na2SO3固体得到黄色固体A,过程中未检测到气体生成。黄色固体A加水得到浊液,放置得无色溶液B。
①检验分解产物Na2S:取少量溶液B,向其中滴加CuSO4溶液,产生黑色沉淀,证实有S2-。该反应的离子方程式为
②黄色固体A中因为生成少量S单质而成黄色,加水得到浊液,放置得无色溶液B,用化学方程式表示浊液变澄清的原因是
③检验分解产物Na2SO4:
步骤一:另取少量溶液B,加入足量盐酸,生成有臭鸡蛋气味的气体(H2S)和少量浅黄色沉淀,写出该步骤中涉及到的化学反应的离子方程式
步骤二:利用离心机离心沉降(固液分离)后,
 。
。
您最近一年使用:0次
【推荐3】下图是中学常见物质的转换关系图。包含了单质、氧化物、酸、碱、盐。其中A、B常温下都为无色液体,且组成元素相同,A、B、X、Y、E都为氧化物,X、E都为黑色固体,Y可用作干燥剂,F是大理石的主要成分,I为蓝色沉淀,L为不溶于稀硝酸的白色沉淀。
请回答:

(1) X在反应①中起____________ 作用。
(2)为什么Y可以用作干燥剂,用化学方程式表示_____________ ,Y所属物质类别是____________ (填序号)。
①金属氧化物;②碱性氧化物;③碱;④碱性干燥剂;⑤化合物;⑥盐
(3)写出反应⑥的离子方程式__________________ 。
(4)写出L的化学式_______________ 。
(5)上述①→⑦反应中属于复分解反应类型的有___________________ 。
请回答:

(1) X在反应①中起
(2)为什么Y可以用作干燥剂,用化学方程式表示
①金属氧化物;②碱性氧化物;③碱;④碱性干燥剂;⑤化合物;⑥盐
(3)写出反应⑥的离子方程式
(4)写出L的化学式
(5)上述①→⑦反应中属于复分解反应类型的有
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
【推荐1】察尔汗盐湖是我国最大的钾肥生成基地,生产过程中会产生大量水氯镁石(MgCl2·6H2O)。为实现资源综合利用,以水氯镁石为原料制轻质氧化镁。工艺如下:

按要求回答问题:
(1)锂与镁元素性质相似,写出向Li2SO4溶液中滴加Na2CO3溶液的离子方程式为___________ 。
(2)在“水浸”时适当升温的目的是___________ 。
(3)“沉镁”采用的温度为90℃~95℃,温度不宜超过95℃的理由是___________ 。
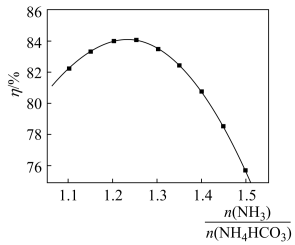
(4) 与沉镁效率(η)的关系如图所示,指出沉镁的
与沉镁效率(η)的关系如图所示,指出沉镁的 最佳范围为
最佳范围为___________ 。
(5)试说明“煅烧”后得到疏松多孔的MgO的原因是分解过程中产生大量的___________ 。
(6)“滤液”中的主要成分为___________ 。(填化学式)

按要求回答问题:
(1)锂与镁元素性质相似,写出向Li2SO4溶液中滴加Na2CO3溶液的离子方程式为
(2)在“水浸”时适当升温的目的是
(3)“沉镁”采用的温度为90℃~95℃,温度不宜超过95℃的理由是
(4)
 与沉镁效率(η)的关系如图所示,指出沉镁的
与沉镁效率(η)的关系如图所示,指出沉镁的 最佳范围为
最佳范围为
(5)试说明“煅烧”后得到疏松多孔的MgO的原因是分解过程中产生大量的
(6)“滤液”中的主要成分为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐2】铜镍电镀废水处理后得到电镀污泥,利用以下T艺可制备硫酸镍晶体( ):
):

已知:①电镀污泥含有 、
、 、
、 、
、 和
和 等。
等。
②该工艺条件下,几种金属离子开始沉淀和完全沉淀的pH如表所示:
|
|
|
| |
开始沉淀的pH | 6.3 | 2.2 | 4.3 | 7.2 |
完全沉淀的pH | 9.6 | 3.2 | 5.6 | 8.4 |
③ 易溶于水,难溶于乙醇。
易溶于水,难溶于乙醇。
请回答下列问题:
(1)“酸浸”步骤中,为了提高浸出速率,可采取的措施有
(2)滤渣2的主要成分为
(3)若上述流程省去“氧化”步骤,造成的后果是
(4)写出“沉镍”步骤中得到碱式碳酸镍[
 ]的离子方程式:
]的离子方程式:(5)一系列操作的实验步骤如下,请补充相关实验内容:
ⅰ.
ⅱ.将沉淀转移至烧杯中,滴加稀硫酸直至沉淀恰好完全溶解;
ⅲ.蒸发浓缩、冷却结晶,过滤得 晶体;
晶体;
ⅳ.用少量 晶体并晾干。
晶体并晾干。
(6)在空气中煅烧26.3g
 ,剩余固体的质量随时间变化的曲线如图所示,该曲线中D点所表示的氧化物中Ni、O的原子个数比为
,剩余固体的质量随时间变化的曲线如图所示,该曲线中D点所表示的氧化物中Ni、O的原子个数比为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐3】三草酸合铁(Ⅲ)酸钾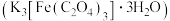 是一种经典的光敏剂,也是制备负载型活性铁催化剂的主要原料。用废铁屑(含少量
是一种经典的光敏剂,也是制备负载型活性铁催化剂的主要原料。用废铁屑(含少量 、
、 )先制备草酸铁,然后再制备三草酸合铁(Ⅲ)酸钾。
)先制备草酸铁,然后再制备三草酸合铁(Ⅲ)酸钾。
Ⅰ.制备草酸亚铁
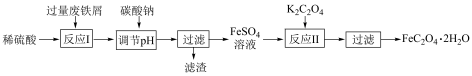
已知:部分氢氧化物沉淀时溶液的 如下表:
如下表:
(1)加入过量废铁屑的主要目的是___________。
(2)加入少量 后,混合溶液
后,混合溶液 范围应调控在___________。
范围应调控在___________。
(3)写出反应Ⅱ的离子方程式:___________ 。
(4)关于 溶液中有关离子浓度的说法正确的是___________。
溶液中有关离子浓度的说法正确的是___________。
Ⅱ.制备三草酸合铁(Ⅲ)酸钾
步骤一:在草酸亚铁固体中,加入饱和 溶液;
溶液;
步骤二:保持恒温40℃,边搅拌边缓慢加入 溶液,直至氧化完全;
溶液,直至氧化完全;
步骤三:将溶液加热至沸,加入饱和 溶液,溶液转为绿色,获得三草酸合铁(Ⅲ)酸钾溶液。
溶液,溶液转为绿色,获得三草酸合铁(Ⅲ)酸钾溶液。
(5)从步骤三所得溶液获得三草酸合铁(Ⅲ)酸钾晶体的操作依次为水浴浓缩、___________ 、___________ ,然后用乙醇淋洗。
(6)步骤二使用 做氧化剂,其优点是
做氧化剂,其优点是___________ ;滴加 时需保持恒温40℃,原因是
时需保持恒温40℃,原因是___________ 。
(7)三草酸合铁(Ⅲ)酸钾溶液中存在如下过程: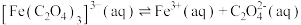 ,某同学想检验
,某同学想检验 的存在,结合
的存在,结合 属于难溶电解质的特点,他向三草酸合铁(Ⅲ)酸钾溶液中加入
属于难溶电解质的特点,他向三草酸合铁(Ⅲ)酸钾溶液中加入 溶液,并未看到有沉淀生成。从平衡角度解释上述现象
溶液,并未看到有沉淀生成。从平衡角度解释上述现象___________ 。
Ⅲ.三草酸合铁(Ⅲ)酸钾含量测定
测定三草酸合铁(Ⅲ)酸钾样品纯度的方法如下:
称取样品0.2415g,放入250mL锥形瓶中,加入25mL水和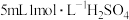 ,用
,用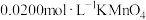 标准溶液滴定至终点,反应原理为:
标准溶液滴定至终点,反应原理为:
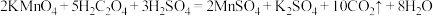
(8)确认滴定终点的操作是___________ 。
(9)若最终消耗 标准溶液23.19mL,则样品纯度为
标准溶液23.19mL,则样品纯度为___________ (精确到0.1%)。
(已知 的摩尔质量为
的摩尔质量为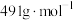 )
)
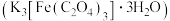 是一种经典的光敏剂,也是制备负载型活性铁催化剂的主要原料。用废铁屑(含少量
是一种经典的光敏剂,也是制备负载型活性铁催化剂的主要原料。用废铁屑(含少量 、
、 )先制备草酸铁,然后再制备三草酸合铁(Ⅲ)酸钾。
)先制备草酸铁,然后再制备三草酸合铁(Ⅲ)酸钾。Ⅰ.制备草酸亚铁

已知:部分氢氧化物沉淀时溶液的
 如下表:
如下表:| 沉淀物 |  |  |  |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
(1)加入过量废铁屑的主要目的是___________。
| A.提高铁的利用率 | B.除去溶液中的 |
C.防止 被氧化 被氧化 | D.抑制 的水解 的水解 |
(2)加入少量
 后,混合溶液
后,混合溶液 范围应调控在___________。
范围应调控在___________。| A.3.2以下 | B. | C.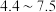 | D.7.5以上 |
(3)写出反应Ⅱ的离子方程式:
(4)关于
 溶液中有关离子浓度的说法正确的是___________。
溶液中有关离子浓度的说法正确的是___________。A.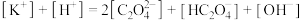 |
B. |
C.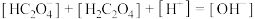 |
D.对溶液进行稀释,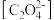 与 与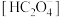 的比值变小 的比值变小 |
Ⅱ.制备三草酸合铁(Ⅲ)酸钾
步骤一:在草酸亚铁固体中,加入饱和
 溶液;
溶液;步骤二:保持恒温40℃,边搅拌边缓慢加入
 溶液,直至氧化完全;
溶液,直至氧化完全;步骤三:将溶液加热至沸,加入饱和
 溶液,溶液转为绿色,获得三草酸合铁(Ⅲ)酸钾溶液。
溶液,溶液转为绿色,获得三草酸合铁(Ⅲ)酸钾溶液。(5)从步骤三所得溶液获得三草酸合铁(Ⅲ)酸钾晶体的操作依次为水浴浓缩、
(6)步骤二使用
 做氧化剂,其优点是
做氧化剂,其优点是 时需保持恒温40℃,原因是
时需保持恒温40℃,原因是(7)三草酸合铁(Ⅲ)酸钾溶液中存在如下过程:
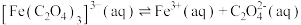 ,某同学想检验
,某同学想检验 的存在,结合
的存在,结合 属于难溶电解质的特点,他向三草酸合铁(Ⅲ)酸钾溶液中加入
属于难溶电解质的特点,他向三草酸合铁(Ⅲ)酸钾溶液中加入 溶液,并未看到有沉淀生成。从平衡角度解释上述现象
溶液,并未看到有沉淀生成。从平衡角度解释上述现象Ⅲ.三草酸合铁(Ⅲ)酸钾含量测定
测定三草酸合铁(Ⅲ)酸钾样品纯度的方法如下:
称取样品0.2415g,放入250mL锥形瓶中,加入25mL水和
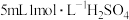 ,用
,用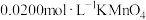 标准溶液滴定至终点,反应原理为:
标准溶液滴定至终点,反应原理为: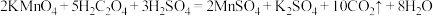
(8)确认滴定终点的操作是
(9)若最终消耗
 标准溶液23.19mL,则样品纯度为
标准溶液23.19mL,则样品纯度为(已知
 的摩尔质量为
的摩尔质量为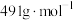 )
)
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐1】CoCl2·6H2O是一种饲料营养强化剂。以含钴废料(含少量Fe、Al等杂质)制取CoCl2·6H2O的一种新工艺流程如下图:
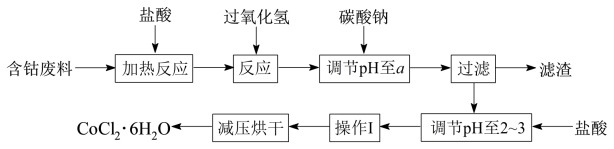
已知:①钴与盐酸反应的化学方程式为:Co+2HCl=CoCl2+H2↑
②CoCl2·6H2O熔点86℃,易溶于水、乙醚等;常温下稳定无毒,加热至110~120℃时,失去结晶水变成有毒的无水氯化钴。
③部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
请回答下列问题:
(1)加入过氧化氢的作用是(用离子方程式表示)____________________________________ 。
(2)加入碳酸钠调节pH至a得到的滤渣可部分溶于氢氧化钠溶液, a的范围是__________ 。
(3)操作Ⅰ包含3个基本实验操作,它们是__________________________________________ 。
(4)制得的CoCl2·6H2O需减压烘干的原因是_______________________________________ 。

已知:①钴与盐酸反应的化学方程式为:Co+2HCl=CoCl2+H2↑
②CoCl2·6H2O熔点86℃,易溶于水、乙醚等;常温下稳定无毒,加热至110~120℃时,失去结晶水变成有毒的无水氯化钴。
③部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 7.6 | 3.4 |
| 完全沉淀 | 4.1 | 9.7 | 9.2 | 5.2 |
请回答下列问题:
(1)加入过氧化氢的作用是(用离子方程式表示)
(2)加入碳酸钠调节pH至a得到的滤渣可部分溶于氢氧化钠溶液, a的范围是
(3)操作Ⅰ包含3个基本实验操作,它们是
(4)制得的CoCl2·6H2O需减压烘干的原因是
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
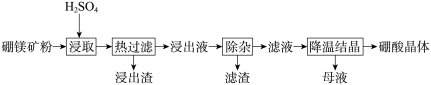
【推荐2】硼酸(H3BO3)大量应用于玻璃制造行业,以硼镁矿(2MgO•B2O3•H2O、SiO2及少量Fe3O4、CaCO3、Al2O3)为原料生产硼酸的工艺流程如下:
②298K下,常见金属氢氧化物的溶度积常数如下表:
(1)“浸取”时2MgO•B2O3•H2O发生的反应的化学方程式为___________ 。
(2)“浸取”后,采用“热过滤”的目的是___________ ,“浸出渣”的成分为___________ (填化学式)。
(3)“浸出液”显酸性, “除杂”时向浸出液中依次加入适量H2O2和MgO,除去的杂质离子是___________ 。
(4)“母液”可用于回收硫酸镁,已知硫酸镁的溶解度随温度变化的曲线如图,且溶液的沸点随压强增大而升高。为了从“母液”中充分回收MgSO4·H2O,应采取的措施是将“母液”蒸发浓缩后,最佳结晶条件是___________。
| 温度 |  |  |  |  |
| 溶解度 | 5.0g | 8.7g | 14.8g | 40.2g |
| Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
 | 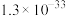 | 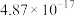 | 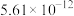 |
(1)“浸取”时2MgO•B2O3•H2O发生的反应的化学方程式为
(2)“浸取”后,采用“热过滤”的目的是
(3)“浸出液”显酸性, “除杂”时向浸出液中依次加入适量H2O2和MgO,除去的杂质离子是
(4)“母液”可用于回收硫酸镁,已知硫酸镁的溶解度随温度变化的曲线如图,且溶液的沸点随压强增大而升高。为了从“母液”中充分回收MgSO4·H2O,应采取的措施是将“母液”蒸发浓缩后,最佳结晶条件是___________。
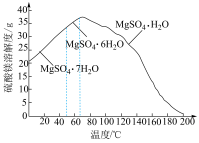
| A.升温结晶 | B.降温结晶 | C.加压升温结晶 | D.降压降温结晶 |
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐3】 和
和 都具有广泛的用途。
都具有广泛的用途。
Ⅰ.工业上用软锰矿(主要含 )和硫锰矿(主要含
)和硫锰矿(主要含 )联合制备
)联合制备 的流程如图。
的流程如图。
(1)为提高浸出速率,可采取的措施有_________________ (答出两条即可)。
(2)浸出过程中产生的 对
对 与
与 的反应起催化作用,机理如下。
的反应起催化作用,机理如下。
ⅰ.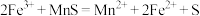 ;
;
ⅱ._________________ (离子方程式)。
(3)流程图中采用①和②共同除去浸出液中金属阳离子杂质,解释不能单独使用①去除这些杂质离子的原因:_____________ 。
(4)滤渣2的主要成分是_________________ 。
Ⅱ.以 溶液为原料,用图1装置(
溶液为原料,用图1装置(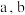 均为惰性电极)同步制备
均为惰性电极)同步制备 和
和 。
。_________________ 。
(6)图1中 电极上
电极上 的电解效率
的电解效率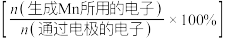 与溶液
与溶液 的关系如图2所示。随
的关系如图2所示。随 的增大,电解效率先增大后减小的原因是
的增大,电解效率先增大后减小的原因是_________________ 。
 和
和 都具有广泛的用途。
都具有广泛的用途。Ⅰ.工业上用软锰矿(主要含
 )和硫锰矿(主要含
)和硫锰矿(主要含 )联合制备
)联合制备 的流程如图。
的流程如图。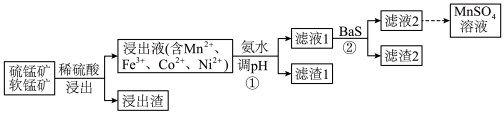
| 硫化物 |  |  |  |  (易溶) (易溶) |
 | 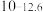 | 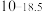 |  | |
| 氢氧化物 |  |  |  |  |
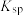 | 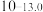 | 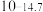 | 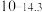 | 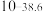 |
(1)为提高浸出速率,可采取的措施有
(2)浸出过程中产生的
 对
对 与
与 的反应起催化作用,机理如下。
的反应起催化作用,机理如下。ⅰ.
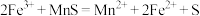 ;
;ⅱ.
(3)流程图中采用①和②共同除去浸出液中金属阳离子杂质,解释不能单独使用①去除这些杂质离子的原因:
(4)滤渣2的主要成分是
Ⅱ.以
 溶液为原料,用图1装置(
溶液为原料,用图1装置(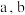 均为惰性电极)同步制备
均为惰性电极)同步制备 和
和 。
。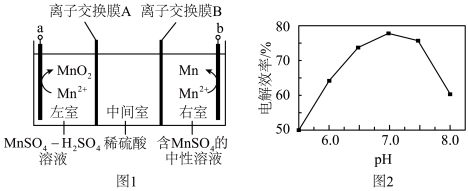
(6)图1中
 电极上
电极上 的电解效率
的电解效率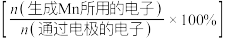 与溶液
与溶液 的关系如图2所示。随
的关系如图2所示。随 的增大,电解效率先增大后减小的原因是
的增大,电解效率先增大后减小的原因是
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐1】纳米氧化锌可作为一些催化剂的载体,二氧化锰也常作催化剂、氧化剂与去极化剂,用途非常广泛。工业上由软锰矿(主要成分为 )与锌精矿(主要成分为
)与锌精矿(主要成分为 )酸性共融法制备
)酸性共融法制备 及纳米
及纳米 ,工艺流程如图:
,工艺流程如图:

已知:P507(酸性磷酸酯)可作萃取剂分离锌、锰离子,它是一种不溶于水的淡黄色透明油状液体,属于酸性萃取剂。
请回答下列问题:
(1)实验室完成步骤③所用到的主要玻璃仪器是_______ (填写名称)。
(2)完成步骤④中发生反应的离子方程式:_______ 。
(3)写出步骤①酸浸时ZnS与MnO2发生的主要反应的化学方程式:_______ (无单质硫生成)。
(4)请分析下列说法正确的是_______。
(5)Zn(OH)2能溶于强酸性和强碱性溶液,常温下其溶度积常数Ksp=1.0×10-17,则步骤⑥调节溶液的pH=_______ 为宜。(当溶液中离子浓度≤10-5mol/L时认为已沉淀完全)
(6)MnO2常用于碱性锌锰电池中,电池的总反应为Zn+2MnO2+2H2O=2MnO(OH)+Zn(OH)2,请写出其正极反应式:_______ 。
 )与锌精矿(主要成分为
)与锌精矿(主要成分为 )酸性共融法制备
)酸性共融法制备 及纳米
及纳米 ,工艺流程如图:
,工艺流程如图:
已知:P507(酸性磷酸酯)可作萃取剂分离锌、锰离子,它是一种不溶于水的淡黄色透明油状液体,属于酸性萃取剂。
请回答下列问题:
(1)实验室完成步骤③所用到的主要玻璃仪器是
(2)完成步骤④中发生反应的离子方程式:
(3)写出步骤①酸浸时ZnS与MnO2发生的主要反应的化学方程式:
(4)请分析下列说法正确的是_______。
| A.步骤①将软锰矿与锌精矿粉碎或适当提高温度均能加快酸浸速率 |
| B.步骤③可用P507萃取分离ZnSO4和MnSO4的原因是P507与水互不相溶且ZnSO4在P507中溶解程度比在水中更大,而MnSO4在P507中溶解程度比在水中更小 |
| C.实验室进行步骤②过滤时,常用玻璃棒搅拌以加快过滤速率 |
| D.实验室完成步骤⑦焙烧时需用到坩埚、坩埚钳、三脚架、泥三角、酒精灯等仪器 |
(6)MnO2常用于碱性锌锰电池中,电池的总反应为Zn+2MnO2+2H2O=2MnO(OH)+Zn(OH)2,请写出其正极反应式:
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐2】实验室模拟“镁法工业烟气脱硫”并制备 ,其实验过程可表示为
,其实验过程可表示为
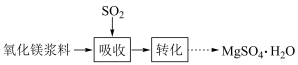
(1)在搅拌下向氧化镁浆料中匀速缓慢通入 气体,生成
气体,生成 ,反应为
,反应为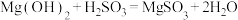 ,其平衡常数K与
,其平衡常数K与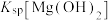 、
、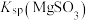 、
、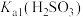 、
、 、
、 的代数关系式为
的代数关系式为
__________ 。
(2)①水浴加热氧化镁浆料,不一定能提高氧化镁浆料吸收 效率,说明原因
效率,说明原因__________ 。
②写出一种能提高氧化镁浆料吸收 效率的操作
效率的操作__________ 。
(3)在负载钴的分子筛催化剂作用下 被
被 氧化为
氧化为 。已知
。已知 的溶解度为
的溶解度为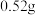 (19℃),若
(19℃),若 饱和溶液的密度以
饱和溶液的密度以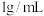 计。
计。
①计算19℃时,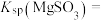
__________ 。
②写出 氧化溶液中
氧化溶液中 的离子方程式为
的离子方程式为__________ 。
③金属钴在周期表中的位置是__________ 。钴原子价电子排布式为__________ 。
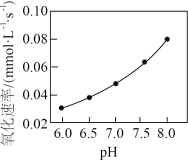
(4)在其他条件相同时,浆料中 被
被 氧化的速率随pH的变化如图所示。在
氧化的速率随pH的变化如图所示。在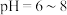 范围内,pH增大,浆料中
范围内,pH增大,浆料中 的氧化速率增大,其主要原因是
的氧化速率增大,其主要原因是__________ 。
 ,其实验过程可表示为
,其实验过程可表示为
(1)在搅拌下向氧化镁浆料中匀速缓慢通入
 气体,生成
气体,生成 ,反应为
,反应为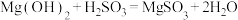 ,其平衡常数K与
,其平衡常数K与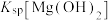 、
、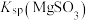 、
、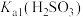 、
、 、
、 的代数关系式为
的代数关系式为
(2)①水浴加热氧化镁浆料,不一定能提高氧化镁浆料吸收
 效率,说明原因
效率,说明原因②写出一种能提高氧化镁浆料吸收
 效率的操作
效率的操作(3)在负载钴的分子筛催化剂作用下
 被
被 氧化为
氧化为 。已知
。已知 的溶解度为
的溶解度为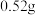 (19℃),若
(19℃),若 饱和溶液的密度以
饱和溶液的密度以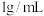 计。
计。①计算19℃时,
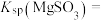
②写出
 氧化溶液中
氧化溶液中 的离子方程式为
的离子方程式为③金属钴在周期表中的位置是
(4)在其他条件相同时,浆料中
 被
被 氧化的速率随pH的变化如图所示。在
氧化的速率随pH的变化如图所示。在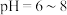 范围内,pH增大,浆料中
范围内,pH增大,浆料中 的氧化速率增大,其主要原因是
的氧化速率增大,其主要原因是
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐3】用镍铂合金废料(主要成分为 ,含少量
,含少量 )回收镍和铂,其工艺流程如图:
)回收镍和铂,其工艺流程如图: 的原子序数为78,推测其在元素周期表中的位置
的原子序数为78,推测其在元素周期表中的位置___________ 。
(2)含 滤渣(除
滤渣(除 外)的成分为
外)的成分为___________ 。
(3)用王水浸取“含 滤渣”可回收
滤渣”可回收 ,浸取时有
,浸取时有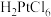 和
和 生成,写出该反应的化学方程式
生成,写出该反应的化学方程式___________ 。
(4)在常温下,若酸浸后溶液中各离子浓度均为 且“滤渣1”为
且“滤渣1”为 ,则“除钴”步骤需要控制溶液的
,则“除钴”步骤需要控制溶液的 范围是
范围是___________ 。已知: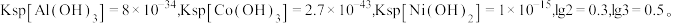
(5)加 调
调 的目的是
的目的是___________ 。
(6)“控温氧化”时控制其他条件一定, 的产率与温度和时间的关系如图。
的产率与温度和时间的关系如图。___________ 。
② 、
、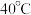 时反应后所得滤液主要为
时反应后所得滤液主要为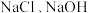 和
和 时反应后所得滤液主要为
时反应后所得滤液主要为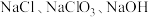 和
和 。反应相同时间,
。反应相同时间,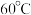 时
时 的产率低于
的产率低于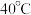 时,原因可能为
时,原因可能为___________ 。
(7) 产品中可能含少量
产品中可能含少量 ,为测定
,为测定 的纯度,进行如下实验:称取
的纯度,进行如下实验:称取 样品,加入足量硫酸后,再加入
样品,加入足量硫酸后,再加入 标准溶液充分反应,加水定容至
标准溶液充分反应,加水定容至 取出
取出 ,用
,用 标准溶液滴定,到达滴定终点时消耗
标准溶液滴定,到达滴定终点时消耗 标准溶液
标准溶液 。(
。( 被
被 还原为
还原为 ,不考虑
,不考虑 与
与 的反应),计算
的反应),计算 的质量分数
的质量分数___________ 。
 ,含少量
,含少量 )回收镍和铂,其工艺流程如图:
)回收镍和铂,其工艺流程如图: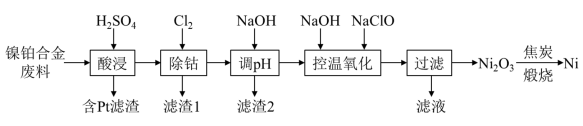
 的原子序数为78,推测其在元素周期表中的位置
的原子序数为78,推测其在元素周期表中的位置(2)含
 滤渣(除
滤渣(除 外)的成分为
外)的成分为(3)用王水浸取“含
 滤渣”可回收
滤渣”可回收 ,浸取时有
,浸取时有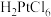 和
和 生成,写出该反应的化学方程式
生成,写出该反应的化学方程式(4)在常温下,若酸浸后溶液中各离子浓度均为
 且“滤渣1”为
且“滤渣1”为 ,则“除钴”步骤需要控制溶液的
,则“除钴”步骤需要控制溶液的 范围是
范围是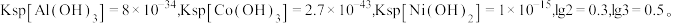
(5)加
 调
调 的目的是
的目的是(6)“控温氧化”时控制其他条件一定,
 的产率与温度和时间的关系如图。
的产率与温度和时间的关系如图。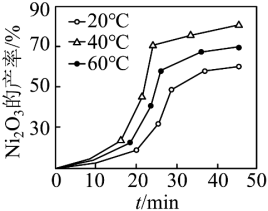
②
 、
、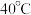 时反应后所得滤液主要为
时反应后所得滤液主要为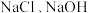 和
和 时反应后所得滤液主要为
时反应后所得滤液主要为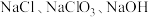 和
和 。反应相同时间,
。反应相同时间,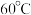 时
时 的产率低于
的产率低于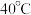 时,原因可能为
时,原因可能为(7)
 产品中可能含少量
产品中可能含少量 ,为测定
,为测定 的纯度,进行如下实验:称取
的纯度,进行如下实验:称取 样品,加入足量硫酸后,再加入
样品,加入足量硫酸后,再加入 标准溶液充分反应,加水定容至
标准溶液充分反应,加水定容至 取出
取出 ,用
,用 标准溶液滴定,到达滴定终点时消耗
标准溶液滴定,到达滴定终点时消耗 标准溶液
标准溶液 。(
。( 被
被 还原为
还原为 ,不考虑
,不考虑 与
与 的反应),计算
的反应),计算 的质量分数
的质量分数
您最近一年使用:0次



