名校
解题方法
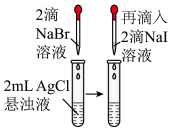
1 . 下列操作或装置能达到实验目的的是
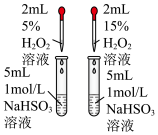
| A.证明Ksp(AgBr)>Ksp(AgI) | B.探究浓度对反应速率的影响 |
|
|
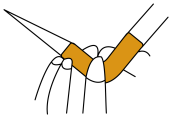
| C.碱式滴定管排气泡 | D.制备FeSO4固体 |
|
|
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2 . 化工生产中常用MnS作为沉淀剂除去工业废水中的Cu2+: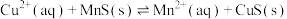 ,下列说法正确的是
,下列说法正确的是
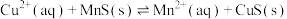 ,下列说法正确的是
,下列说法正确的是A.相同温度时,MnS的 比CuS的 比CuS的 小 小 |
B.该反应达到平衡时 |
C.设该反应的平衡常数为K,则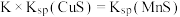 |
D.向平衡体系中加入少量 固体后, 固体后, 减小, 减小, 增大 增大 |
您最近一年使用:0次
3 . 某温度下,BaSO4的溶解平衡曲线如图,下列说法正确的是
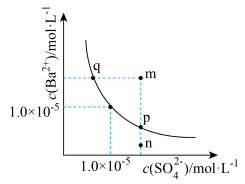
| A.该温度下Ba SO4的溶度积的数量级为10-5 |
| B.m、p点均有BaSO4沉淀析出,而n没有 |
| C.加入BaCl2固体可使p点移动到q点 |
| D.升高温度可使p点移动到q点 |
您最近一年使用:0次
4 . 下列关于难溶电解质沉淀溶解平衡的说法正确的是
| A.可直接根据Ksp的数值大小比较同温度下不同难溶电解质在水中的溶解度大小 |
| B.在AgCl的饱和溶液中,加入蒸馏水,Ksp(AgCl)不变 |
C.难溶电解质的溶解平衡过程是可逆的,且在平衡状态时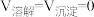 |
| D.25 ℃时,Ksp(AgCl)>Ksp(AgI),向AgCl的饱和溶液中加入少量KI固体,一定有黄色沉淀生成 |
您最近一年使用:0次
解题方法
5 . 广安代市镇火力发电厂需要燃烧大量的煤,产生大量CO2和SO2等,并留下大量煤渣,对环境有较大影响。其中一种不能继续燃烧的煤渣成分俗名叫“铁甲石”,主要成分为:Al2O3(15%~24%)、SiO2(40%~50%)、Fe2O3(0.5%~3.0%)、FeO(0.9%~2.0%)、CuO(8.5%~11.0%)以及其他不溶性杂质,铁甲石中的氧化铝难溶于酸,可以通过煅烧改变铁甲石结构,使其溶于酸。铁甲石经过下列化工工艺,可以制取无水CuCl2。

已知Cu2+、Fe2+、Fe3+、Al3+生成沉淀pH范围如下:
(1)第一次过滤的滤渣为___________ 。
(2)加H2O2后发生反应的离子方程式为___________ 。
(3)调节溶液pH需要控制的范围是___________ ,“调节溶液pH”的过程中除添加试剂,还需借助于___________ 测定溶液pH值。
(4)调节pH值用到的试剂或物质是___________(填下列字母)。
(5)从滤液2中得到无水CuCl2的操作为___________ 。

已知Cu2+、Fe2+、Fe3+、Al3+生成沉淀pH范围如下:
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 |
| 开始沉淀pH | 5.8 | 5.8 | 2.0 | 4.0 |
| 沉淀完成pH | 7.5 | 8.3 | 3.1 | 5.4 |
(1)第一次过滤的滤渣为
(2)加H2O2后发生反应的离子方程式为
(3)调节溶液pH需要控制的范围是
(4)调节pH值用到的试剂或物质是___________(填下列字母)。
| A.氢氧化钠 | B.氨水 | C.CuO | D.AlCl3 |
(5)从滤液2中得到无水CuCl2的操作为
您最近一年使用:0次
6 . 不同温度(T1和T2)时,硫酸钡在水中的沉淀溶解平衡曲线如图所示,已知硫酸钡在水中溶解时吸收热量。下列说法不正确的是
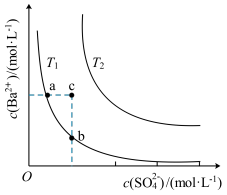
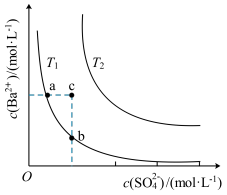
| A.T1<T2 |
| B.T2温度时c点对应的分散系均一稳定 |
| C.T1温度时b点和c点的Ksp相等 |
| D.加入BaCl2固体,可使分散系由a点变到b点 |
您最近一年使用:0次
7 . 已知Ksp(AgCl)=1.56×10-10、Ksp(AgBr)=7.7×10-13、Ksp(Ag2CrO4)=9×10-11,某溶液中含有Cl-、Br-和CrO ,浓度均为0.010mol/L,向该溶液中逐滴加入0.010mol/L的AgNO3溶液时,三种阴离子产生沉淀的先后顺序为
,浓度均为0.010mol/L,向该溶液中逐滴加入0.010mol/L的AgNO3溶液时,三种阴离子产生沉淀的先后顺序为
 ,浓度均为0.010mol/L,向该溶液中逐滴加入0.010mol/L的AgNO3溶液时,三种阴离子产生沉淀的先后顺序为
,浓度均为0.010mol/L,向该溶液中逐滴加入0.010mol/L的AgNO3溶液时,三种阴离子产生沉淀的先后顺序为A. Cl-、Br-、CrO | B.Br-、Cl-、CrO | C.CrO42-、Br-、Cl- | D.Br-、CrO 、Cl- 、Cl- |
您最近一年使用:0次
8 . 在一定温度下,AgCl(s) Ag+(aq)+Cl-(aq)体系中,c(Ag+)和c(Cl-)关系如图所示。下列说法正确的是
Ag+(aq)+Cl-(aq)体系中,c(Ag+)和c(Cl-)关系如图所示。下列说法正确的是

 Ag+(aq)+Cl-(aq)体系中,c(Ag+)和c(Cl-)关系如图所示。下列说法正确的是
Ag+(aq)+Cl-(aq)体系中,c(Ag+)和c(Cl-)关系如图所示。下列说法正确的是
| A.a、b、c三点对应的Ksp的大小关系为:Kspa>Kspb>Kspc |
| B.AgCl在c点的溶解度比b点的大 |
| C.AgCl溶于水形成的饱和溶液中,c(Ag+)=c(Cl-) |
| D.b点的溶液中加入AgNO3固体,c(Ag+)沿曲线向c点方向变化 |
您最近一年使用:0次
9 . 硫化汞(HgS)是一种难溶于水的红褐色颜料,其在水中的沉淀溶解平衡曲线如图所示(已知T1<T2),下列说法错误的是


| A.图中a点对应的是T2温度下HgS的不饱和溶液 |
| B.图中各点对应的Ksp的关系为:p<q |
| C.向p点的溶液中加入少量Hg(NO3)2固体,p点向a点转化 |
| D.升高温度,可实现p点向q点的转化 |
您最近一年使用:0次
10 . 要除去CuCl2溶液中的Fe3+ ,甲同学不知道调整溶液pH=4是否能达到除去Fe3+而不损失Cu2+的目的,乙同学认为可以通过计算确定,他查阅有关资料得到如下数据,常温下Fe(OH)3的溶度积Ksp = 1×10-38,Cu(OH)2的溶度积Ksp=3×10-20,通常认为残留在溶液中的离子浓度小于1×10-5 mol•L-1时就认为沉淀完全,设溶液中CuSO4的浓度为3.0mol•L-1,通过调节溶液pH除去Fe3+而不损失Cu2+,调节pH的取值范围
| A.3≤pH<4 | B.3≤pH≤4 |
| C.2<pH≤3 | D.2≤pH<3 |
您最近一年使用:0次