1 . 常温下,用 溶液分别滴定浓度均为
溶液分别滴定浓度均为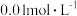 的
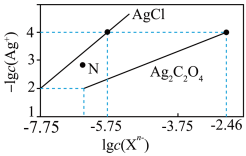
的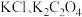 溶液,所得的沉淀溶解平衡图像如图所示(不考虑C2O
溶液,所得的沉淀溶解平衡图像如图所示(不考虑C2O 的水解)。其中Xn-表示
的水解)。其中Xn-表示 或
或 ,下列叙述错误的是
,下列叙述错误的是
 溶液分别滴定浓度均为
溶液分别滴定浓度均为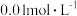 的
的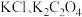 溶液,所得的沉淀溶解平衡图像如图所示(不考虑C2O
溶液,所得的沉淀溶解平衡图像如图所示(不考虑C2O 的水解)。其中Xn-表示
的水解)。其中Xn-表示 或
或 ,下列叙述错误的是
,下列叙述错误的是 
A.Ksp(Ag2C2O4)的数量级为 |
B. 点表示 点表示 的过饱和溶液 的过饱和溶液 |
C.向c(Cl-)=c(C2O )的混合溶液中滴入 )的混合溶液中滴入 溶液时,先生成 溶液时,先生成 沉淀 沉淀 |
D.常温下,Ag2C2O4(s)+2Cl-(aq) 2AgCl(s)+C2O 2AgCl(s)+C2O 的平衡常数为108.04 的平衡常数为108.04 |
您最近一年使用:0次
2019高二上·全国·专题练习
名校
解题方法
2 . 下列有关AgCl的沉淀溶解平衡的说法中,正确的是
| A.AgCl的生成和溶解不断进行,但速率相等 |
B.AgCl难溶于水,溶液中没有 和 和 |
| C.升高温度,AgCl的溶解度不变 |
| D.向AgCl的沉淀溶解平衡体系中加入NaCl固体,AgCl溶解的量不变 |
您最近一年使用:0次
2024-02-08更新
|
89次组卷
|
14卷引用:第33练 沉淀溶解平衡-2023年高考化学一轮复习小题多维练(全国通用)
(已下线)第33练 沉淀溶解平衡-2023年高考化学一轮复习小题多维练(全国通用)第四节 沉淀溶解平衡 第1课时 难溶电解质的沉淀溶解平衡天津市河北区2022-2023学年高二上学期期末考试化学试题黑龙江省哈尔滨市德强学校2022-2023学年高二上学期期末考试化学试题(已下线)2019年11月11日《每日一题》人教版(选修4)—— 沉淀溶解平衡的理解福建省莆田第十五中学2018-2019学年高二下学期期中测试化学试题内蒙古呼伦贝尔市满洲里市第一中学2022-2023学年高二下学期第一次月考化学试题(已下线)考点巩固卷09 水溶液中的离子反应与平衡(4大考点62题)-2024年高考化学一轮复习考点通关卷(新高考通用)3.4.1沉淀溶解平衡原理 课前(已下线)专题07 沉淀溶解平衡-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(天津专用)四川省宜宾市叙州区第一中学校2023-2024学年高二上学期1月期末化学试题安徽省阜阳市临泉第一中学(高铁分校)2023-2024学年高二上学期期末考试化学试题黑龙江省海林市朝鲜族中学2023-2024学年高二上学期第二次月考化学试题天津北京师范大学静海附属学校2023-2024学年高二上学期第三次月考化学试题
解题方法
3 . 室温下,通过下列实验探究NaHS溶液的性质。下列有关说法错误的是
| 实验 | 实验操作和现象 |
| 1 | 向0.1mol•L-1NaHS溶液中通入过量氯气,无淡黄色沉淀产生 |
| 2 | 向0.1mol•L-1NaHS溶液中加入等体积0.1mol•L-1NaOH溶液充分混合 |
| 3 | 向0.1mol•L-1NaHS溶液中滴加几滴酚酞试剂,溶液变红 |
| 4 | 向0.1mol•L-1NaHS溶液中滴加过量CuCl2溶液,产生黑色沉淀 |
| A.实验1说明HS-不能被氯气氧化 |
| B.实验2所得溶液中:c(Na+)=2[c(S2-)+c(HS-)+c(H2S)] |
| C.0.1mol•L-1NaHS溶液中:c(S2-)<c(H2S) |
| D.实验4反应静置后的上层清液中有:c(S2-)•c(Cu2+)=Ksp(CuS) |
您最近一年使用:0次
名校
4 . 室温下,下列实验探究方案设计正确且能达到探究目的的是
| 选项 | 探究方案 | 探究目的 |
| A | 向紫色石蕊溶液中通入过量二氧化硫,溶液先变红后褪色 | SO2为酸性氧化物且具有漂白性 |
| B | 将20℃ 0.5 mol·L-1CH3COONa溶液加热到40℃,用pH传感器测量溶液的pH | 温度对CH3COO-水解平衡的影响 |
| C | 向Na2CO3溶液中滴加浓盐酸,反应产生的气体直接通入Na2SiO3溶液中 | 非金属性:C>Si |
| D | 向浓度均为0.01mol·L-1的Na2CO3和Na2SO4的混合液中滴少量0.01mol·L-1的BaCl2溶液 | Ksp(BaCO3>Ksp(BaSO4) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
5 . 软锰矿的主要成分是MnO2,黄铁矿的主要成分是FeS2,还含有硅、铝的氧化物等杂质。工业上采用同槽酸浸工艺制备碳酸锰并回收硫酸铵,其主要流程如下:
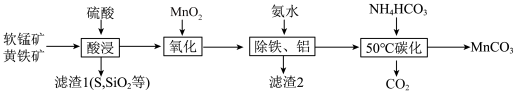
常温下此体系中各氢氧化物开始沉淀与沉淀完全时的pH范围如下表所示:
(1)为了提高锰元素的浸出率,在“浸取”时可采取的措施为_____ 。
(2)“氧化”中加入MnO2发生反应的离子方程式为_____ 。
(3)“除铁、铝”时,需要调节溶液pH的范围为_____ 。
(4)“50℃碳化”得到碳酸锰,反应为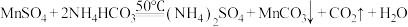 。能否用碳酸钠溶液代替碳酸氢铵溶液
。能否用碳酸钠溶液代替碳酸氢铵溶液_____ ,理由是_____ 。
(5)测定软锰矿中MnO2的纯度,称取0.1500 g软锰矿样品置于具塞锥形瓶中,加水润湿后,依次加入足量稀硫酸和过量KI溶液。盖上玻璃塞,充分摇匀后静置30 min,MnO2被还原为Mn2+(杂质不参加反应)。用0.1500 mol/LNa2S2O3标准溶液滴定生成的 ,消耗Na2S2O3标准溶液20.00 mL。滴定反应为
,消耗Na2S2O3标准溶液20.00 mL。滴定反应为 。计算软锰矿中MnO2的质量分数:
。计算软锰矿中MnO2的质量分数:_____ (写出计算过程)。

常温下此体系中各氢氧化物开始沉淀与沉淀完全时的pH范围如下表所示:
| pH值 | Mn(OH)2 | Fe(OH)2 | Al(OH)3 | Fe(OH)3 |
| 开始沉淀时 | 7.1 | 7.6 | 3.7 | 2.3 |
| 沉淀完全时 | 10.8 | 9.6 | 4.7 | 3.7 |
(1)为了提高锰元素的浸出率,在“浸取”时可采取的措施为
(2)“氧化”中加入MnO2发生反应的离子方程式为
(3)“除铁、铝”时,需要调节溶液pH的范围为
(4)“50℃碳化”得到碳酸锰,反应为
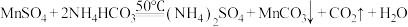 。能否用碳酸钠溶液代替碳酸氢铵溶液
。能否用碳酸钠溶液代替碳酸氢铵溶液(5)测定软锰矿中MnO2的纯度,称取0.1500 g软锰矿样品置于具塞锥形瓶中,加水润湿后,依次加入足量稀硫酸和过量KI溶液。盖上玻璃塞,充分摇匀后静置30 min,MnO2被还原为Mn2+(杂质不参加反应)。用0.1500 mol/LNa2S2O3标准溶液滴定生成的
 ,消耗Na2S2O3标准溶液20.00 mL。滴定反应为
,消耗Na2S2O3标准溶液20.00 mL。滴定反应为 。计算软锰矿中MnO2的质量分数:
。计算软锰矿中MnO2的质量分数:
您最近一年使用:0次
6 . 已知在常温时,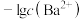 随
随 和
和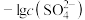 的变化趋势如图所示(A表示
的变化趋势如图所示(A表示 、B表示
、B表示 ),下列说法正确的是
),下列说法正确的是
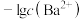 随
随 和
和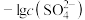 的变化趋势如图所示(A表示
的变化趋势如图所示(A表示 、B表示
、B表示 ),下列说法正确的是
),下列说法正确的是
| A.碳酸钡是一种比硫酸钡更难溶的物质 |
| B.图中m点碳酸钡的结晶速率大于其溶解速率 |
C.向含有 、 、 的溶液中逐滴加入 的溶液中逐滴加入 溶液, 溶液, 一定先沉淀 一定先沉淀 |
D.常温下反应 的平衡常数为10 的平衡常数为10 |
您最近一年使用:0次
2023-08-12更新
|
232次组卷
|
3卷引用:河南省周口市无锡天一企业管理有限公司等2校2022-2023学年高二上学期12月期末考试化学试题
名校
解题方法
7 . 已知室温下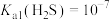 ,
,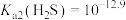 ;
;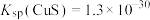 ,
,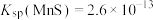 。下列说法正确的是
。下列说法正确的是
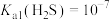 ,
,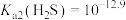 ;
; ,
,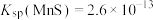 。下列说法正确的是
。下列说法正确的是A. 溶液显酸性 溶液显酸性 |
B.0.1mol/LH2S溶液的pH约为4,溶液中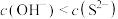 |
C.等浓度的 和 和 混合溶液中 混合溶液中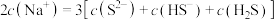 |
D.向等浓度的 和 和 混合溶液中滴加 混合溶液中滴加 溶液,先生成 溶液,先生成 沉淀 沉淀 |
您最近一年使用:0次
2023-08-12更新
|
285次组卷
|
2卷引用:河南省周口市无锡天一企业管理有限公司等2校2022-2023学年高二上学期12月期末考试化学试题
8 . 根据下列实验操作和现象所得到的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 某卤代烃与氢氧化钠的乙醇溶液混合共热,得到的气体通入酸性高锰酸钾溶液,酸性高锰酸钾溶液褪色 | 生成了不饱和烃 |
| B | 室温下,向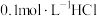 溶液中加入少量镁粉,产生大量气泡,测得溶液温度上升 溶液中加入少量镁粉,产生大量气泡,测得溶液温度上升 | 镁与盐酸反应放热 |
| C | 向盛有: 溶液的试管中滴加2~3滴 溶液的试管中滴加2~3滴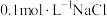 溶液,有白色沉淀生成,向其中继续滴加 溶液,有白色沉淀生成,向其中继续滴加 溶液,有黄色沉淀产生 溶液,有黄色沉淀产生 | 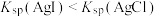 |
| D | 向 酸化的 酸化的 溶液中加入Cu片,观察Cu片溶解 溶液中加入Cu片,观察Cu片溶解 |  氧化性比 氧化性比 强 强 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
9 . 按要求回答下列问题:
(1)配制FeCl3溶液时,需将固体溶于较浓的盐酸后按需要进行稀释,用离子方程式解释其原因_______ 。
(2)常温下,浓度均为0.1mol/L的下列五种溶液的pH值如下表所示:
①根据表中数据,将pH=2的下列四种酸的溶液分别稀释100倍,pH变化最小的是_______ 。
A. HCN B. HClO C. H2CO3 D. CH3COOH
②根据以上数据,判断下列反应可以成立的是_______ 。(填字母)
A.CH3COOH+Na2CO3=NaHCO3+CH3COONa
B.CH3COOH+NaCN=CH3COONa+HCN
C.CO2+H2O+2NaClO=Na2CO3+2HClO
D.NaHCO3+HCN=NaCN+H2O+CO2
(3)已知在Cu2+、Mg2+、Fe2+浓度相同的溶液中,其开始沉淀时的pH如下:
①若向该溶液中滴加NaOH溶液,则离子沉淀先后顺序是_______ (填离子符号)。
②已知Ksp[Cu(OH)2]=2.5×10-20,若向该溶液中加入生石灰调节其pH,当pH=_______ 时,溶液中Cu2+沉淀完全。[已知1g2=0.3]
③下列说法不正确的是_______ (填字母)。
A.用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl少
B.一般地,物质的溶解度随温度的升高而增加,故物质的溶解大多是吸热的
C.除去溶液中的Mg2+,用OH-沉淀比用CO 好,说明Mg(OH)2的溶解度比MgCO3的大
好,说明Mg(OH)2的溶解度比MgCO3的大
D.沉淀反应中常加过量的沉淀剂,其目的是使沉淀更完全
(1)配制FeCl3溶液时,需将固体溶于较浓的盐酸后按需要进行稀释,用离子方程式解释其原因
(2)常温下,浓度均为0.1mol/L的下列五种溶液的pH值如下表所示:
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
A. HCN B. HClO C. H2CO3 D. CH3COOH
②根据以上数据,判断下列反应可以成立的是
A.CH3COOH+Na2CO3=NaHCO3+CH3COONa
B.CH3COOH+NaCN=CH3COONa+HCN
C.CO2+H2O+2NaClO=Na2CO3+2HClO
D.NaHCO3+HCN=NaCN+H2O+CO2
(3)已知在Cu2+、Mg2+、Fe2+浓度相同的溶液中,其开始沉淀时的pH如下:
| 离子 | Fe2+ | Cu2+ | Mg2+ |
| pH | 7.6 | 5.2 | 10.4 |
②已知Ksp[Cu(OH)2]=2.5×10-20,若向该溶液中加入生石灰调节其pH,当pH=
③下列说法不正确的是
A.用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl少
B.一般地,物质的溶解度随温度的升高而增加,故物质的溶解大多是吸热的
C.除去溶液中的Mg2+,用OH-沉淀比用CO
 好,说明Mg(OH)2的溶解度比MgCO3的大
好,说明Mg(OH)2的溶解度比MgCO3的大D.沉淀反应中常加过量的沉淀剂,其目的是使沉淀更完全
您最近一年使用:0次
2023-06-07更新
|
57次组卷
|
2卷引用:广东省梅州市大埔县虎山中学2022-2023学年高二上学期12月月考化学试题
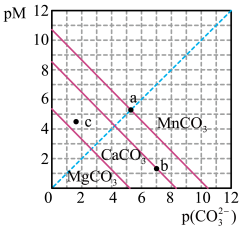
10 . 一定温度下,三种碳酸盐MCO3(M:Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线如下图所示。已知:pM=-lgc(M),pc(CO )=-lgc(CO
)=-lgc(CO )。下列说法正确的是
)。下列说法正确的是
 )=-lgc(CO
)=-lgc(CO )。下列说法正确的是
)。下列说法正确的是
| A.MgCO3、CaCO3、MnCO3的Ksp依次增大 |
B.a点可表示MnCO3的饱和溶液,且c(Mn2+)=c(CO ) ) |
C.b点可表示CaCO3的饱和溶液,且c(Ca2+)<c(CO ) ) |
D.c点可表示MgCO3的过饱和溶液,且c(Mg2+)>c(CO ) ) |
您最近一年使用:0次



