常温下,用 溶液分别滴定浓度均为
溶液分别滴定浓度均为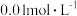 的
的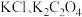 溶液,所得的沉淀溶解平衡图像如图所示(不考虑C2O
溶液,所得的沉淀溶解平衡图像如图所示(不考虑C2O 的水解)。其中Xn-表示
的水解)。其中Xn-表示 或
或 ,下列叙述错误的是
,下列叙述错误的是
 溶液分别滴定浓度均为
溶液分别滴定浓度均为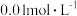 的
的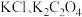 溶液,所得的沉淀溶解平衡图像如图所示(不考虑C2O
溶液,所得的沉淀溶解平衡图像如图所示(不考虑C2O 的水解)。其中Xn-表示
的水解)。其中Xn-表示 或
或 ,下列叙述错误的是
,下列叙述错误的是 
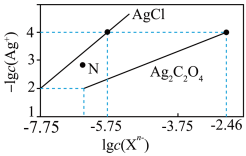
A.Ksp(Ag2C2O4)的数量级为 |
B. 点表示 点表示 的过饱和溶液 的过饱和溶液 |
C.向c(Cl-)=c(C2O )的混合溶液中滴入 )的混合溶液中滴入 溶液时,先生成 溶液时,先生成 沉淀 沉淀 |
D.常温下,Ag2C2O4(s)+2Cl-(aq) 2AgCl(s)+C2O 2AgCl(s)+C2O 的平衡常数为108.04 的平衡常数为108.04 |
更新时间:2024-02-17 15:53:36
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】依据下表有关铁难溶化合物的溶度积,有关说法正确的是
| 化合物 | 溶度积(25℃) | 化合物 | 溶度积(25℃) |
| FeCO3 | 3.2×10-11 | Fe(OH)3 | 4.0×10-38 |
| Fe(OH)2 | 8.0×10-11 | FeS | 6.3×10-18 |
| A.在c(CO32-)=0.1 mol·L-1的溶液中,c(Fe2+)≥3.2×10-10 mol·L-1 |
| B.将FeCl3和 FeCl2溶液分别调至PH=10,则c(Fe2+)< c(Fe3+) |
| C.增加溶液的酸性,有利于将Fe2+沉淀为FeS和FeCO3 |
| D.将反应液中的Fe2+氧化为 Fe3+有利于将铁从溶液中除尽 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】通过佛尔哈德法可以测定三氯氧磷(POCl3)样品中Cl元素的含量,实验步骤如下:
Ⅰ.取mg样品于锥形瓶中,加入足量的NaOH溶液,待完全反应后加稀硝酸至溶液显酸性;
Ⅱ.向锥形瓶中加入0.1000mol·L-1的AgNO3溶液50.00mL,使Cl-完全沉淀;
Ⅲ.向其中加入2mL硝基苯,用力摇动,使沉淀表面被有机物覆盖;
Ⅳ.加入指示剂,用cmol·mol-1NH4SCN溶液滴定过量Ag+至终点,记下所用体积为VmL。
已知:Ksp(AgCl)=3.2×10-10,Ksp(AgSCN)=2×10-12。
下列说法正确的是
Ⅰ.取mg样品于锥形瓶中,加入足量的NaOH溶液,待完全反应后加稀硝酸至溶液显酸性;
Ⅱ.向锥形瓶中加入0.1000mol·L-1的AgNO3溶液50.00mL,使Cl-完全沉淀;
Ⅲ.向其中加入2mL硝基苯,用力摇动,使沉淀表面被有机物覆盖;
Ⅳ.加入指示剂,用cmol·mol-1NH4SCN溶液滴定过量Ag+至终点,记下所用体积为VmL。
已知:Ksp(AgCl)=3.2×10-10,Ksp(AgSCN)=2×10-12。
下列说法正确的是
| A.滴定选用的指示剂为甲基橙 |
B.本次实验测得Cl元素的质量分数为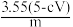 % % |
| C.硝基苯的作用为防止沉淀被氧化 |
| D.若取消步骤Ⅲ,测定结果偏大 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】 成本低、储氢量高,具有很好的发展前景。
成本低、储氢量高,具有很好的发展前景。 、
、 、
、 等盐溶液能提升
等盐溶液能提升 的水解制氢性能。
的水解制氢性能。 在
在 (
( 代表
代表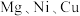 )溶液中水解的示意图如下:
)溶液中水解的示意图如下:
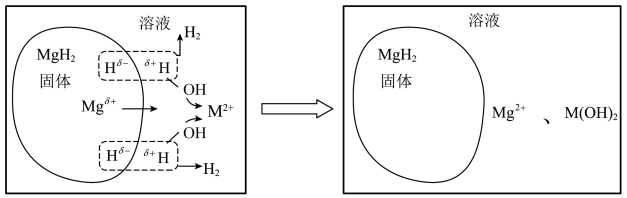
已知: 、
、 、
、 的
的 分别为
分别为 、
、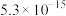 、
、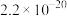 。下列说法正确的是
。下列说法正确的是
 成本低、储氢量高,具有很好的发展前景。
成本低、储氢量高,具有很好的发展前景。 、
、 、
、 等盐溶液能提升
等盐溶液能提升 的水解制氢性能。
的水解制氢性能。 在
在 (
( 代表
代表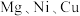 )溶液中水解的示意图如下:
)溶液中水解的示意图如下:
已知:
 、
、 、
、 的
的 分别为
分别为 、
、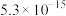 、
、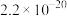 。下列说法正确的是
。下列说法正确的是A. 的水解反应属于复分解反应 的水解反应属于复分解反应 |
B.使用 溶液制备 溶液制备 比 比 溶液、 溶液、 溶液更易进行 溶液更易进行 |
C.溶液中 若更换为 若更换为 ,则生成 ,则生成 |
D.盐溶液换成硫酸溶液也能提高 的制氢性能 的制氢性能 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】室温下,通过下列实验探究 溶液的性质。
溶液的性质。
下列有关说法正确的是
 溶液的性质。
溶液的性质。| 选项 | 实验操作和现象 |
| 1 | 向0.1  溶液中滴加酸性高锰酸钾溶液,溶液紫红色褪去 溶液中滴加酸性高锰酸钾溶液,溶液紫红色褪去 |
| 2 | 用pH试纸测定0.1  溶液的pH,测得pH约为8 溶液的pH,测得pH约为8 |
| 3 | 向0.1  溶液中加入过量0.2 溶液中加入过量0.2  溶液,产生白色沉淀 溶液,产生白色沉淀 |
| 4 | 向0.1  溶液中滴加等体积的0.1 溶液中滴加等体积的0.1 HCl溶液,测得pH约为5.5 HCl溶液,测得pH约为5.5 |
A.实验1说明 具有漂白性 具有漂白性 |
B.0.1  溶液中存在 溶液中存在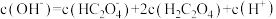 |
C.实验3反应静置后的上层清液中有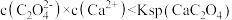 |
D.实验4得到的溶液中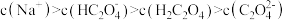 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】室温下,将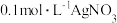 溶液和
溶液和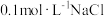 溶液等体积充分混合,一段时间后过滤,得滤液a和沉淀b。取等量的滤液a于两支试管中,分别滴加相同体积、浓度均为
溶液等体积充分混合,一段时间后过滤,得滤液a和沉淀b。取等量的滤液a于两支试管中,分别滴加相同体积、浓度均为 的
的 溶液和
溶液和 溶液,前者出现浑浊,后者溶液仍澄清;再取少量的沉淀b,滴加几滴氨水,沉淀逐渐溶解。下列说法正确的是
溶液,前者出现浑浊,后者溶液仍澄清;再取少量的沉淀b,滴加几滴氨水,沉淀逐渐溶解。下列说法正确的是
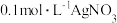 溶液和
溶液和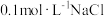 溶液等体积充分混合,一段时间后过滤,得滤液a和沉淀b。取等量的滤液a于两支试管中,分别滴加相同体积、浓度均为
溶液等体积充分混合,一段时间后过滤,得滤液a和沉淀b。取等量的滤液a于两支试管中,分别滴加相同体积、浓度均为 的
的 溶液和
溶液和 溶液,前者出现浑浊,后者溶液仍澄清;再取少量的沉淀b,滴加几滴氨水,沉淀逐渐溶解。下列说法正确的是
溶液,前者出现浑浊,后者溶液仍澄清;再取少量的沉淀b,滴加几滴氨水,沉淀逐渐溶解。下列说法正确的是A.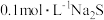 溶液中存在: 溶液中存在: |
B.过滤后所得滤液中一定存在: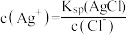 |
C.沉淀b中滴加氨水发生反应的离子方程式: |
D.从实验现象可以得出该温度下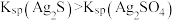 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】某废水处理过程中始终保持 ,通过调节pH使
,通过调节pH使 和
和 形成硫化物而分离,体系中pH与
形成硫化物而分离,体系中pH与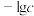 关系如下图所示,c为
关系如下图所示,c为 、
、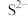 、
、 和
和 的浓度,单位为
的浓度,单位为 。已知:
。已知: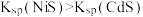 。下列说法正确的是
。下列说法正确的是
 ,通过调节pH使
,通过调节pH使 和
和 形成硫化物而分离,体系中pH与
形成硫化物而分离,体系中pH与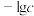 关系如下图所示,c为
关系如下图所示,c为 、
、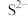 、
、 和
和 的浓度,单位为
的浓度,单位为 。已知:
。已知: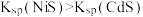 。下列说法正确的是
。下列说法正确的是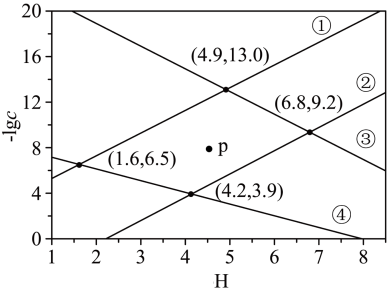
A.④为pH与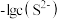 的关系曲线 的关系曲线 |
B.p点生成的沉淀中含有 和 和 |
C. 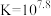 |
D.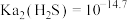 |
您最近一年使用:0次

 溶液浸泡
溶液浸泡 粉末,一段时间后过滤,向滤渣中加入过量盐酸,产生气泡,滤渣仍有剩余。已知
粉末,一段时间后过滤,向滤渣中加入过量盐酸,产生气泡,滤渣仍有剩余。已知 。下列说法正确的是
。下列说法正确的是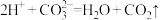
 且
且
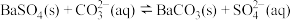 能够正向进行,则需要满足条件:
能够正向进行,则需要满足条件:
 ,
, (酸根离子)
(酸根离子) (酸根离子)。下列说法
(酸根离子)。下列说法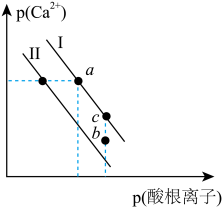
 沉淀溶解曲线
沉淀溶解曲线 气体,溶液中
气体,溶液中 不变
不变 ,
,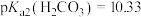
 溶液中平衡时
溶液中平衡时 物质的量分数
物质的量分数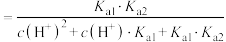
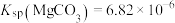 ,
,

 且调节溶液的pH=12时,有
且调节溶液的pH=12时,有 沉淀生成
沉淀生成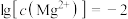 且调节溶液的pH=9时,平衡后溶液中存在:
且调节溶液的pH=9时,平衡后溶液中存在: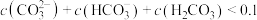
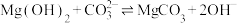 正向移动
正向移动

