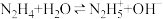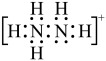室温下,通过下列实验探究 溶液的性质。
溶液的性质。
下列有关说法正确的是
 溶液的性质。
溶液的性质。| 选项 | 实验操作和现象 |
| 1 | 向0.1  溶液中滴加酸性高锰酸钾溶液,溶液紫红色褪去 溶液中滴加酸性高锰酸钾溶液,溶液紫红色褪去 |
| 2 | 用pH试纸测定0.1  溶液的pH,测得pH约为8 溶液的pH,测得pH约为8 |
| 3 | 向0.1  溶液中加入过量0.2 溶液中加入过量0.2  溶液,产生白色沉淀 溶液,产生白色沉淀 |
| 4 | 向0.1  溶液中滴加等体积的0.1 溶液中滴加等体积的0.1 HCl溶液,测得pH约为5.5 HCl溶液,测得pH约为5.5 |
A.实验1说明 具有漂白性 具有漂白性 |
B.0.1  溶液中存在 溶液中存在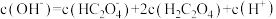 |
C.实验3反应静置后的上层清液中有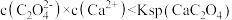 |
D.实验4得到的溶液中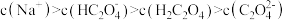 |
更新时间:2021-06-27 08:55:16
|
相似题推荐
单选题
|
较难
(0.4)
解题方法
【推荐1】已知某二元酸H2A的Ka1=1.1×10-3,Ka2=3.9×10-6。常温下,用0.10mol·L-1的KOH溶液滴定20.0mL0.10mol·L-1的NaHA溶液,溶液pH的变化曲线如图所示。下列叙述错误的是


| A.c点溶液pH在9~10之间 |
| B.b点的混合溶液中:c(Na+)=2c(A2-)+c(HA-) |
| C.a点的混合溶液中:c(Na+)>c(A2-)>c(K+)>c(HA-) |
| D.a、b、c三点中,c点水的电离程度最大 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】常温时,下列关于微粒浓度关系的说法正确的是
A.向 溶液加 溶液加 至中性: 至中性: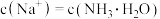 |
B. 的 的 溶液与 溶液与 的 的 溶液混合: 溶液混合: |
C. 溶液中: 溶液中: |
D.① 溶液,② 溶液,②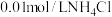 溶液,③ 溶液,③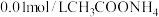 溶液,同温时 溶液,同温时 由大到小的顺序为:③>②>① 由大到小的顺序为:③>②>① |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】室温下,下列实验过程能达到预期目的的是
| 选项 | 实验过程 | 实验目的 |
| A | 向 NaCl、NaI 的混合溶液中滴加少量 AgNO3 溶液,生成淡黄色沉淀 | 证明 Ksp(AgCl)> Ksp(AgI) |
| B | 相同条件下,分别用 pH 试纸测定0.1 mol/LNaClO 溶液、0.1mol/LCH3COONa 溶液的 pH | 比较HClO 和 CH3COOH 的酸性强弱 |
| C | 苯和液溴的混合液中加入铁粉,将产生的气体通入硝酸酸化的AgNO3 溶液中,产生淡黄色沉淀 | 证明苯与液溴在Fe 催化下发生取代反应 |
| D | 向 NaAlO2 溶液中加入NaHCO3 溶液,观察到有白色沉淀生成 | 证明AlO 得质子的能力强于CO 得质子的能力强于CO |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】常温下,0.1mol/L 的下列溶液中,c(NH4+)最大的是( )
| A.NH4Cl | B.(NH4)2Fe(SO4)2 | C.(NH4)2CO3 | D.CH3COONH4 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】室温时,用0.100mol· L -1AgNO3溶液滴定50.0mL0.0500mol· L -1NaCl溶液的滴定曲线如图所示[pCl=-lg(Cl-)]。下列有关描述错误的是


| A.室温时Ksp(AgCl)的数量级为10-10 |
| B.室温时,各点Ksp(AgCl)的关系:a=b=c |
| C.相同实验条件下,若改用0.0400mol· L-1 NaCl溶液,反应终点b移动到d |
| D.相同实验条件下,若改用0.0500mol· L-1 NaBr溶液,反应终点b向e方向移动 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】已知25℃时,CaCO3饱和溶液中c(Ca2+)为5.3×10-5 mol·L-1 MgCO3的饱和溶液中c(Mg2+)为2.6×10-3 mol·L-1。若在5 mL浓度均为0.01 mol·L-1的CaCl2和MgCl2溶液中,逐滴加入5 mL 0.012 mol·L-1 Na2CO3溶液,充分反应后过滤得到溶液M和沉淀N(不考虑溶液体积的变化)。下列观点不正确的是
| A.25℃时,Ksp(CaCO3)=2.8×10-9 |
| B.加入Na2CO3溶液的过程中,先生成CaCO3沉淀 |
| C.滤液M中:c(Cl-)>c(Na+)>c(Mg2+)>c(CO32-)>c(OH-) |
D.滤液M中: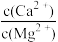 = =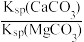 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】已知常温下,几种难溶电解质的溶度积(Ksp):
下列说法不正确的是( )
| 化学式 | Mg(OH)2 | MgF2 | Fe(OH)3 | AgCl | Cu(OH)2 | Ag2CrO4 |
| 溶度积 | 5.6×10-12 | 7.4×10-11 | 4 .0×10-38 | 1.8×10-10 | 2.2×10-20 | 2.0×10-12 |
下列说法不正确的是( )
| A.在Mg(OH)2 的悬浊液中加入少量的NH4Cl固体,c(Mg2+)增大 |
| B.在Mg(OH)2 的悬浊液中加入NaF 溶液后,Mg(OH)2 不可能转化为MgF2 |
| C.CuCl2溶液中混入了一定量的FeCl3溶液,可以通过向溶液中加入CuO的方法,调整溶液的pH,除去Fe3+杂质 |
| D.向浓度均为1×10-3mol/L 的KCl 和K2CrO4混合液中滴加1×10-3mo/LAgNO3溶液,Cl-先形成沉淀 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】根据下列实验操作和现象所得到的结论正确的是( )
| 选项 | 实验操作和现象 | 结论 |
| A | 将气体X分别通入溴水和酸性高锰酸钾溶液中,两溶液均褪色 | 气体X一定是SO2 |
| B | 向NaAlO2溶液中滴入NaHCO3溶液,产生白色沉淀 | AlO2-结合H+的能力比CO32-强 |
| C | 向某溶液中先滴加少量氯水,再滴加2滴KSCN溶液,溶液变成血红色 | 原溶液中一定含有Fe2+ |
| D | 在2mL0.01mol/L的Na2S溶液中先滴入几滴0.01mol/L ZnSO4溶液有白色沉淀,再滴入CuSO4溶液,又出现黑色沉淀 | Ksp(CuS)<Ksp(ZnS) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】下列根据实验操作和现象所得出的结论正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向硅酸钠溶液中滴加1滴酚酞,然后逐滴加入稀盐酸至红色褪去 | 2 min后,试管里出现凝胶 | 非金属性:Cl>Si |
| B | 向滴有甲基橙的AgNO3溶液中滴加KC1溶液 | 溶液由红色变为黄色 | KC1溶液具有碱性 |
| C | 在CuSO4溶液中加入KI溶液,再加入苯,振荡 | 有白色沉淀生成,苯层呈紫红色 | 白色沉淀可能为 CuI |
| D | 取久置的Na2O2粉末,向其中滴加过量的盐酸 | 产生无色气体 | Na2O2没有变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

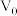 的HA、HB、HC溶液,分别加水稀释至体积为V,溶液pH随
的HA、HB、HC溶液,分别加水稀释至体积为V,溶液pH随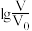 的变化关系如图所示,下列叙述正确的是
的变化关系如图所示,下列叙述正确的是
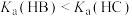
 点
点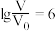 时,HA溶液的pH为8
时,HA溶液的pH为8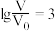 时,三种溶液同时升高温度,
时,三种溶液同时升高温度,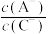 减小
减小 )为二元弱碱,在水中的电离方程式与氨相似。下列说法错误的是
)为二元弱碱,在水中的电离方程式与氨相似。下列说法错误的是