1 . 按要求回答问题
(1)一种电解法制备高纯铬和硫酸的简单装置如图所示,请回答下列问题。
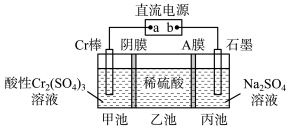
a为直流电源的_______ (填“正”或“负”)极;阳极反应式为_______ 工作时乙池中溶液的
_______ (填“增大”、“减小”或“不变”);若有 离子通过A膜,理论上阳极生成
离子通过A膜,理论上阳极生成_______  气体。
气体。
(2)为了验证 与
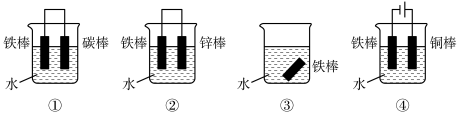
与 氧化性强弱,图中装置能达到实验目的是
氧化性强弱,图中装置能达到实验目的是_______ (填序号)。

(3)图中各个装置中铁棒被腐蚀由易到难的顺序是_______ 。
(4)甲醇( )燃料电池,两电极均为铂网,电解质溶液为
)燃料电池,两电极均为铂网,电解质溶液为 ,写出该原电池负极的电极反应式为
,写出该原电池负极的电极反应式为_______ 。
(1)一种电解法制备高纯铬和硫酸的简单装置如图所示,请回答下列问题。

a为直流电源的

 离子通过A膜,理论上阳极生成
离子通过A膜,理论上阳极生成 气体。
气体。(2)为了验证
 与
与 氧化性强弱,图中装置能达到实验目的是
氧化性强弱,图中装置能达到实验目的是
(3)图中各个装置中铁棒被腐蚀由易到难的顺序是

(4)甲醇(
 )燃料电池,两电极均为铂网,电解质溶液为
)燃料电池,两电极均为铂网,电解质溶液为 ,写出该原电池负极的电极反应式为
,写出该原电池负极的电极反应式为
您最近一年使用:0次
2022-03-20更新
|
151次组卷
|
3卷引用:福建省福州华侨中学2021-2022学年高二上学期期中考试化学试题
2 . 电化学原理在现实生活中有着十分广泛的应用。请回答下列问题:
(1)某研究性学习小组设计了如图所示装置探究钢铁的腐蚀与防护。

为防止金属Fe被腐蚀,可以采用上述_______ (填装置序号)装置原理进行防护;装置③中总反应的离子方程式为_______ 。
(2)电镀在工业上有着广泛的应用,可以镀锌、镀铜、镀金等。利用如图所示装置可以将铜牌变为银牌,即在铜牌表面电镀一层银,该电解池的阴极反应可表示为_______ 。

(3)钴(Co)的合金材料广泛应用于航空航天、机械制造等领域。用乙醇燃料电池作为电源电解含 的水溶液制备金属钴,其装置如图甲、乙。
的水溶液制备金属钴,其装置如图甲、乙。

①图乙中Co电极应连接乙醇燃料电池的_______ 极(填“a”或“b”。
②图甲中a极上发生的电极反应是_______ 。
③生成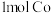 ,Ⅰ室溶液质量理论上减少
,Ⅰ室溶液质量理论上减少_______ g。
(1)某研究性学习小组设计了如图所示装置探究钢铁的腐蚀与防护。

为防止金属Fe被腐蚀,可以采用上述
(2)电镀在工业上有着广泛的应用,可以镀锌、镀铜、镀金等。利用如图所示装置可以将铜牌变为银牌,即在铜牌表面电镀一层银,该电解池的阴极反应可表示为

(3)钴(Co)的合金材料广泛应用于航空航天、机械制造等领域。用乙醇燃料电池作为电源电解含
 的水溶液制备金属钴,其装置如图甲、乙。
的水溶液制备金属钴,其装置如图甲、乙。
①图乙中Co电极应连接乙醇燃料电池的
②图甲中a极上发生的电极反应是
③生成
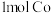 ,Ⅰ室溶液质量理论上减少
,Ⅰ室溶液质量理论上减少
您最近一年使用:0次
2022-01-16更新
|
228次组卷
|
2卷引用:福建省宁德市2021-2022学年高二上学期期末质量检测化学试题1
名校
3 . 用如图所示的装置进行实验,能达到实验目的是
| A | B | C | D |
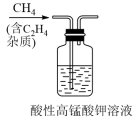 | 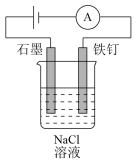 | 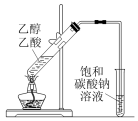 | 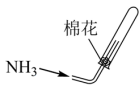 |
| 提纯CH4 | 防止铁钉生锈 | 制备并收集乙酸乙酯 | 收集氨气 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
4 . 关于图中各装置图的叙述正确的是
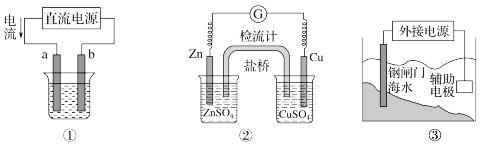

| A.用图①装置电解饱和食盐水制备烧碱、氢气和氯气,a电极可以用铁电极 |
| B.用图①装置在铁钉上镀铜,电解质溶液一定要用铜盐溶液 |
| C.图②装置中,理论上,每转移0.2mol电子,两电极质量差为6.5g |
| D.图③装置中保护钢闸门的辅助电极一定要选金属活动性顺序中排在铁前面的金属 |
您最近一年使用:0次
2021-01-13更新
|
107次组卷
|
2卷引用:福建省厦门市湖滨中学2020-2021学年高二上学期期中考试化学(等级考)试题
名校
解题方法
5 . 下列电化学装置正确且能达到目的的是
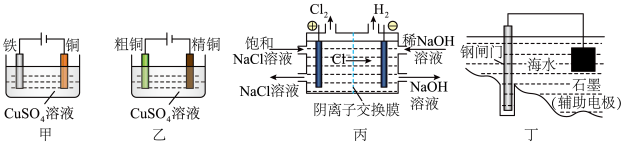

| A.用装置甲在铁制品表面镀铜 | B.用装置乙电解精炼铜 |
| C.用装置丙制备NaOH和氯气 | D.用装置丁保护钢闸门 |
您最近一年使用:0次
2020-07-21更新
|
561次组卷
|
10卷引用:福建省仙游一中、莆田二中、莆田四中2020-2021学年高二上学期期末联考化学试题
福建省仙游一中、莆田二中、莆田四中2020-2021学年高二上学期期末联考化学试题江苏省苏州市2019-2020学年高二下学期学业质量阳光指标调研化学试题江苏省苏州市2019-2020学年高二下学期期末考试化学试题江苏省扬州市扬州中学2021届高三开学检测化学试题江苏省苏州外国语中学2020-2021学年高二下学期3月月考化学试题江苏省镇江中学2020-2021学年高二上学期期末考试化学试题河南省南阳市2022届高三上学期期中考试化学试题江苏省昆山中学2022-2023学年高一下学期5月月考化学试题江苏省苏州市苏州大学附属中学2023-2024学年高二上学期10月月考化学试题18 2024年苏州高新区吴县高级中学高二3月月考
名校
6 . Ⅰ.铁、铝及其化合物在生产和生活中有着广泛的应用。
(1)某研究性学习小组设计了如图所示装置探究钢铁的腐蚀与防护。
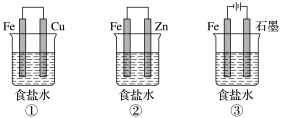
为防止金属Fe被腐蚀,可以采用上述________ (填装置序号)装置原理进行防护;装置③中总反应的离子方程式为_________________ 。
(2)为处理银器表面的黑斑(Ag2S),将银器浸于铝质容器里的食盐水中并与铝接触,Ag2S转化为Ag,食盐水的作用为_______________________ 。
Ⅱ.纳米级Cu2O由于具有优良的催化性能而受到关注,采用肼(N2H4)燃料电池为电源,用离子交换膜控制电解液中c(OH-)制备纳米Cu2O,其装置如图甲、乙。
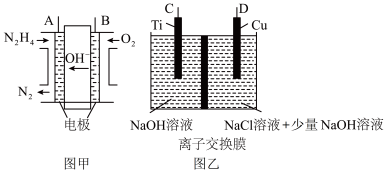
(1)上述装置中D电极应连接肼燃料电池的________ 极(填“A”或“B”),该电解池中离子交换膜为________ 离子交换膜(填“阴”或“阳”)。
(2)该电解池的阳极反应式为____________________ 。
(3)当反应生成14.4 g Cu2O时,至少需要肼________ mol。
(1)某研究性学习小组设计了如图所示装置探究钢铁的腐蚀与防护。

为防止金属Fe被腐蚀,可以采用上述
(2)为处理银器表面的黑斑(Ag2S),将银器浸于铝质容器里的食盐水中并与铝接触,Ag2S转化为Ag,食盐水的作用为
Ⅱ.纳米级Cu2O由于具有优良的催化性能而受到关注,采用肼(N2H4)燃料电池为电源,用离子交换膜控制电解液中c(OH-)制备纳米Cu2O,其装置如图甲、乙。

(1)上述装置中D电极应连接肼燃料电池的
(2)该电解池的阳极反应式为
(3)当反应生成14.4 g Cu2O时,至少需要肼
您最近一年使用:0次



