10-11高二下·山东德州·期中
1 . 金属的防腐常用方法有A.覆盖油漆 B. 覆盖塑料 C. 电镀金属 D. 电化学保护法E. 制成不锈钢;请为以下钢铁制品选择一种适当的防止生锈的方法(填写序号):
(1) 邮筒__________________
(2) 手术刀________________
(3) 海水中的钢闸门____________
(4) 电线___________________
(5) 自行车的钢圈___________
(1) 邮筒
(2) 手术刀
(3) 海水中的钢闸门
(4) 电线
(5) 自行车的钢圈
您最近一年使用:0次
11-12高二上·吉林松原·期末
解题方法
2 . I.炒过菜的铁锅未及时洗净,不久便会因腐蚀而出现红褐色锈斑。请回答:
(1)铁锅的锈蚀是_______ 腐蚀(填“析氢”或“吸氧”)。
(2)写出铁锅腐蚀正极的电极反应式:_______
II.美国阿波罗宇宙飞船上使用的氢氧燃料电池是一种新型的化学电源,其构造如图所示:a、b两个极均由多孔性碳制成,通入的气体由孔隙中逸出,并在电极表面放电。

(1)a是_______ 极;电极反应式为_______ 。
(2)已知:2H2(g)+O2(g)=2H2O(l) ΔH=-572kJ/mol,飞船上宇航员的生活用水由燃料电池提供。已知这种电池发1度电(3600KJ)时能生成360g水,则该电池的能量的利用率为_______ 。
(1)铁锅的锈蚀是
(2)写出铁锅腐蚀正极的电极反应式:
II.美国阿波罗宇宙飞船上使用的氢氧燃料电池是一种新型的化学电源,其构造如图所示:a、b两个极均由多孔性碳制成,通入的气体由孔隙中逸出,并在电极表面放电。

(1)a是
(2)已知:2H2(g)+O2(g)=2H2O(l) ΔH=-572kJ/mol,飞船上宇航员的生活用水由燃料电池提供。已知这种电池发1度电(3600KJ)时能生成360g水,则该电池的能量的利用率为
您最近一年使用:0次
3 . 电化学原理在防止金属腐蚀、能量转换、物质合成等方面应用广泛。

(1)图1中,为了减缓海水对钢闸门A的腐蚀,材料B可以选择________ (填字母序号)。
a.碳棒 b.锌板 c.铜板
用电化学原理解释材料B需定期拆换的原因:__________________________ 。
(2)图2中,钢闸门C做_____ 极。用氯化钠溶液模拟海水进行实验,D为石墨块,则D上的电极反应式为______________________ ,检测该电极反应产物的方法是_______________________ 。
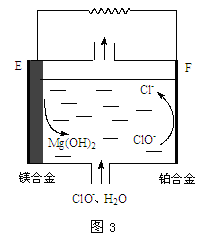
(3)镁燃料电池在可移动电子设备电源和备用电源等方面应用前景广阔。图3为“镁—次氯酸盐”燃料电池原理示意图,电极为镁合金和铂合金。
①E为该燃料电池的极________ (填“正”或“负”)。F电极上的电极反应式为___________ 。
②镁燃料电池负极容易发生自腐蚀产生氢气,使负极利用率降低,用化学用语解释其原因_______ 。

(1)图1中,为了减缓海水对钢闸门A的腐蚀,材料B可以选择
a.碳棒 b.锌板 c.铜板
用电化学原理解释材料B需定期拆换的原因:
(2)图2中,钢闸门C做

(3)镁燃料电池在可移动电子设备电源和备用电源等方面应用前景广阔。图3为“镁—次氯酸盐”燃料电池原理示意图,电极为镁合金和铂合金。
①E为该燃料电池的极
②镁燃料电池负极容易发生自腐蚀产生氢气,使负极利用率降低,用化学用语解释其原因
您最近一年使用:0次
10-11高三下·广东茂名·阶段练习
4 . Ⅰ.维生素C的结构简式是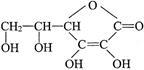 ,它的分子式是
,它的分子式是_______ 。由于它能防治坏血病,又称为_______ 。在维生素C溶液中滴入紫色石蕊试液,溶液颜色变红,说明维生素C溶液具有_______ 性;在维生素C溶液中滴入少量蓝色的含有淀粉的碘水,可观察到的现象是_______ ,说明维生素C具有_______ 性。

Ⅱ.(1)如图所示,铁处于Ⅰ、Ⅱ、Ⅲ三种不同的环境中,铁被腐蚀的速率由大到小的顺序是(填序号)_______ 。
(2)氟氯代烷是一种能破坏臭氧层的物质。在大气平流层中,氟氯代烷受紫外线的照射分解出氯原子,氯原子参与下列有关反应:
①Cl+O3→ClO+O2 ②O3→O+O2 ③ClO+O→Cl+O2
上列的反应的总反应式是_______ ,少量氟氯代烷能破坏大量臭氧的原因是_______ 。
 ,它的分子式是
,它的分子式是
Ⅱ.(1)如图所示,铁处于Ⅰ、Ⅱ、Ⅲ三种不同的环境中,铁被腐蚀的速率由大到小的顺序是(填序号)
(2)氟氯代烷是一种能破坏臭氧层的物质。在大气平流层中,氟氯代烷受紫外线的照射分解出氯原子,氯原子参与下列有关反应:
①Cl+O3→ClO+O2 ②O3→O+O2 ③ClO+O→Cl+O2
上列的反应的总反应式是
您最近一年使用:0次
10-11高三·黑龙江绥化·阶段练习
5 . 钢铁工业是国家工业的基础,请回答:钢铁冶炼、腐蚀与防护过程中的有关问题。
(1)工业用热还原法冶炼生铁的主要原料有_______________________ ,设备的名称是_________________ 写出用还原剂CO还原赤铁矿(主要成分为Fe2O3)的化学方程式_________________ 。
(2)写出钢铁在潮湿空气中发生锈蚀时的正极反应方程式___________________ ,生成铁锈(Fe2O3˙xH2O)的化学方程式为__________________ 。
(3)生铁的用途远远不及钢材广泛,人们把较多的高炉生铁直接冶炼成钢,由生铁直接在纯氧顶吹转炉中转化成钢时,是把有害杂质除掉而保留有益元素,可以概括为______________________________________ 。为了防止钢铁制品发生锈蚀,可以在钢铁零件的表面进行电镀铜等措施,电镀铜时的阳极反应为_______________________ 。
(1)工业用热还原法冶炼生铁的主要原料有
(2)写出钢铁在潮湿空气中发生锈蚀时的正极反应方程式
(3)生铁的用途远远不及钢材广泛,人们把较多的高炉生铁直接冶炼成钢,由生铁直接在纯氧顶吹转炉中转化成钢时,是把有害杂质除掉而保留有益元素,可以概括为
您最近一年使用:0次
10-11高二上·甘肃天水·阶段练习
解题方法
6 . 在原电池中,较活泼的金属发生_______ 反应,是______ 极;活动性较差的金属极上发生_______ 反应,是______ 极。潮湿空气中钢铁表面容易发生腐蚀,发生腐蚀时,铁是______ 极,电极反应式为_____ ;杂质碳是____ 极,电极反应式为_________ 。
您最近一年使用:0次
7 . 对金属制品进行抗腐蚀处理,可延长其使用寿命。
(1)利用如图装置,可以模拟铁的电化学防护。

若X为碳棒,为减缓铁的腐蚀,开关K应置于________ 处。若X为锌,开关K置于M处,该电化学防护法称为__________________ 。
(2)以下为铝材表面处理的一种方法:
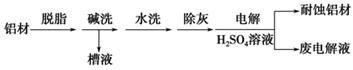
①碱洗的目的是除去铝材表面的自然氧化膜,碱洗时常有气泡冒出,原因是_________________ (用离子方程式表示)。为将碱洗槽液中的铝以沉淀形式回收,最好向槽液中加入下列试剂中的________ 。
a.NH3 b.CO2 c.NaOH d.HNO3
②以铝材为阳极,在H2SO4溶液中电解,铝材表面形成氧化膜,阳极电极反应式为_________________ 。
取少量废电解液,加入NaHCO3溶液后产生气泡和白色沉淀,产生沉淀的原因是____________________ 。
(3)镀铜可防止铁制品腐蚀,电镀时阳极材料为________________ ,用铜而不用石墨作阳极的原因是______________________ 。
(1)利用如图装置,可以模拟铁的电化学防护。

若X为碳棒,为减缓铁的腐蚀,开关K应置于
(2)以下为铝材表面处理的一种方法:

①碱洗的目的是除去铝材表面的自然氧化膜,碱洗时常有气泡冒出,原因是
a.NH3 b.CO2 c.NaOH d.HNO3
②以铝材为阳极,在H2SO4溶液中电解,铝材表面形成氧化膜,阳极电极反应式为
取少量废电解液,加入NaHCO3溶液后产生气泡和白色沉淀,产生沉淀的原因是
(3)镀铜可防止铁制品腐蚀,电镀时阳极材料为
您最近一年使用:0次
8 . 家用炒菜铁锅用水清洗放置后,便会因腐蚀而出现红棕色的锈斑,铁锅发生腐蚀应属于_____ 腐蚀,负极反应式为____________ ,正极反应式为________ ,
您最近一年使用:0次
10-11高二上·福建福州·期中
解题方法
9 . 钢铁工业是国家工业的基础。请回答钢铁冶炼、腐蚀、防护过程中的有关问题。
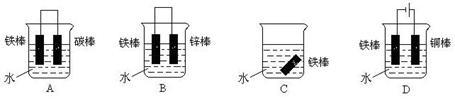
(1)下列哪个装置可防止铁棒被腐蚀_____________ 。
(2)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀。装置示意图如右:
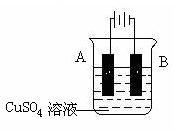
请回答:
①A电极对应的金属是______ (写元素名称),B电极的电极反应式是____________ 。
②若电镀前铁、铜两电极的质量相同,电镀完成后将它们取出洗净、烘干、称量,二者质量差为51.2 g,则电镀时电路中通过的电子物质的量为_______ 。
(1)下列哪个装置可防止铁棒被腐蚀

(2)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀。装置示意图如右:

请回答:
①A电极对应的金属是
②若电镀前铁、铜两电极的质量相同,电镀完成后将它们取出洗净、烘干、称量,二者质量差为51.2 g,则电镀时电路中通过的电子物质的量为
您最近一年使用:0次
10 . 对金属制品进行防腐蚀处理,可延长其使用寿命。
(1)以下为铝材表面处理的一种方法:
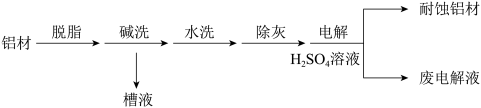
①碱洗的目的是除去铝材表面的自然氧化膜,碱洗时候常有气泡冒出,原因是:________ (用离子方程式表示)。为将碱洗槽液中的铝以沉淀形式回收,最好向槽液中加入下列试剂中的__________ 。
a.NH3b.CO2c.NaOH d.HNO3
②以铝材为阳极,在H2SO4溶液中电解,铝村表面形成氧化膜,阳极电极反应式为:_____ 。
取少量废电解液,加入NaHCO3溶液后产生气泡和白色沉淀,产生沉淀的原因是_________ 。
(2)镀铜可防止铁制品腐蚀,电镀时用铜而不用石墨做阳极的原因是___________ 。
(3)利用下图装置,可以模拟铁的电化学防护。
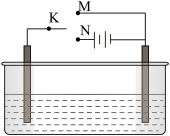
若X为碳棒,为减缓铁的腐蚀,开关K应该置于_______________ 处。
若X为锌,开关K置于M处,该电化学防护法称为_______________ 。
(1)以下为铝材表面处理的一种方法:

①碱洗的目的是除去铝材表面的自然氧化膜,碱洗时候常有气泡冒出,原因是:
a.NH3b.CO2c.NaOH d.HNO3
②以铝材为阳极,在H2SO4溶液中电解,铝村表面形成氧化膜,阳极电极反应式为:
取少量废电解液,加入NaHCO3溶液后产生气泡和白色沉淀,产生沉淀的原因是
(2)镀铜可防止铁制品腐蚀,电镀时用铜而不用石墨做阳极的原因是
(3)利用下图装置,可以模拟铁的电化学防护。

若X为碳棒,为减缓铁的腐蚀,开关K应该置于
若X为锌,开关K置于M处,该电化学防护法称为
您最近一年使用:0次
2016-12-09更新
|
578次组卷
|
13卷引用:2010年普通高等学校招生全国统一考试理综化学部分(山东卷)
2010年普通高等学校招生全国统一考试理综化学部分(山东卷)2010年高考化学试题分项专题九 电化学(已下线)2010年湖北省孝感高中高二上学期期中考试化学试卷(已下线)2011届广东省高三全真高考模拟试卷(二)(理综)化学部分(已下线)2013-2014学年湖北省部分重点中学高二上学期期末考试化学试卷2015-2016学年四川省新津中学高二4月月考化学试卷黑龙江省哈尔滨市第六中学2017-2018学年高二3月月考化学试题云南省文山壮族苗族自治州马关县第一中学2020届高三上学期9月份考试化学试题云南省文山州砚山县一中2020届高三上学期开学考试化学试题云南省双柏县一中2020届高三上学期开学考试化学试题云南省大理白族自治州宾川县第三完全中学2019-2020学年高二上学期开学考试化学试题贵州省台江县第二中学2019-2020学年高三上学期期末考试化学试题云南省玉溪师范学院附属中学2021-2022学年高三 上学期期末考试化学试题



