1 . 完成下列问题。
(1)一种甲醇燃料电池是采用铂或碳化钨作为电极催化剂,在稀硫酸中直接加入纯化后的甲醇(CH3OH),同时向一个电极通入空气。
①此电池的正极发生的电极反应为_______ 。
②电解液中H+向_____ 极移动。
(2)如图所示,该装置通电5 min后,电极5的质量增加2.16 g,回答下列问题:____ 极,A池阴极电极反应:______ ,C池阳极电极反应:_______ 。
②如果B槽中共收集到224 mL气体(标准状况)且溶液体积为200 mL(设电解过程中溶液体积不变),则通电前溶液中Cu2+的物质的量浓度为______ 。
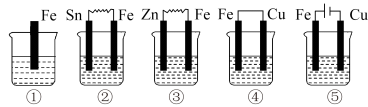
(3)下图各烧杯中盛有海水,铁在其中被腐蚀,腐蚀的速率由大到小的顺序为_____ 。______ 。
(1)一种甲醇燃料电池是采用铂或碳化钨作为电极催化剂,在稀硫酸中直接加入纯化后的甲醇(CH3OH),同时向一个电极通入空气。
①此电池的正极发生的电极反应为
②电解液中H+向
(2)如图所示,该装置通电5 min后,电极5的质量增加2.16 g,回答下列问题:
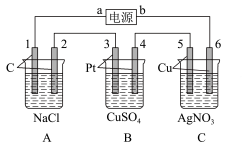
②如果B槽中共收集到224 mL气体(标准状况)且溶液体积为200 mL(设电解过程中溶液体积不变),则通电前溶液中Cu2+的物质的量浓度为
(3)下图各烧杯中盛有海水,铁在其中被腐蚀,腐蚀的速率由大到小的顺序为
您最近一年使用:0次
名校
解题方法
2 . 金属阳极钝化是一种电化学防护方法。将Fe 作阳极置于一定浓度的H2SO4 溶液中,一定条件下,Fe钝化形成致密Fe3O4氧化膜,试写出该过程中阳极的电极反应_______ 。
您最近一年使用:0次
名校
解题方法
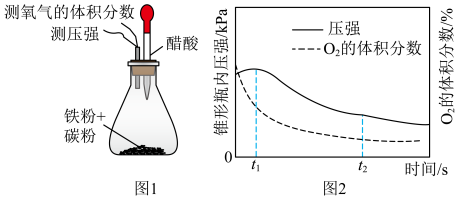
3 . 按图1进行实验,测得锥形瓶内气压和空气中氧气的体积分数随时间变化如图2所示。t1~t2之间主要发生_______ (填“吸氧”或“析氢”)腐蚀,其正极反应式为_______ 。
您最近一年使用:0次
名校
4 . 恒温条件下,用图1所示装置研究铁的电化学腐蚀,测定结果如图2。 段主要发生
段主要发生___________ 腐蚀, 段负极反应式为
段负极反应式为___________ 。
 段主要发生
段主要发生 段负极反应式为
段负极反应式为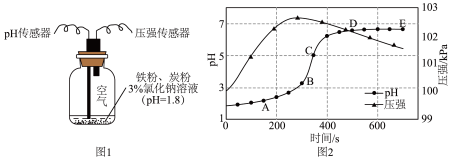
您最近一年使用:0次
5 . 钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢材占世界钢铁年产量的四分之一。
(1)钢铁腐蚀主要是吸氧腐蚀,该腐蚀过程中的电极反应式为:正极_________ , 负极_________ 。
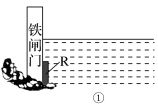
(2)为了降低某水库的铁闸门被腐蚀的速率,可以采用如图所示的方案,其中焊接在闸门上的固体材料R可以采用_________。
(3)如图所示的方案也可以降低铁闸门的腐蚀速率,其中铁闸门应该连接在直流电源的_________ 极。
①若溶液的pH=7,则该溶液中c( )
)_________ c(Cl-)。
②若溶液的pH>7,则该溶液中c( )
)_________ c(Cl-)。
③若c( )<c (Cl-),则溶液的pH
)<c (Cl-),则溶液的pH_________ 7。
(1)钢铁腐蚀主要是吸氧腐蚀,该腐蚀过程中的电极反应式为:正极
(2)为了降低某水库的铁闸门被腐蚀的速率,可以采用如图所示的方案,其中焊接在闸门上的固体材料R可以采用_________。
| A.铜 | B.钠 | C.锌 | D.石墨 |
(3)如图所示的方案也可以降低铁闸门的腐蚀速率,其中铁闸门应该连接在直流电源的

①若溶液的pH=7,则该溶液中c(
 )
)②若溶液的pH>7,则该溶液中c(
 )
)③若c(
 )<c (Cl-),则溶液的pH
)<c (Cl-),则溶液的pH
您最近一年使用:0次
解题方法
6 . 如图所示,甲、乙两池电极材料都是铁棒和碳棒,请回答下列问题: 溶液,则反应一段时间后:
溶液,则反应一段时间后:
①乙池中阳极的电极反应式是_______ 。
②若要保护金属铁,可将甲池中的C棒换成 棒,则该防护方法称为
棒,则该防护方法称为_______ 。
(2)若两池中电解质溶液均为饱和 溶液:
溶液:
①写出乙池中总反应的离子方程式_______ 。
②甲池中碳极上电极反应式是_______ 。
③若乙池转移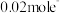 后停止实验,池中电解质溶液体积是
后停止实验,池中电解质溶液体积是 ,则室温下溶液混合均匀后的
,则室温下溶液混合均匀后的
_______ 。

 溶液,则反应一段时间后:
溶液,则反应一段时间后:①乙池中阳极的电极反应式是
②若要保护金属铁,可将甲池中的C棒换成
 棒,则该防护方法称为
棒,则该防护方法称为(2)若两池中电解质溶液均为饱和
 溶液:
溶液:①写出乙池中总反应的离子方程式
②甲池中碳极上电极反应式是
③若乙池转移
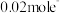 后停止实验,池中电解质溶液体积是
后停止实验,池中电解质溶液体积是 ,则室温下溶液混合均匀后的
,则室温下溶液混合均匀后的
您最近一年使用:0次
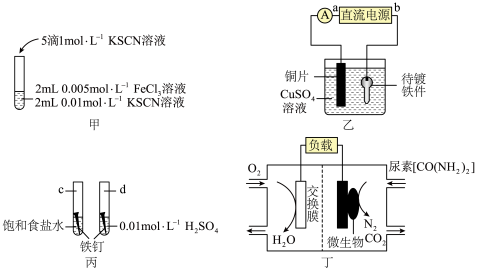
7 . 根据下列装置图,回答有关问题:___________ ,该反应为可逆反应,其离子方程式为___________ 。
(2)装置乙中,直流电源a为___________ 极(填“正”或“负”),阳极反应式为___________ 。
(3)装置丙中,d试管内铁钉除发生化学腐蚀外,还发生了___________ (填“析氢腐蚀”或“吸氧腐蚀”),其腐蚀速率比c试管中铁钉的腐蚀速率___________ (“快”“慢”或“相等”),c试管内正极的电极反应式为___________ 。
(4)装置丁中,从交换膜右侧向左侧迁移的离子是___________ ,负极的电极反应式为___________ 。
(2)装置乙中,直流电源a为
(3)装置丙中,d试管内铁钉除发生化学腐蚀外,还发生了
(4)装置丁中,从交换膜右侧向左侧迁移的离子是
您最近一年使用:0次
8 . I.Ti、Na、Mg、C、N、O、Fe等元素单质及化合物在诸多领域都有广泛的应用。回答下列问题:
(1)已知C、CO的燃烧热分别为393.5kJ/mol和283.0kJ/mol,写出碳不完全燃烧生成CO的热化学方程式___________ 。
(2)Na、Mg、C、N、O的第一电离能由大到小的顺序为___________ 。
(3)基态 原子最高能层的原子轨道形状为
原子最高能层的原子轨道形状为___________ ,其价电子轨道表示式为___________ 。
(4)钢铁发生吸氧腐蚀时正极的电极反应式为:___________ 。为防止钢铁输水管的腐蚀,可用导线将其与镁块连接,这种防护方法为___________ 。(电化学保护法中的一种)
(5)用琥珀酸亚铁片是用于缺铁性贫血的预防和治疗的常见药物,临床建议服用维生素C促进“亚铁”的吸收,避免生成 ,从结构角度来看,
,从结构角度来看, 易被氧化成
易被氧化成 的原因是
的原因是___________ 。
II.制备硫酸四氨合铜晶体
①取20mL配制好的硫酸铜溶液于试管中,向其中滴加1mol/L氨水,有蓝色沉淀生成。
②继续慢慢加入氨水并振荡试管,沉淀逐渐消失,生成深蓝色溶液。
(6) 中,形成配位键提供孤电子对的原子是
中,形成配位键提供孤电子对的原子是___________ (填元素符号),1mol该微粒中,含有σ键的数目为___________  (设
(设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
(7)步骤②中蓝色沉淀溶解的离子方程式为___________ 。
(8)步骤③中加入无水乙醇的目的是___________ 。
(1)已知C、CO的燃烧热分别为393.5kJ/mol和283.0kJ/mol,写出碳不完全燃烧生成CO的热化学方程式
(2)Na、Mg、C、N、O的第一电离能由大到小的顺序为
(3)基态
 原子最高能层的原子轨道形状为
原子最高能层的原子轨道形状为(4)钢铁发生吸氧腐蚀时正极的电极反应式为:
(5)用琥珀酸亚铁片是用于缺铁性贫血的预防和治疗的常见药物,临床建议服用维生素C促进“亚铁”的吸收,避免生成
 ,从结构角度来看,
,从结构角度来看, 易被氧化成
易被氧化成 的原因是
的原因是II.制备硫酸四氨合铜晶体
①取20mL配制好的硫酸铜溶液于试管中,向其中滴加1mol/L氨水,有蓝色沉淀生成。
②继续慢慢加入氨水并振荡试管,沉淀逐渐消失,生成深蓝色溶液。
③再向试管中加入15mL无水乙醇,混合后静置30分钟,有深蓝色晶体析出
(6)
 中,形成配位键提供孤电子对的原子是
中,形成配位键提供孤电子对的原子是 (设
(设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。(7)步骤②中蓝色沉淀溶解的离子方程式为
(8)步骤③中加入无水乙醇的目的是
您最近一年使用:0次
9 . 请按要求回答下列问题。
(1)25℃,pH=1的CH3COOH溶液中由水电离出的H+浓度约为_______ mol•L-1。
(2)如图烧杯中盛的是海水,铁腐蚀的速率最慢的是_______ (填标号)。
(3)用如图所示的装置研究电化学的相关问题(乙装置中X为阳离子交换膜)。
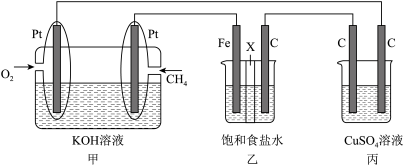
①甲装置中负极反应式为_______ 。
②乙装置中石墨电极上生成的气体为_______ (填化学式)。
③丙装置中CuSO4足量,工作一段时间后,溶液的pH_______ (填“变大”、“变小”或“不变”),反应的化学方程式为_______ ,若要将电解后的溶液复原,需加入一定量的_______ (填化学式)。
(1)25℃,pH=1的CH3COOH溶液中由水电离出的H+浓度约为
(2)如图烧杯中盛的是海水,铁腐蚀的速率最慢的是
A.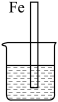 | B. | C.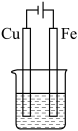 | D. |
(3)用如图所示的装置研究电化学的相关问题(乙装置中X为阳离子交换膜)。

①甲装置中负极反应式为
②乙装置中石墨电极上生成的气体为
③丙装置中CuSO4足量,工作一段时间后,溶液的pH
您最近一年使用:0次
10 . 铁、铜等金属在生产和生活中有着广泛的应用。回答下列问题:
(1)某研究性学习小组设计了如下图所示装置探究钢铁的腐蚀与防护,烧杯内液体均为饱和食盐水。
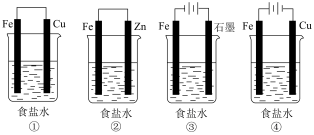
在相同条件下,四组装置中铁电极腐蚀最快的是___________ (填序号,下同);为防止金属被腐蚀,可以采用上述___________ 装置原理进行防护。
(2)钴酸锂电池是目前常见的锂离子二次电池,电池总反应为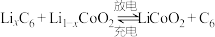 ,用它做电源按如图装置进行电解,通电后,d电极附近先出现白色沉淀(CuCl)。
,用它做电源按如图装置进行电解,通电后,d电极附近先出现白色沉淀(CuCl)。
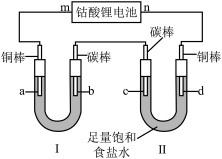
①放电时,负极反应式为___________ 。
②该电池充电时,n极接电源的___________ 极,试写出装置Ⅱ中d电极附近产生白色沉淀的反应式___________ 。
③电极a上的现象是___________ 。
④若装置I为铜上镀银,则装置I中U形管内的溶液为___________ (填化学式,下同),电解一段时间后,若铜棒上无气体产生,要使溶液恢复原状态,需加入___________ 。
(1)某研究性学习小组设计了如下图所示装置探究钢铁的腐蚀与防护,烧杯内液体均为饱和食盐水。

在相同条件下,四组装置中铁电极腐蚀最快的是
(2)钴酸锂电池是目前常见的锂离子二次电池,电池总反应为
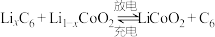 ,用它做电源按如图装置进行电解,通电后,d电极附近先出现白色沉淀(CuCl)。
,用它做电源按如图装置进行电解,通电后,d电极附近先出现白色沉淀(CuCl)。
①放电时,负极反应式为
②该电池充电时,n极接电源的
③电极a上的现象是
④若装置I为铜上镀银,则装置I中U形管内的溶液为
您最近一年使用:0次



