解题方法
1 . “对比实验”是科学探究中的重要方法。请根据图回答下列问题:

(1)图甲铜片上白磷燃烧而水中白磷不燃烧,说明燃烧条件之一是________ 。
(2)图乙A中溶液呈紫红色,B中溶液无色,说明A中溶液呈紫红色的原因是________ 含有(填离子符号或名称)。
(3)图丙中铁钉最容易生锈的是________ (填序号)。自行车链条防锈措施是________ (任填一条)。

(1)图甲铜片上白磷燃烧而水中白磷不燃烧,说明燃烧条件之一是
(2)图乙A中溶液呈紫红色,B中溶液无色,说明A中溶液呈紫红色的原因是
(3)图丙中铁钉最容易生锈的是
您最近半年使用:0次
2 . 金属电化学防护的方法有哪些?哪一个效果更好_______ 。
您最近半年使用:0次
3 . 铁的腐蚀以哪种类型为主_______ 。
您最近半年使用:0次
解题方法
4 . 生铁在干燥的空气中不易被腐蚀,但在潮湿的空气中却很快被腐蚀,为什么?为什么生铁比纯铁更易被腐蚀_______ 。
您最近半年使用:0次
名校
解题方法
5 . 某博物馆修复出土铁器的过程如下:
检测锈蚀产物
(1)铁器在潮湿的空气里容易发生_____腐蚀; 中铁元素的化合价为_____。
中铁元素的化合价为_____。
(2)不锈钢中一般加入铬元素,Cr元素基态原子的简化核外电子排布式_____ 。
分析腐蚀原理:一般认为,铁经过了如下腐蚀循环。
Fe转化为 。
。
(3) 和
和 反应形成致密的
反应形成致密的 保护层,
保护层, 的作用是
的作用是_____ (填字母)。
A.氧化剂 B.还原剂 C.既不是氧化剂也不是还原剂
(4)工业上冶炼Fe常用的方法是_____(填字母)。
(5)不同价态铁离子在水溶液中转化的离子反应有: ,为了探究该反应存在一定的限度,某化学兴趣小组取
,为了探究该反应存在一定的限度,某化学兴趣小组取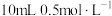 的KI溶液于试管中,再加入
的KI溶液于试管中,再加入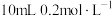 的
的 溶液,振荡,使试管中的物质充分反应一段时间。为了达到实验目的,还需要再向试管中加入下列试剂中的_____(填字母)。
溶液,振荡,使试管中的物质充分反应一段时间。为了达到实验目的,还需要再向试管中加入下列试剂中的_____(填字母)。
检测锈蚀产物
| 主要成分的化学式 | |||
 | 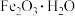 |  |  |
 中铁元素的化合价为_____。
中铁元素的化合价为_____。| A.化学 | B.电化学 | C. | D. |
分析腐蚀原理:一般认为,铁经过了如下腐蚀循环。
Fe转化为
 。
。(3)
 和
和 反应形成致密的
反应形成致密的 保护层,
保护层, 的作用是
的作用是A.氧化剂 B.还原剂 C.既不是氧化剂也不是还原剂
(4)工业上冶炼Fe常用的方法是_____(填字母)。
| A.电解法 | B.还原法 | C.热分解法 | D.物理方法 |
 ,为了探究该反应存在一定的限度,某化学兴趣小组取
,为了探究该反应存在一定的限度,某化学兴趣小组取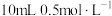 的KI溶液于试管中,再加入
的KI溶液于试管中,再加入 的
的 溶液,振荡,使试管中的物质充分反应一段时间。为了达到实验目的,还需要再向试管中加入下列试剂中的_____(填字母)。
溶液,振荡,使试管中的物质充分反应一段时间。为了达到实验目的,还需要再向试管中加入下列试剂中的_____(填字母)。| A.淀粉溶液 | B.KSCN溶液 | C. | D.酸性高锰酸钾溶液 |
您最近半年使用:0次
名校
解题方法
6 . 用如图所示装置研究铁的防腐蚀过程:
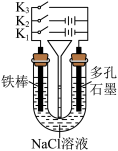
(1)K1、K2、K3只关闭一个,则铁腐蚀的速度最快的是只闭合_______ (选填“K1”、“K2”或“K3”,下同)。
(2)为减缓铁的腐蚀,应只闭合_______ ,该防护法称为_______ 。
(3)只闭合K3,石墨电极附近的pH将_______ (选填“变大”、“变小”或“不变”)。

(1)K1、K2、K3只关闭一个,则铁腐蚀的速度最快的是只闭合
(2)为减缓铁的腐蚀,应只闭合
(3)只闭合K3,石墨电极附近的pH将
您最近半年使用:0次
2023-09-18更新
|
100次组卷
|
2卷引用:上海市青浦高级中学2023-2024学年高三上学期9月测质量检测化学试题
名校
7 . 研究金属的腐蚀过程及防腐蚀对人们的日常生活有重大意义。
(1)如图中的铁棒若为纯铁,则其腐蚀过程属于_______ 腐蚀(选填“化学”或“电化学”)。
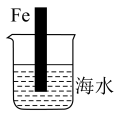
(2)若铁棒的含碳量为10.8%,浸入一段时间之后发现,越靠近烧杯底部发生电化学腐蚀就越轻微,该实验说明_______ 因素会影响铁的腐蚀速率;腐蚀时,正极的电极反应式为_______ 。(已知:海水pH约为8.1)
(1)如图中的铁棒若为纯铁,则其腐蚀过程属于

(2)若铁棒的含碳量为10.8%,浸入一段时间之后发现,越靠近烧杯底部发生电化学腐蚀就越轻微,该实验说明
您最近半年使用:0次
名校
解题方法
8 . 1.某课外小组同学对不同条件下铁钉的锈蚀进行了如图实验:
(1)一周后观察,铁钉被腐蚀程度最大的是___________ (填实验序号)。
(2)实验③中主要发生的是___________ (填“化学腐蚀”或“电化学腐蚀”)。
(3)铁发生电化学腐蚀的负极反应式为___________ 。
(4)钢铁表面常电镀一层铬(Cr)达到防腐蚀的目的,这是由于铬具有优良的抗腐蚀性能。电镀时,把待镀的金属制品与直流电源的___________ 极(填“正”或“负”)相连,把镀层金属铬作___________ 极(填“阳”或“阴”)。
(5)利用如图装置,可以模拟铁的电化学保护。
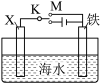
若X为碳棒,为减缓铁的腐蚀,开关K应置于N处,该电化学保护法称为___________ 若X为锌,开关K置于M处,铁棒上发生的电极反应式___________
| 实验序号 | ① | ② | ③ | ④ |
| 实验内容 | 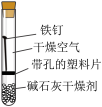 |  |  | 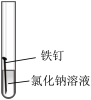 |
(1)一周后观察,铁钉被腐蚀程度最大的是
(2)实验③中主要发生的是
(3)铁发生电化学腐蚀的负极反应式为
(4)钢铁表面常电镀一层铬(Cr)达到防腐蚀的目的,这是由于铬具有优良的抗腐蚀性能。电镀时,把待镀的金属制品与直流电源的
(5)利用如图装置,可以模拟铁的电化学保护。

若X为碳棒,为减缓铁的腐蚀,开关K应置于N处,该电化学保护法称为
您最近半年使用:0次
9 . 电化学理论在钢铁防腐、废水处理中有着重要应用价值。请按要求回答下列问题
(1)下图为探究金属 是否腐蚀的示意图
是否腐蚀的示意图
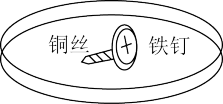
在培养皿中加入一定量的琼脂和饱和 溶液混合,滴入5~6滴酚酞溶液,混合均匀,将缠有铜丝的铁钉放入培养皿中。溶液变红的部位为
溶液混合,滴入5~6滴酚酞溶液,混合均匀,将缠有铜丝的铁钉放入培养皿中。溶液变红的部位为___________ (填“左”或“右”)端,结合化学用语解释变红的原因:___________ 。
(2)碳钢在空气中容易被腐蚀,加入钼酸盐有利于缓蚀,其缓蚀原理是在钢铁表面形成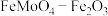 保护膜。要对密闭式循环冷却水系统中的碳钢管道缓蚀,除需加入铝酸盐外还需加入
保护膜。要对密闭式循环冷却水系统中的碳钢管道缓蚀,除需加入铝酸盐外还需加入 ,则
,则 的作用是
的作用是___________ 。
(3)支撑海港码头基础的钢管桩,常采用如图所示的方法进行防腐,其中高硅铸铁为惰性辅助阳极。

①该保护方法叫作___________ (填“牺牲阳极法”或“外加电流法”)。
②下列有关表述正确的是___________ (填字母)。
a.钢管桩被迫成为阴极而受到保护,其表面的腐蚀电流接近于零
b.高硅铸铁的作用是作为损耗阳极材料和传递电流
c.通电后,调整外加电压,外电路中的电子被强制从钢管桩流向高硅铸铁
d.石墨能导电且化学性质不活泼,可用石墨代替高硅铸铁作辅助阳极
(4)利用烧结的铁碳混合材料可除去废水中的污染物,在有、无溶解氧的情况下均可在溶液中生成絮凝剂,实现高效工作,其作用原理图示如下:

铁电极的电极反应为___________ 。
下列叙述正确的是___________ (填字母)。
A.铁电极为正极,碳电极为负极
B.经过加热烧结的铁碳混合物表面空隙发达,吸附能力大幅提高,有利于除污
C.碳电极上的反应环境为无溶解氧环境
D.铁碳混合材料工作过程中电子从铁电极流出,被絮凝剂运输至碳电极表面
(1)下图为探究金属
 是否腐蚀的示意图
是否腐蚀的示意图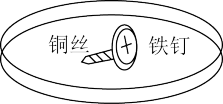
在培养皿中加入一定量的琼脂和饱和
 溶液混合,滴入5~6滴酚酞溶液,混合均匀,将缠有铜丝的铁钉放入培养皿中。溶液变红的部位为
溶液混合,滴入5~6滴酚酞溶液,混合均匀,将缠有铜丝的铁钉放入培养皿中。溶液变红的部位为(2)碳钢在空气中容易被腐蚀,加入钼酸盐有利于缓蚀,其缓蚀原理是在钢铁表面形成
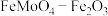 保护膜。要对密闭式循环冷却水系统中的碳钢管道缓蚀,除需加入铝酸盐外还需加入
保护膜。要对密闭式循环冷却水系统中的碳钢管道缓蚀,除需加入铝酸盐外还需加入 ,则
,则 的作用是
的作用是(3)支撑海港码头基础的钢管桩,常采用如图所示的方法进行防腐,其中高硅铸铁为惰性辅助阳极。

①该保护方法叫作
②下列有关表述正确的是
a.钢管桩被迫成为阴极而受到保护,其表面的腐蚀电流接近于零
b.高硅铸铁的作用是作为损耗阳极材料和传递电流
c.通电后,调整外加电压,外电路中的电子被强制从钢管桩流向高硅铸铁
d.石墨能导电且化学性质不活泼,可用石墨代替高硅铸铁作辅助阳极
(4)利用烧结的铁碳混合材料可除去废水中的污染物,在有、无溶解氧的情况下均可在溶液中生成絮凝剂,实现高效工作,其作用原理图示如下:

铁电极的电极反应为
下列叙述正确的是
A.铁电极为正极,碳电极为负极
B.经过加热烧结的铁碳混合物表面空隙发达,吸附能力大幅提高,有利于除污
C.碳电极上的反应环境为无溶解氧环境
D.铁碳混合材料工作过程中电子从铁电极流出,被絮凝剂运输至碳电极表面
您最近半年使用:0次
10 . 研究能量的转化与利用具有重要的现实意义。
(1)依据下列金属腐蚀的有关示意图回答问题。
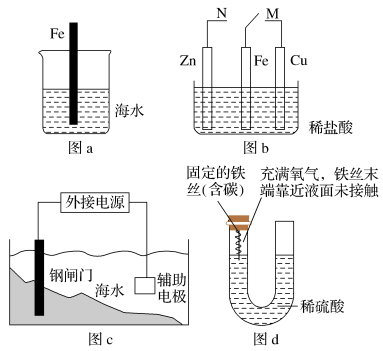
①图a插入海水中的铁棒(含碳量为10.8%)越靠近烧杯底部发生电化学腐蚀就越______________ (填“轻微”或“严重”)。
②图b铁棒上的接触导线由N改置于M时,铁的腐蚀速率________________ (填“减小”或“增大”)。
③图c为牺牲阳极的阴极保护法,钢闸门应与外接电源的________________ 极相连。
④图d在反应过程中U形管内左侧液面的变化是:____________________ 。
(2)应用电化学原理回答下列问题。

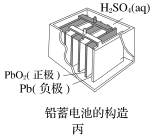
①上述三个装置中,负极反应物在化学性质上的共同特点是:________ 。
②甲中电流计指针偏移时,含KCl的盐桥中Cl-离子移向电极所在的溶液是:________ 。
③乙中电池工作时,负极区KOH溶液的浓度将逐渐________ 。
④丙放电一段时间后进行充电,充电时该电池发生反应的化学方程式为______ 。
(3)铁及其化合物在处理工业废水、废气过程中发挥着重要作用。
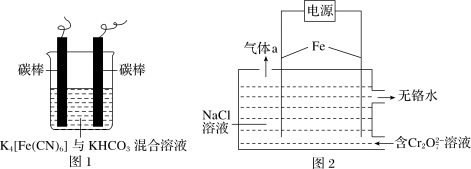
①工业上用铁的化合物除硫化氢:2[Fe(CN)6]3-+CO +HS-=2[Fe(CN)6]4-+HCO
+HS-=2[Fe(CN)6]4-+HCO +S↓,可通过图1使[Fe(CN)6]3-再生。电解时,阳极的电极反应式为
+S↓,可通过图1使[Fe(CN)6]3-再生。电解时,阳极的电极反应式为_______________ ;电解过程中阴极区溶液的pH________ (填“变大” “变小”或“不变”)。
②图2以铁作电极电解除铬。已知转化反应:Cr2O +H2O
+H2O 2CrO
2CrO +2H+,电解过程中主要反应之一:Cr2O
+2H+,电解过程中主要反应之一:Cr2O +6Fe2++17H2O=2Cr(OH)3↓+6Fe(OH)3↓+10H+;图中气体a的主要成分是
+6Fe2++17H2O=2Cr(OH)3↓+6Fe(OH)3↓+10H+;图中气体a的主要成分是________________ 。
(1)依据下列金属腐蚀的有关示意图回答问题。

①图a插入海水中的铁棒(含碳量为10.8%)越靠近烧杯底部发生电化学腐蚀就越
②图b铁棒上的接触导线由N改置于M时,铁的腐蚀速率
③图c为牺牲阳极的阴极保护法,钢闸门应与外接电源的
④图d在反应过程中U形管内左侧液面的变化是:
(2)应用电化学原理回答下列问题。


①上述三个装置中,负极反应物在化学性质上的共同特点是:
②甲中电流计指针偏移时,含KCl的盐桥中Cl-离子移向电极所在的溶液是:
③乙中电池工作时,负极区KOH溶液的浓度将逐渐
④丙放电一段时间后进行充电,充电时该电池发生反应的化学方程式为
(3)铁及其化合物在处理工业废水、废气过程中发挥着重要作用。

①工业上用铁的化合物除硫化氢:2[Fe(CN)6]3-+CO
 +HS-=2[Fe(CN)6]4-+HCO
+HS-=2[Fe(CN)6]4-+HCO +S↓,可通过图1使[Fe(CN)6]3-再生。电解时,阳极的电极反应式为
+S↓,可通过图1使[Fe(CN)6]3-再生。电解时,阳极的电极反应式为②图2以铁作电极电解除铬。已知转化反应:Cr2O
 +H2O
+H2O 2CrO
2CrO +2H+,电解过程中主要反应之一:Cr2O
+2H+,电解过程中主要反应之一:Cr2O +6Fe2++17H2O=2Cr(OH)3↓+6Fe(OH)3↓+10H+;图中气体a的主要成分是
+6Fe2++17H2O=2Cr(OH)3↓+6Fe(OH)3↓+10H+;图中气体a的主要成分是
您最近半年使用:0次



