1 . 回答下列问题:
(1)图中甲装置为 碱性燃料电池,其电极均为
碱性燃料电池,其电极均为 电极,装置乙中,C、D电极为
电极,装置乙中,C、D电极为 电极,其表面均覆盖着
电极,其表面均覆盖着 ,其电解液为稀
,其电解液为稀 溶液。
溶液。
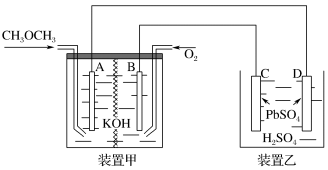
①甲装置中能量的转化形式主要为_______ 。
②写出乙装置中D极的电极反应式_______ 。
③当有46g二甲醚参加反应时,电路中通过的电子的数目为_______ 。
(2)钢铁锈蚀图如图丙所示:
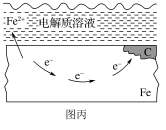
①钢铁锈蚀的负极反应式为_______ 。
②钢铁发生吸氧腐蚀的正极反应式为_______ 。
(3)我国的科技人员为了消除 的污染,利用原电池原理,变废为宝,设计由
的污染,利用原电池原理,变废为宝,设计由 和
和 来制备硫酸,设计装置如图丁所示,电极A、B为多孔的惰性材料,则A极为
来制备硫酸,设计装置如图丁所示,电极A、B为多孔的惰性材料,则A极为_______ (填“正极”或“负极”),B极的电极反应式是_______ 。

(1)图中甲装置为
 碱性燃料电池,其电极均为
碱性燃料电池,其电极均为 电极,装置乙中,C、D电极为
电极,装置乙中,C、D电极为 电极,其表面均覆盖着
电极,其表面均覆盖着 ,其电解液为稀
,其电解液为稀 溶液。
溶液。
①甲装置中能量的转化形式主要为
②写出乙装置中D极的电极反应式
③当有46g二甲醚参加反应时,电路中通过的电子的数目为
(2)钢铁锈蚀图如图丙所示:

①钢铁锈蚀的负极反应式为
②钢铁发生吸氧腐蚀的正极反应式为
(3)我国的科技人员为了消除
 的污染,利用原电池原理,变废为宝,设计由
的污染,利用原电池原理,变废为宝,设计由 和
和 来制备硫酸,设计装置如图丁所示,电极A、B为多孔的惰性材料,则A极为
来制备硫酸,设计装置如图丁所示,电极A、B为多孔的惰性材料,则A极为
您最近一年使用:0次
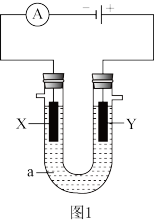
2 . 电解原理在化学领域应用广泛如图1表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请完成以下问题:
 +
+
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液:
①在X极附近观察到的现象是______________ ;_______ .
②电解一段时间后,该反应总离子方程式_______ ;
(2)若用该装置电解精炼铜,电解液a选用CuSO4溶液,则:X电极的材料是_______ ,电解一段时间后,CuSO4溶液浓度_______ (填“增大”、减小”或“不变”)。
(3)下列各情况,在其中Fe片腐蚀由快到慢的顺序是:____ ;

(4)如图, 水槽中试管内有一枚铁钉,放置数天观察:
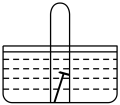
若试管内液面上升,则正极电极反应式为:______________________ 。
 +
+(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液:
①在X极附近观察到的现象是
②电解一段时间后,该反应总离子方程式
(2)若用该装置电解精炼铜,电解液a选用CuSO4溶液,则:X电极的材料是
(3)下列各情况,在其中Fe片腐蚀由快到慢的顺序是:

(4)如图, 水槽中试管内有一枚铁钉,放置数天观察:

若试管内液面上升,则正极电极反应式为:
您最近一年使用:0次
2023高三·全国·专题练习
3 . 钢铁工业是国家工业的基础,钢铁生锈现象却随处可见,为此每年国家损失大量资金。请回答下列问题:
(1)钢铁的电化学腐蚀原理:在酸性环境中发生析氢腐蚀,在中性或碱性环境中发生吸氧腐蚀。

①分别写出图1中铁电极和石墨电极的电极反应式:_______ ,_______ 。
②将该装置作简单修改即可成为钢铁电化学防护的装置,请在图1虚线框内所示位置做出修改,并用箭头标出导线中电子流动方向_____ 。
③写出修改后石墨电极的电极反应式:_______ 。
(2)工业上常用盐酸除去铁锈。现将一生锈的铁片放入盐酸中,溶液中可能发生反应的化学方程式有__________ 。
(3)在实际生产中,可在铁制品的表面镀铜防止铁被腐蚀。装置如图2所示:
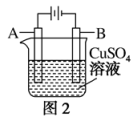
①A电极对应的金属是_______ (填元素名称),B电极的电极反应式为_______ 。
②若电镀前铁、铜两片金属质量相同,电镀完成后将它们取出洗净、烘干、称量,二者质量差为5.12g,则电镀时电路中通过的电子为_______ mol。
③镀层破损后,镀铜铁比镀锌铁更容易被腐蚀,请简要说明原因:_______ 。
(1)钢铁的电化学腐蚀原理:在酸性环境中发生析氢腐蚀,在中性或碱性环境中发生吸氧腐蚀。

①分别写出图1中铁电极和石墨电极的电极反应式:
②将该装置作简单修改即可成为钢铁电化学防护的装置,请在图1虚线框内所示位置做出修改,并用箭头标出导线中电子流动方向
③写出修改后石墨电极的电极反应式:
(2)工业上常用盐酸除去铁锈。现将一生锈的铁片放入盐酸中,溶液中可能发生反应的化学方程式有
(3)在实际生产中,可在铁制品的表面镀铜防止铁被腐蚀。装置如图2所示:

①A电极对应的金属是
②若电镀前铁、铜两片金属质量相同,电镀完成后将它们取出洗净、烘干、称量,二者质量差为5.12g,则电镀时电路中通过的电子为
③镀层破损后,镀铜铁比镀锌铁更容易被腐蚀,请简要说明原因:
您最近一年使用:0次
4 . Ⅰ.为探究原电池和电解池的工作原理,某研究性小组分别用如图所示装置进行实验。
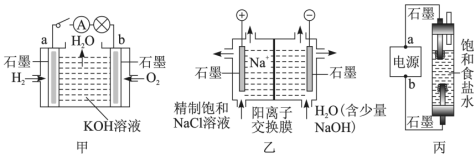
(1)甲装置中,a电极的反应式为___________ 。
(2)乙装置中,阴极区产物为___________ 。
(3)丙装置是一种家用环保型消毒液发生器。外接电源a为___________ (填“正”或“负”)极,该装置内发生反应的化学方程式为___________ 。
(4)若甲装置作为乙装置的电源,一段时间后,甲中消耗气体与乙中产生气体的物质的量之比为___________ (不考虑气体的溶解)。
Ⅱ.利用如图装置,可以模拟铁的电化学防护。
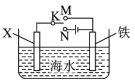
(5)若X为碳棒,为减缓铁的腐蚀,开关K应置于___________ 处。
(6)若X为锌,开关K置于M处,该电化学防护法称为___________ 。

(1)甲装置中,a电极的反应式为
(2)乙装置中,阴极区产物为
(3)丙装置是一种家用环保型消毒液发生器。外接电源a为
(4)若甲装置作为乙装置的电源,一段时间后,甲中消耗气体与乙中产生气体的物质的量之比为
Ⅱ.利用如图装置,可以模拟铁的电化学防护。

(5)若X为碳棒,为减缓铁的腐蚀,开关K应置于
(6)若X为锌,开关K置于M处,该电化学防护法称为
您最近一年使用:0次
2023-03-16更新
|
210次组卷
|
2卷引用:湖北省部分重点中学(武汉市,十堰市,襄阳市,恩施土家族苗族自治州)2022-2023学年高二下学期三月智学联合检测化学试题
解题方法
5 . 根据所学电化学知识填空。
(1)如图为锌铜原电池的装置示意图,其中盐桥内装有含饱和KCl溶液的琼胶。请回答下列问题:
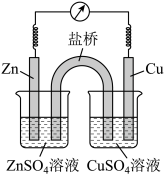
①Zn电极为电池的_______ (填“正极”或“负极”)。
②写出电极反应式:Zn电极_______ ,Cu电极_______ 。
③盐桥中向CuSO4溶液中迁移的离子是_______ (填离子符号)。
(2)金属腐蚀现象在生产生活中普遍存在,依据下列两种腐蚀现象回答下列问题:
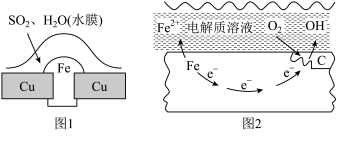
①图1中被腐蚀的金属为_______ (填化学式);图2中金属腐蚀类型属于_______ (填字母)。
A.化学腐蚀 B.析氢腐蚀 C.吸氧腐蚀
②图2中铁的生锈过程中正极反应式为_______ 。
(1)如图为锌铜原电池的装置示意图,其中盐桥内装有含饱和KCl溶液的琼胶。请回答下列问题:

①Zn电极为电池的
②写出电极反应式:Zn电极
③盐桥中向CuSO4溶液中迁移的离子是
(2)金属腐蚀现象在生产生活中普遍存在,依据下列两种腐蚀现象回答下列问题:

①图1中被腐蚀的金属为
A.化学腐蚀 B.析氢腐蚀 C.吸氧腐蚀
②图2中铁的生锈过程中正极反应式为
您最近一年使用:0次
6 . 回答下列问题:
(1)在一个小烧杯中加入20g 晶体和10g
晶体和10g  晶体,然后将小烧杯放在事先滴有3~4滴水的玻璃片上,立即用玻璃棒搅拌。实验过程的示意图如下:
晶体,然后将小烧杯放在事先滴有3~4滴水的玻璃片上,立即用玻璃棒搅拌。实验过程的示意图如下:
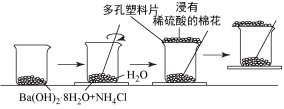
①实验中玻璃棒的作用:_______ 。
②浸有稀硫酸的棉花的作用:_______ 。
③出现结冰现象时,说明该反应为_______ 反应。
(2)沼气是一种廉价能源,农村存在大量的秸秆、杂草等废弃物,它们经微生物发酵之后,便可产生沼气,其主要成分是甲烷,可用来点火做饭。在农村推广建造沼气池,不仅能有效地利用_______ 能,还能为农业生产提供优良的肥料。已知:标准状况下,112.0L 气体完全燃烧生成
气体完全燃烧生成 和液态水时,放出4448kJ的热量。如果上述反应生成的是水蒸气,则反应放出的热量
和液态水时,放出4448kJ的热量。如果上述反应生成的是水蒸气,则反应放出的热量_______ 4448kJ(填“>”“<”或“=”)。
(3)钢铁中因含有碳,容易因构成原电池而发生电化学腐蚀。若在中性环境下,钢铁中少量的碳作为原电池的_______ 极,正极发生的电极反应式:_______ 。
(1)在一个小烧杯中加入20g
 晶体和10g
晶体和10g  晶体,然后将小烧杯放在事先滴有3~4滴水的玻璃片上,立即用玻璃棒搅拌。实验过程的示意图如下:
晶体,然后将小烧杯放在事先滴有3~4滴水的玻璃片上,立即用玻璃棒搅拌。实验过程的示意图如下:
①实验中玻璃棒的作用:
②浸有稀硫酸的棉花的作用:
③出现结冰现象时,说明该反应为
(2)沼气是一种廉价能源,农村存在大量的秸秆、杂草等废弃物,它们经微生物发酵之后,便可产生沼气,其主要成分是甲烷,可用来点火做饭。在农村推广建造沼气池,不仅能有效地利用
 气体完全燃烧生成
气体完全燃烧生成 和液态水时,放出4448kJ的热量。如果上述反应生成的是水蒸气,则反应放出的热量
和液态水时,放出4448kJ的热量。如果上述反应生成的是水蒸气,则反应放出的热量(3)钢铁中因含有碳,容易因构成原电池而发生电化学腐蚀。若在中性环境下,钢铁中少量的碳作为原电池的
您最近一年使用:0次
2023-03-11更新
|
223次组卷
|
2卷引用:湖南省长沙市湖南师大附中2022-2023学年高一下学期第一次月考化学试题
名校
7 . 铁、铜等金属及其化合物在生产和生活中有着广泛的应用。
(1)某研究性学习小组设计了如图所示装置探究钢铁的腐蚀与防护。

为防止金属Fe被腐蚀,可以采用上述_____ (填装置序号)装置原理进行防护;装置③中总反应的离子方程式为______ 。
(2)科学家制造出一种使用固体电解质的燃料电池,其效率更高,可用于航天航空。如图1所示装置中,以稀土金属材料作惰性电极,在电极上分别通入甲烷和空气,其中固体电解质是掺杂了Y2O3的ZrO2固体,在高温下能传导O2-。
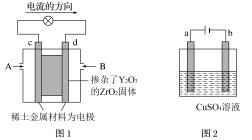
①图1中d电极上的电极反应式为______ 。
②如图2所示用惰性电极电解100mL0.50mol•L-1硫酸铜溶液,若要使电解质溶液恢复到电解前的状态,可加入______ (填字母)。
A.CuO B.Cu(OH)2 C.CuCO3 D.Cu2(OH)2CO3
(1)某研究性学习小组设计了如图所示装置探究钢铁的腐蚀与防护。

为防止金属Fe被腐蚀,可以采用上述
(2)科学家制造出一种使用固体电解质的燃料电池,其效率更高,可用于航天航空。如图1所示装置中,以稀土金属材料作惰性电极,在电极上分别通入甲烷和空气,其中固体电解质是掺杂了Y2O3的ZrO2固体,在高温下能传导O2-。

①图1中d电极上的电极反应式为
②如图2所示用惰性电极电解100mL0.50mol•L-1硫酸铜溶液,若要使电解质溶液恢复到电解前的状态,可加入
A.CuO B.Cu(OH)2 C.CuCO3 D.Cu2(OH)2CO3
您最近一年使用:0次
解题方法
8 . 材料是人类赖以生存与发展的重要物质基础。
(1)以下是生活中常见的物品:a.玻璃杯 b.电源插座 c.废旧干电池 d.废报纸 e.尼龙绳 f.轮胎 g.铁锅。请用相应的字母 填空:
①用无机非金属材料制作的是_______ 。
②用合成高分子材料中橡胶制作的是_______ 。
③随意丢弃会对水体和土壤都造成污染的是_______ 。
④如图所示,物品d可投入_______ (填“A”或“B”)标志的垃圾桶中。
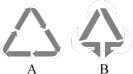
(2)经研究发现,长期使用铁锅炒菜,可有效减少缺铁性_______ 病症的发生,为了提高补铁效果,在炒菜时可经常加入适量的_______ (填“食醋”或“料酒”)。炒完菜之后不洗锅,铁锅通常会生锈,此过程中主要发生_______ 腐蚀(填“化学”或“电化学”),请写出金属防护的一种方法_______ 。
(1)以下是生活中常见的物品:a.玻璃杯 b.电源插座 c.废旧干电池 d.废报纸 e.尼龙绳 f.轮胎 g.铁锅。请用
①用无机非金属材料制作的是
②用合成高分子材料中橡胶制作的是
③随意丢弃会对水体和土壤都造成污染的是
④如图所示,物品d可投入
(2)经研究发现,长期使用铁锅炒菜,可有效减少缺铁性
您最近一年使用:0次
9 . 烧过菜的铁锅未及时洗净,第二天便出现红棕色锈斑(该锈斑为Fe(OH)3失水的产物),试用有关的电极反应式,离子方程式和化学方程式表示Fe(OH)3的生成:
(1)负极_______ ;
(2)正极_______ ;
(3)离子方程式_______ 。
(4)化学方程式_______ 。
(1)负极
(2)正极
(3)离子方程式
(4)化学方程式
您最近一年使用:0次
名校
解题方法
10 . 钢铁很容易生锈腐蚀,每年因腐蚀而损失的钢材占世界钢铁年产量的四分之一。因此,该小组同学又进行了钢铁腐蚀探究,希望能找到防止钢铁腐蚀的好办法。如图,U形管内为红墨水,a、b试管内分别盛有氯化铵溶液(显酸性)和食盐水,各加入生铁块,放置一段时间均被腐蚀。红墨水柱两边液面变为:左低、右高。
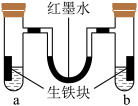
(1)请猜测a试管中铁发生的是________ (填“析氢”或“吸氧”)腐蚀。
(2)b管中生铁中碳上发生的电极反应式________________________ 。

(1)请猜测a试管中铁发生的是
(2)b管中生铁中碳上发生的电极反应式
您最近一年使用:0次



