1 . 化学是材料科学发展的基础。
(1)玻璃是一种常见的硅酸盐材料。制备普通玻璃的原料有CaCO3、_________ 和_________ (填化学式)
(2)①在下列材料中,属于新型硅酸盐材料的是_________ (填字母)。
a.硬币 b.聚氯乙烯塑料 c.氮化硅陶瓷 d.玻璃钢
②水泥是常用的建筑材料,它主要是以_________ 和黏土为原料制成。
③钢铁在潮湿的空气中主要发生的电化学腐蚀是_________ (填“析氢”或“吸氧”)腐蚀。
(1)玻璃是一种常见的硅酸盐材料。制备普通玻璃的原料有CaCO3、
(2)①在下列材料中,属于新型硅酸盐材料的是
a.硬币 b.聚氯乙烯塑料 c.氮化硅陶瓷 d.玻璃钢
②水泥是常用的建筑材料,它主要是以
③钢铁在潮湿的空气中主要发生的电化学腐蚀是
您最近一年使用:0次
解题方法
2 . 材料是人类赖以生存和发展的重要物质基础。
(1)试管、烧杯和烧瓶等化学仪器的主要材质是_________ 。
A.玻璃 B.陶瓷
(2)钢铁是目前用量最大的铁合金。钢铁接触海水发生电化学腐蚀,其负极反应式为_________ ;
A.O2+2H2O+4e-=4OH- B.Fe-2e-=Fe2+
(3)太阳能电池现已被广泛使用。生产太阳能电池主要用到的是_________ (填字母)。
A.晶体硅 B.石墨 C.金属锂
(4)钢铁是日常生活中使用最为广泛的金属,在潮湿的环境中易发生_________ (填“化学”或“电化学”)腐蚀,在铁制闸门上常嵌入_________ (填“铜块”、“锌块”)来保护闸门防止腐蚀。
(1)试管、烧杯和烧瓶等化学仪器的主要材质是
A.玻璃 B.陶瓷
(2)钢铁是目前用量最大的铁合金。钢铁接触海水发生电化学腐蚀,其负极反应式为
A.O2+2H2O+4e-=4OH- B.Fe-2e-=Fe2+
(3)太阳能电池现已被广泛使用。生产太阳能电池主要用到的是
A.晶体硅 B.石墨 C.金属锂
(4)钢铁是日常生活中使用最为广泛的金属,在潮湿的环境中易发生
您最近一年使用:0次
3 . 电化学知识在工业生产、科技研究中应用广泛。
Ⅰ.可采用电化学防护技术减缓海水中钢铁设施的腐蚀,下图是钢铁桥墩部分防护原理示意图。
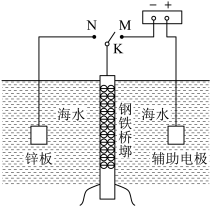
(1)K与M连接时钢铁桥墩的电化学防护方法为_______ ,K与N连接时,钢铁桥墩为_______ 极(填"正"、"负"、"阴"或"阳")
Ⅱ.利用电化学原理,将CO、O2和熔融K2CO3制成燃料电池,模拟工业电解法处理含Cr2O72-的废水,电解过程中溶液中发生如下反应:Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O。如下图所示:
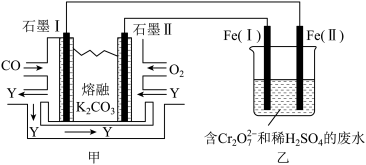
(2)甲池工作时,CO在石墨Ⅰ电极放电生成Y,Y可循环使用,甲池内的CO32-向_______ 移动(填“左”或“右”);石墨Ⅱ附近发生的电极反应式为_______ 。
(3)乙池中Fe(Ⅰ)的电极反应式为_______ 。
(4)甲池中消耗3.6molCO,最多可以处理含Cr2O
_______ mol的废水。
Ⅲ.某科研机构用NaOH溶液吸收硫酸工业废气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到某种副产物,其原理如图所示(电极材料均为石墨)。
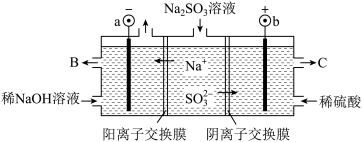
(5)稀NaOH溶液的作用是_______ ,阳极的电极反应式为_______ 。
Ⅰ.可采用电化学防护技术减缓海水中钢铁设施的腐蚀,下图是钢铁桥墩部分防护原理示意图。

(1)K与M连接时钢铁桥墩的电化学防护方法为
Ⅱ.利用电化学原理,将CO、O2和熔融K2CO3制成燃料电池,模拟工业电解法处理含Cr2O72-的废水,电解过程中溶液中发生如下反应:Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O。如下图所示:

(2)甲池工作时,CO在石墨Ⅰ电极放电生成Y,Y可循环使用,甲池内的CO32-向
(3)乙池中Fe(Ⅰ)的电极反应式为
(4)甲池中消耗3.6molCO,最多可以处理含Cr2O

Ⅲ.某科研机构用NaOH溶液吸收硫酸工业废气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到某种副产物,其原理如图所示(电极材料均为石墨)。

(5)稀NaOH溶液的作用是
您最近一年使用:0次
名校
解题方法
4 . 回答下列问题:
(1)钢铁工业是国家工业的基础,请回答钢铁腐蚀与防护过程中的有关问题。
①钢铁腐蚀主要是吸氧腐蚀,该腐蚀过程中正极的电极反应式为_______ 。
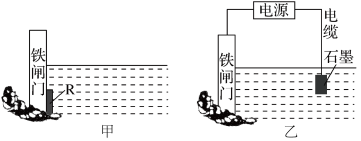
②为了降低某水库的铁闸门被腐蚀的速率,可以采用图甲所示的方案,其中焊接在铁闸门上的固体材料 可以采用
可以采用_______  填写字母序号
填写字母序号 。
。
A.铜 B.钠 C.锌 D.石墨
③图乙所示的方案也可以降低铁闸门的腐蚀速率,此种防护方法叫_______ 。
(2)在实际生产中,可在铁件的表面上镀铜防止铁被腐蚀。装置示意图如下图:
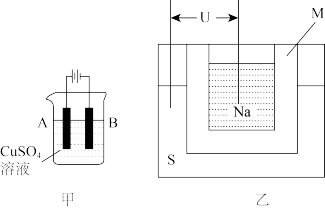
①甲图为电镀装置,镀件与电源的_______ 极连接,写出B电极反应式为_______ 。
② 图是一种钠硫高能电池的结构示意图,
图是一种钠硫高能电池的结构示意图, 由
由 和
和 制得,其作用是导电和隔膜,该电池总反应为
制得,其作用是导电和隔膜,该电池总反应为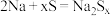 。该电池正极的电极反应式为
。该电池正极的电极反应式为_______ 。
(1)钢铁工业是国家工业的基础,请回答钢铁腐蚀与防护过程中的有关问题。

①钢铁腐蚀主要是吸氧腐蚀,该腐蚀过程中正极的电极反应式为
②为了降低某水库的铁闸门被腐蚀的速率,可以采用图甲所示的方案,其中焊接在铁闸门上的固体材料
 可以采用
可以采用 填写字母序号
填写字母序号 。
。A.铜 B.钠 C.锌 D.石墨
③图乙所示的方案也可以降低铁闸门的腐蚀速率,此种防护方法叫
(2)在实际生产中,可在铁件的表面上镀铜防止铁被腐蚀。装置示意图如下图:

①甲图为电镀装置,镀件与电源的
②
 图是一种钠硫高能电池的结构示意图,
图是一种钠硫高能电池的结构示意图, 由
由 和
和 制得,其作用是导电和隔膜,该电池总反应为
制得,其作用是导电和隔膜,该电池总反应为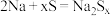 。该电池正极的电极反应式为
。该电池正极的电极反应式为
您最近一年使用:0次
2022-12-05更新
|
148次组卷
|
2卷引用:福建省福州市三校2022-2023学年高二上学期期中联考化学试题
解题方法
5 . 铝作为一种应用广泛的金属,在电化学领域也发挥着举足轻重的作用。回答下列问题:
(1)某同学根据氧化还原反应:2Al(s)+3Cu2+(aq)=2Al3+(aq)+3Cu(s),设计如图所示的原电池。
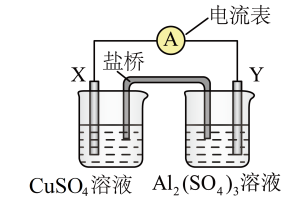
①两个电极一个是铜,一个是铝,电极X的化学式为_______ 。
②盐桥中的阴离子向_______ (填化学式)溶液中移动。
(2)新型电池中的铝电池类型较多。Li-Al/FeS是一种二次电池,可用于车载电源,其电池总反应为2Li+FeS=Li2S+Fe。放电时的正极反应式为_______ 。
(3)钢铁发生电化学腐蚀可分为析氢腐蚀和吸氧腐蚀,可以采用电化学手段进行防腐。
①写出钢铁在酸性较强的环境中发生电化学腐蚀的正极反应式:_______ 。
②为了减缓水库铁闸门被腐蚀的速率,可以采用下图乙所示的方案:

其中连接在铁闸门上的固体材料R可以采用_______ (填写字母序号)。
A.铜 B.钠 C.锌 D.石墨
(1)某同学根据氧化还原反应:2Al(s)+3Cu2+(aq)=2Al3+(aq)+3Cu(s),设计如图所示的原电池。

①两个电极一个是铜,一个是铝,电极X的化学式为
②盐桥中的阴离子向
(2)新型电池中的铝电池类型较多。Li-Al/FeS是一种二次电池,可用于车载电源,其电池总反应为2Li+FeS=Li2S+Fe。放电时的正极反应式为
(3)钢铁发生电化学腐蚀可分为析氢腐蚀和吸氧腐蚀,可以采用电化学手段进行防腐。
①写出钢铁在酸性较强的环境中发生电化学腐蚀的正极反应式:
②为了减缓水库铁闸门被腐蚀的速率,可以采用下图乙所示的方案:

其中连接在铁闸门上的固体材料R可以采用
A.铜 B.钠 C.锌 D.石墨
您最近一年使用:0次
6 . 根据下列四种电化学装置图,回答下列问题:
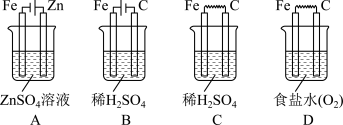
(1)装置名称:A____ 。
(2)装置A中Fe是____ 极;装置B中Fe是____ 极;装置D中Fe是____ 极。
(3)装置B、C相比较,其反应速率的大小关系是___ 。

(1)装置名称:A
(2)装置A中Fe是
(3)装置B、C相比较,其反应速率的大小关系是
您最近一年使用:0次
7 . 请通过上网搜索、查阅文献等方式,举例说明生产中应用的金属腐蚀防护措施___________ 。
您最近一年使用:0次
8 . 马口铁和白铁都是钢板表面有镀层的材料,前者表面镀锡,后者表面镀锌。试分析二者在以下两种情况下的抗腐蚀能力。
(1)表面镀层完好无损___________ 。
(2)表面镀层略有损伤___________ 。
(1)表面镀层完好无损
(2)表面镀层略有损伤
您最近一年使用:0次
解题方法
9 . 在空气中,如图所示的四种情况里,可以加速铁的腐蚀的是_______ ,可以阻止铁的腐蚀的是_______
A. B.
B. 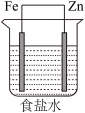 C.
C. 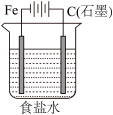 D.
D. 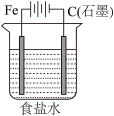
A.
 B.
B.  C.
C.  D.
D. 
您最近一年使用:0次
10 . 下图各烧杯中盛有等浓度的食盐水,铁在其中被腐蚀的速率由快至慢的顺序为_______ 。
A.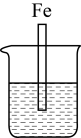 B.
B.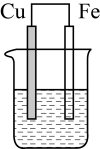 C.
C.
A.
 B.
B. C.
C.
您最近一年使用:0次



