10-11高二·江西·阶段练习
1 . 对金属制品进行抗腐蚀处理,可延长其使用寿命。
(1)以下为铝材表面处理的一种方法:
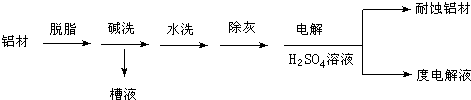
碱洗的目的是除去铝材表面的自然氧化膜,碱洗时常有气泡冒出,原因是______ (用离子方程式表示)。为将碱洗槽液中的铝元素以沉淀形式回收,最好向槽液中加入下列试剂中的____ 。
a.NH3 b.CO2 c.NaOH d.HNO3
(2)镀铜可防止铁制品腐蚀,电镀时用铜而不用石墨作阳极的原因是________ 。
(3)利用下图装置,可以模拟铁的电化学防护。
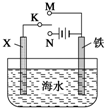
若X为碳棒,为减缓铁的腐蚀,开关K应置于______ 处。
若X为锌,开关K置于M处,该电化学防护法称为________ 。
(1)以下为铝材表面处理的一种方法:

碱洗的目的是除去铝材表面的自然氧化膜,碱洗时常有气泡冒出,原因是
a.NH3 b.CO2 c.NaOH d.HNO3
(2)镀铜可防止铁制品腐蚀,电镀时用铜而不用石墨作阳极的原因是
(3)利用下图装置,可以模拟铁的电化学防护。

若X为碳棒,为减缓铁的腐蚀,开关K应置于
若X为锌,开关K置于M处,该电化学防护法称为
您最近一年使用:0次
11-12高二上·山东·期中
2 . 如图所示装置中,甲、乙两个烧杯分别依次盛放200mL饱和食盐水、足量的AgNO3溶液,a、b、c、d四个电极均为石墨电极。接通电源,经过一段时间后,测得乙中d电极质量增加了2.16g。据此回答问题:
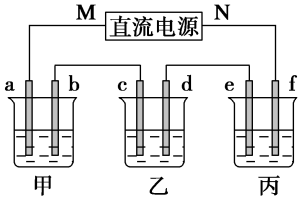
(1)电源的N端为________ 极;
(2)电极b上发生的电极反应为_______ ;
(3)电极c上生成的气体在标准状态下的体积:_______ ;
(4)甲溶液的氢氧根离子浓度为______ (设溶液体积仍为200mL);
(5)欲在丙烧杯中实现铁的表面镀上一层铜,则电解质溶液为_______ ,e电极的材料是:________ ,f电极的电极反应式为________ 。

(1)电源的N端为
(2)电极b上发生的电极反应为
(3)电极c上生成的气体在标准状态下的体积:
(4)甲溶液的氢氧根离子浓度为
(5)欲在丙烧杯中实现铁的表面镀上一层铜,则电解质溶液为
您最近一年使用:0次
3 . 写出下列反应的热化学方程式或电极反应式:
(1)N2(g)与H2(g)反应生成1molNH3(g),放出46.1kJ热量_____________________ 。
(2)钢铁发生吸氧腐蚀时的正极电极反应式________________________________ 。
(3)CH4与O2在酸性条件下形成原电池时,负极的电极反应式_______________ 。
(1)N2(g)与H2(g)反应生成1molNH3(g),放出46.1kJ热量
(2)钢铁发生吸氧腐蚀时的正极电极反应式
(3)CH4与O2在酸性条件下形成原电池时,负极的电极反应式
您最近一年使用:0次
11-12高二上·江苏盐城·期中
4 . 材料是人类赖以生存的重要物质基础。材料种类很多,通常可分为金属材料、无机非金属材料(包括硅酸盐材料)、高分子合成材料及复合材料。
(1) ①合金是生活中常见的材料。某合金具有密度小、强度高的优良性能,常用于制造门窗框架。该合金中含量最高的金属为____________ (填元素符号)。
②铁锈的主要成分是_____________ (填化学式),它是钢铁在潮湿的空气中发生______ 腐蚀的结果,其负极反应式为___________________ 。
③玻璃是一种常用的硅酸盐材料。制备普通玻璃的原料有CaCO3、_______ 和______ (填化学式)。
(2)聚苯乙烯是造成白色污染的物质之一,其结构简式为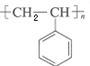 ,则制取聚苯乙烯的单体是
,则制取聚苯乙烯的单体是___________________ 。
(1) ①合金是生活中常见的材料。某合金具有密度小、强度高的优良性能,常用于制造门窗框架。该合金中含量最高的金属为
②铁锈的主要成分是
③玻璃是一种常用的硅酸盐材料。制备普通玻璃的原料有CaCO3、
(2)聚苯乙烯是造成白色污染的物质之一,其结构简式为
 ,则制取聚苯乙烯的单体是
,则制取聚苯乙烯的单体是
您最近一年使用:0次
5 . 金属的腐蚀是指金属与周围接触到的气体或液体物质发生________ 而引起损耗的现象。金属腐蚀的本质是________________ ,发生________ 反应。一般可分为________ 腐蚀和________ 腐蚀。
您最近一年使用:0次
11-12高二上·北京·期中
解题方法
6 . 如何防止铁的锈蚀是工业上研究的重点内容。为研究铁的锈蚀,某同学做了探究实验,如下图所示,铁处于①、②、③三种不同的环境中。请回答:
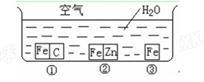
(1)铁被腐蚀的速率由快到慢的顺序是_____________________________ (填序号)。
(2)铁处于①环境时,正极反应式___________________________
(3)请你为以下钢铁制品选择适当的防锈方法。
①自行车的链条、齿轮___________________
②海水中的轮船___________________________

(1)铁被腐蚀的速率由快到慢的顺序是
(2)铁处于①环境时,正极反应式
(3)请你为以下钢铁制品选择适当的防锈方法。
①自行车的链条、齿轮
②海水中的轮船
您最近一年使用:0次
11-12高二上·甘肃兰州·期中
解题方法
7 . 烧过菜的铁锅未及时洗净,第二天便出现红棕色锈斑(该锈斑为Fe(OH)3失水的产物),试用有关的电极反应式,离子方程式和化学方程式表示Fe(OH)3的生成:
(1)负极_____________________ ;
(2)正极_______________ ;
(3)离子方程式____________________ ;
(4)化学方程式______________________ .
(1)负极
(2)正极
(3)离子方程式
(4)化学方程式
您最近一年使用:0次
8 . 原电池是化学对人类的一项重大贡献。某兴趣小组为研究原电池原理,设计如图装置:

(1)a和b用导线连接,Cu极为原电池_________ 极(填“正”或“负”),电极反应式为________________ Zn极发生_________ (填“氧化”或“还原”)反应。溶液中H+移向____________ (填“Cu”或“Zn”)极。
(2)无论a和b是否连接,Zn片均被腐蚀。若转移了0.2mol电子,则理论上Zn片质量减轻______ g。
(3)有同学想把Ba(OH)2•8H2O晶体与NH4Cl晶体的反应设计成原电池,你认为是否可行?_______ (填“是”或“否”),理由是____________________________ 。

(1)a和b用导线连接,Cu极为原电池
(2)无论a和b是否连接,Zn片均被腐蚀。若转移了0.2mol电子,则理论上Zn片质量减轻
(3)有同学想把Ba(OH)2•8H2O晶体与NH4Cl晶体的反应设计成原电池,你认为是否可行?
您最近一年使用:0次
2016-12-09更新
|
656次组卷
|
3卷引用:2014-2015学年重庆市七校高一下学期期中联考化学试卷
10-11高一下·辽宁沈阳·阶段练习
9 . 潜艇的金属外壳浸在海水中,在海水和空气的作用下会被腐蚀:
(1)若海水呈中性,一艘钢制外壳的潜艇在海水中发生腐蚀的电极反应式为:
正极:___________ ,负极:____________________ 。
(2)为有效地保护潜艇。下列措施中最好的是______________ (填序号)
A.采用纯铁制造潜艇外壳 B.采用耐腐蚀的合金制造潜艇外壳
C.在潜艇上涂一层油 D.在潜艇外壳上装一定数量的锌块
(1)若海水呈中性,一艘钢制外壳的潜艇在海水中发生腐蚀的电极反应式为:
正极:
(2)为有效地保护潜艇。下列措施中最好的是
A.采用纯铁制造潜艇外壳 B.采用耐腐蚀的合金制造潜艇外壳
C.在潜艇上涂一层油 D.在潜艇外壳上装一定数量的锌块
您最近一年使用:0次
10-11高一下·浙江嘉兴·期中
10 . 用化学用语填空:
(1)原子核内有8个质子和10个中子,则表示该核素的符号为__________
(2)二氧化碳的结构式______________ 。
(3)用石墨电极电解饱和食盐水的阳极的电极反应式___________________________ 。
(4)钢铁发生吸氧腐蚀时正极的电极反应式________________________________ 。
(1)原子核内有8个质子和10个中子,则表示该核素的符号为
(2)二氧化碳的结构式
(3)用石墨电极电解饱和食盐水的阳极的电极反应式
(4)钢铁发生吸氧腐蚀时正极的电极反应式
您最近一年使用:0次



